Image fluorescente montrant des cellules avec des nucléoles normaux (orange vif) dans des noyaux (violet) entourés de filaments d’actine (bleu foncé). Crédit : Image gracieuseté de Tamara Potapova, Gerton Lab, Stowers Institute for Medical Research
Les résultats pourraient potentiellement améliorer le taux de réussite du développement de médicaments contre le cancer.
Environ 90 % des médicaments n’arrivent pas sur le marché, ce qui souligne la nécessité évidente d’accroître l’efficacité du développement de médicaments. La situation n’est pas différente pour les médicaments destinés au traitement du cancer, dont beaucoup échouent pour diverses raisons. Aujourd’hui, des chercheurs ont révélé une raison pour laquelle certains composés anticancéreux peuvent provoquer des effets secondaires inattendus. Cette recherche pourrait aider à comprendre pourquoi certains médicaments sont plus prometteurs que d’autres, en fournissant un nouvel outil pouvant être utilisé pour identifier ces médicaments et candidats-médicaments.
L’un des processus cellulaires les plus essentiels et les plus énergivores est la biogenèse des ribosomes, la formation des machines cellulaires qui fabriquent toutes les protéines. Pour les cellules cancéreuses, ce processus est primordial. Une étude récente publiée dans la revue eLife du Stowers Institute for Medical Research a examiné plus de 1 000 médicaments anticancéreux existants pour évaluer leur impact sur la structure et la fonction du nucléole, l’organite cellulaire omniprésent où sont fabriqués les ribosomes.
« Toutes les cellules doivent fabriquer des protéines pour fonctionner, elles doivent donc fabriquer des ribosomes, qui sont également eux-mêmes des complexes protéiques », a déclaré l’auteur principal Tamara Potapova, Ph.D., spécialiste de recherche dans le laboratoire de la chercheuse Jennifer Gerton, Ph.D. « Dans les cellules cancéreuses, la production de ribosomes doit être accélérée pour compenser les taux de prolifération élevés nécessitant encore plus de protéines. »
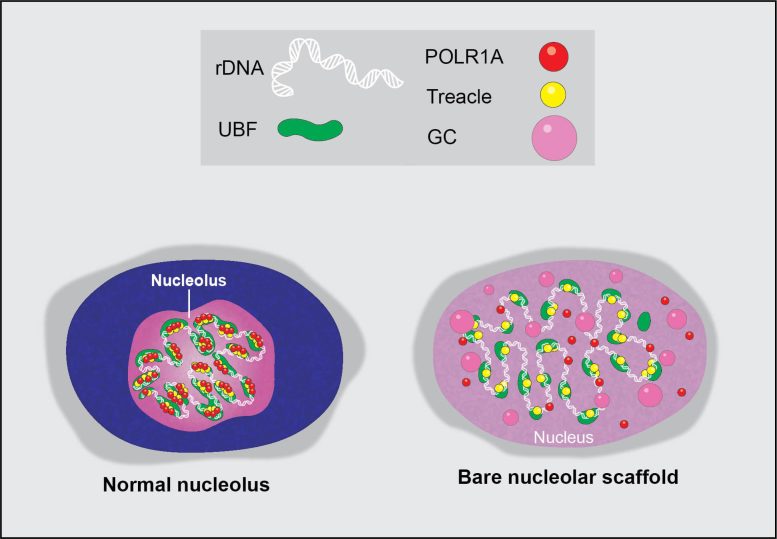
Illustration graphique d’un nucléole normal et de son état de stress extrême suite à l’inhibition de la kinase transcriptionnelle dépendante de la cycline par des agents de chimiothérapie. Crédit : Image gracieuseté de Mark Miller et Tamara Potapova, Stowers Institute for Medical Research
Le nucléole est une partie spéciale du noyau cellulaire qui abrite les ribosomes. ADNet où ribosomique ARN la production et l’assemblage des ribosomes ont lieu en grande partie. L’apparence des nucléoles peut varier considérablement et sert d’indicateurs visuels de l’état de santé général de ce processus. Ainsi, l’équipe a trouvé un moyen de capitaliser sur cette variation et a demandé quel impact les médicaments de chimiothérapie avaient sur le nucléole, provoquant un stress nucléolaire.
« Dans cette étude, nous avons non seulement évalué comment les médicaments anticancéreux modifient l’apparence des nucléoles, mais nous avons également identifié des catégories de médicaments provoquant des formes nucléolaires distinctes », a déclaré Gerton. « Cela nous a permis de créer un système de classification des nucléoles basé sur leur apparence, qui constitue une ressource que d’autres chercheurs peuvent utiliser. »
Parce que le cancer se caractérise par une prolifération incontrôlée, la plupart des agents chimiothérapeutiques existants sont conçus pour ralentir cette prolifération. « La logique était de voir si ces médicaments, intentionnellement ou non, affectent la biogenèse des ribosomes et dans quelle mesure », a déclaré Potapova. « Frapper la biogenèse des ribosomes pourrait être une arme à double tranchant : cela nuirait à la viabilité des cellules cancéreuses tout en modifiant simultanément la production de protéines dans les cellules normales. »
Différents médicaments ont un impact sur différentes voies impliquées dans la croissance du cancer. Ceux qui influencent la production de ribosomes peuvent induire des états distincts de stress nucléolaire qui se manifestent par des changements morphologiques facilement visibles. Cependant, le stress nucléolaire peut être difficile à mesurer.
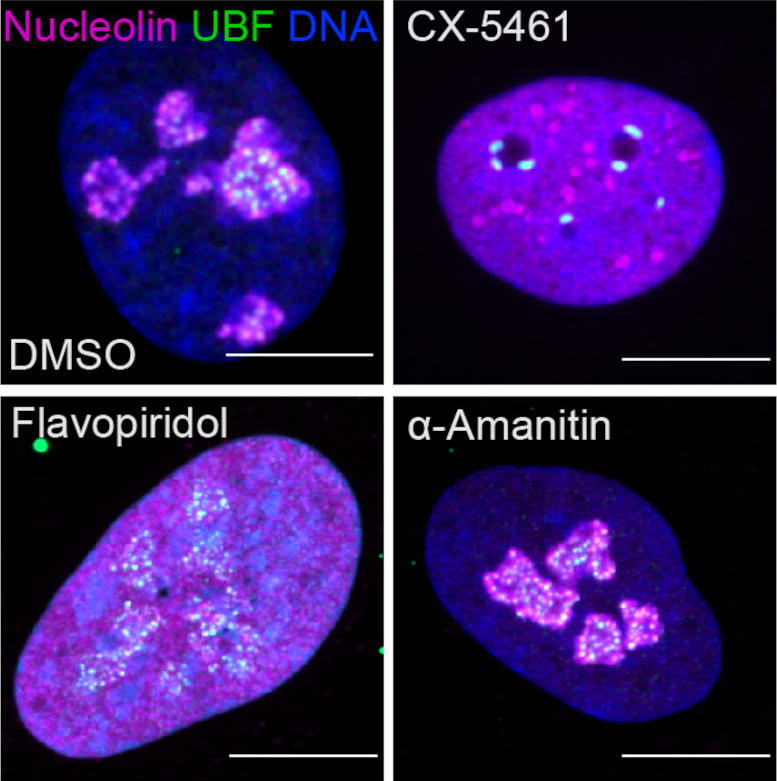
Images fluorescentes montrant le stress nucléolaire induit par des médicaments qui inhibent les enzymes transcriptionnelles ou les kinases dépendantes des cyclines (CDK). Le panneau supérieur gauche montre une cellule normale avec deux protéines nucléolaires importantes colorées (magenta et vert) et de l’ADN (bleu). Les panneaux restants montrent l’impact des CDK ou des médicaments inhibiteurs de transcription sur les nucléoles. Crédit : Image gracieuseté de Tamara Potapova, Gerton Lab, Stowers Institute for Medical Research
« C’est l’un des problèmes qui ont entravé ce domaine », a déclaré Potapova. « Les cellules peuvent avoir différents nombres de nucléoles de tailles et de formes différentes, et il a été difficile de trouver un paramètre unique capable de décrire pleinement un nucléole « normal ». Le développement de cet outil, que nous avons appelé « score de normalité nucléolaire », nous a permis de mesurer avec précision le stress nucléolaire, et il peut être utilisé par d’autres laboratoires pour mesurer le stress nucléolaire dans leurs modèles expérimentaux.
Grâce au criblage complet de composés anticancéreux sur le stress nucléolaire, l’équipe a identifié une classe d’enzymes en particulier, les kinases cyclines-dépendantes, dont l’inhibition détruit presque complètement le nucléole. Beaucoup de ces inhibiteurs ont échoué lors des essais cliniques et leur impact néfaste sur le nucléole n’avait pas été pleinement apprécié auparavant.
Les médicaments échouent souvent lors des essais cliniques en raison d’une toxicité excessive et involontaire qui peut être causée par leurs effets non ciblés. Cela signifie qu’une molécule conçue pour cibler une voie peut également avoir un impact sur une voie différente ou inhiber une enzyme nécessaire au fonctionnement cellulaire. Dans cette étude, l’équipe a constaté un effet sur un organite entier.
« J’espère qu’au minimum cette étude fera prendre conscience du fait que certains médicaments anticancéreux peuvent provoquer une perturbation involontaire du nucléole, qui peut être très importante », a déclaré Potapova. « Cette possibilité devrait être envisagée lors du développement de nouveaux médicaments. »
Ce travail a été financé par le soutien institutionnel du Stowers Institute for Medical Research.