Une nouvelle étude de l'Université hébraïque de Jérusalem publiée dans le Actes de l'Académie nationale des sciences Jette la lumière sur l'un des plus grands mystères de la vie: pourquoi la biologie est basée sur un ensemble très spécifique d'acides aminés, et en particulier pourquoi la nature a sélectionné les acides aminés alpha comme fondement des protéines.
La recherche, dirigée par le Dr Moran Frenkel-Pinter et les membres de son laboratoire Sarah Fisher et Yishi Ezerzer de l'Institut de chimie et du Center for Nanoscience and Nanotechnology de l'Université hébraïque, ont exploré les propriétés de Depsipeptides – des molécules de type peptide modèle.
Contrairement aux peptides modernes, les dépsipeptides contiennent un mélange de liaisons d'ester et d'amide, ce qui les rend plus faciles à se former dans des conditions prébiotiques mais moins stables au fil du temps.
Chaque organisme vivant sur Terre forme ses protéines à partir du même ensemble de 20 acides aminés. Pourquoi cet ensemble spécifique? La nouvelle étude suggère que la dépendance de la vie à l'égard de ces 20 acides aminés n'est pas un accident. Une question clé a intrigué les scientifiques depuis des décennies: pourquoi la vie privilégie les acides aminés alpha sur leurs homologues bêta ou gamma, même si tous étaient abondants sur la terre prébiotique?
Pour tester si l'assemblage moléculaire a joué un rôle, Frenkel-Pinter et son équipe ont synthétisé les dépsipeptides en utilisant une large gamme d'hydroxy et d'acides aminés, puis ont observé leur capacité à s'auto-assembler en solution.
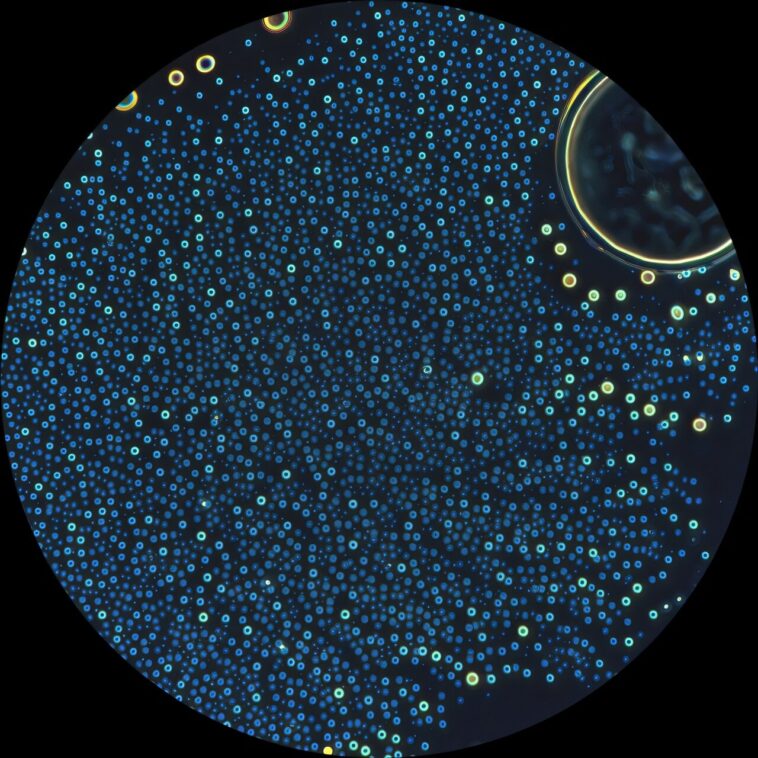
Les résultats étaient frappants. Les dépsipeptides construits à partir d'acides alpha ont facilement formé des assemblages stables en forme de gouttelettes qui ont persisté pendant des semaines, même après le gel et le dégel. En revanche, les assemblages bêta, s'ils sont formés, séparaient plus rapidement en phase en solution et présentaient une stabilité physique significativement plus faible. Cette différence, selon les chercheurs, aurait pu être un facteur décisif dans le «choix» évolutif de l'épine dorsale alpha.
« L'auto-assemblage est l'une des conditions les plus fondamentales de la vie », a déclaré le Dr Frenkel-Pinter. « Nos résultats suggèrent que la capacité supérieure des proto-peptides alpha à former des compartiments stables peut leur avoir donné un bord évolutif crucial, préparant le terrain pour les squelettes protéiques que nous voyons en biologie aujourd'hui. »
« La question de savoir pourquoi l'évolution a trié sur le volet un ensemble spécifique d'acides aminés est restée un mystère depuis très longtemps. Faire une seule étape pour répondre à cette question durable est remarquable, et il est un privilège de contribuer à cette poursuite », a déclaré Ezerzer, le co-frontant de ce projet avec Fisher.
« Nous démontrons ici, pour la première fois, la capacité des dépsipeptides à s'auto-assembler, similaires aux peptides modernes. Bien que ces résultats soient une percée dans le domaine de l'évolution chimique, ils peuvent également avoir des implications futures pour d'autres domaines tels que l'industrie pharmaceutique », a déclaré Fisher.
L'étude marque la première fois que les propriétés d'assemblage des squelettes alpha et bêta-peptide-peptide ont été directement comparées. En démontrant que la stabilité au niveau moléculaire aurait pu influencer l'évolution chimique, la recherche propose un modèle de sélection basé sur l'assemblage pour les premiers blocs de construction de la vie.
Ces résultats ajoutent une nouvelle dimension aux études d'origine de vie, ce qui suggère qu'il ne s'agissait pas seulement de la réactivité chimique, mais aussi de la capacité d'auto-assemblage durable qui a façonné la transition de la chimie prébiotique à la biologie.