Les chercheurs du Mont Sinaï ont identifié une voie allergique qui améliore l’immunité antitumorale dans le cancer du poumon. La combinaison de l’immunothérapie avec un médicament contre les allergies, le dupilumab, a donné lieu à une réduction significative des tumeurs dans une étude clinique, suggérant une nouvelle approche pour améliorer le traitement du cancer.
Une étude du Mont Sinaï a révélé que le blocage d’une voie allergique renforce l’immunité antitumorale dans le cancer du poumon, grâce à un médicament contre les allergies, le dupilumab, renforçant l’efficacité de l’immunothérapie chez les patients.
Des chercheurs de l’École de médecine Icahn du Mont Sinaï ont identifié une voie allergique qui, lorsqu’elle est bloquée, libère une immunité antitumorale chez des modèles murins de cancer du poumon non à petites cellules (CPNPC).
Et dans une première étude parallèle chez l’homme, associant l’immunothérapie au dupilumab—un anticorps bloquant les récepteurs de l’interleukine-4 (IL-4) largement utilisé pour traiter les allergies et l’asthme—a renforcé le système immunitaire des patients, un patient sur six ayant constaté une réduction significative de sa tumeur.
Les résultats ont été décrits dans le numéro du 6 décembre de Nature.
Améliorer l’efficacité de l’immunothérapie
« L’immunothérapie utilisant le blocage des points de contrôle a révolutionné le traitement du cancer du poumon non à petites cellules, la forme la plus courante de cancer du poumon, mais actuellement, seulement un tiers environ des patients y répondent seuls, et chez la plupart des patients, le bénéfice est temporaire », explique le senior. auteur de l’étude Miriam Merad, MD, PhD, directrice de l’Institut d’immunologie de précision Marc et Jennifer Lipschultz et directrice du département d’immunologie et d’immunothérapie de l’École de médecine Icahn du Mont Sinaï. « L’un des principaux objectifs de notre programme TARGET est d’utiliser la technologie unicellulaire et l’intelligence artificielle pour identifier les programmes immunitaires moléculaires capables d’atténuer la réponse immunitaire de la tumeur au blocage des points de contrôle. »
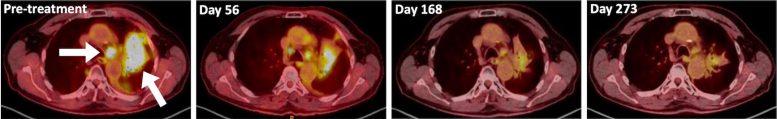
Scanners thoraciques montrant des tumeurs pulmonaires chez un patient atteint d’un cancer du poumon non à petites cellules métastatique avant et après avoir reçu du dupilumab avec une immunothérapie conventionnelle. Crédit : LaMarche et coll., Nature.
Également connu sous le nom d’inhibiteur de PD1, le blocage des points de contrôle est un type d’immunothérapie anticancéreuse qui peut libérer l’activité anticancéreuse des cellules T.
« En utilisant des technologies unicellulaires, nous avons découvert que les cellules immunitaires infiltrant les cancers du poumon, ainsi que d’autres cancers que nous avons étudiés, présentaient les caractéristiques d’une réponse immunitaire de « type 2 », qui est généralement associée à des affections allergiques comme eczéma et l’asthme », déclare le premier auteur de l’étude, Nelson LaMarche, PhD, chercheur postdoctoral dans le laboratoire du Dr Merad.
Essais cliniques prometteurs et orientations futures
« Ces résultats nous ont amenés à explorer si nous pouvions réutiliser un médicament généralement utilisé pour les affections allergiques afin de « sauver » ou d’améliorer la réponse tumorale au blocage des points de contrôle », déclare Thomas Marron, MD, PhD, directeur de l’unité d’essais de phase précoce à Tisch de Mount Sinai. Cancer Center et co-auteur principal de l’étude. « De manière frappante, nous avons constaté que le blocage de l’IL-4 améliorait la réponse du cancer du poumon au blocage des points de contrôle chez la souris et chez six patients atteints d’un cancer du poumon présentant une maladie résistante au traitement. En fait, un patient dont le cancer du poumon se développait malgré le blocage des points de contrôle a vu presque tout son cancer disparaître après avoir reçu seulement trois doses du médicament contre les allergies, et son cancer reste contrôlé aujourd’hui, plus de 17 mois plus tard.
Les chercheurs sont encouragés par les premiers résultats mais soulignent la nécessité de mener des essais cliniques plus vastes pour valider l’efficacité du médicament dans le traitement du CPNPC. Au-delà des résultats des essais cliniques rapportés dans la présente Nature Dans cet article, les enquêteurs ont maintenant élargi l’essai clinique, en ajoutant le dupilumab au blocage des points de contrôle pour un groupe plus large de patients atteints d’un cancer du poumon, et le Dr Marron a récemment reçu une subvention de l’Institut de recherche sur le cancer pour étudier également les effets sur le cancer du poumon à un stade précoce. . Grâce à ces essais, ils recherchent des biomarqueurs capables de prédire quels patients atteints de cancer pourraient bénéficier du traitement par dupilumab et lesquels ne le pourraient pas.
« Dans notre quête incessante de progrès, l’Institut de recherche sur le cancer (CRI) soutient fièrement l’équipe visionnaire de l’École de médecine Icahn du Mont Sinaï. Leurs résultats valident notre engagement à financer la recherche tout au long du continuum de la découverte, du laboratoire à la mise en œuvre clinique, grâce à une technologie et des données de pointe. Nous sommes impatients de voir notre soutien apporter un nouvel espoir en découvrant des voies permettant d’améliorer les réponses au blocus des points de contrôle. Nous défendons cette découverte et sommes fiers de faire partie de son parcours du laboratoire à la clinique, renforçant ainsi notre engagement à transformer des vies », déclare Jill O’Donnell-Tormey, PhD, PDG et directrice des affaires scientifiques au CRI.
Les auteurs restants, tous travaillant avec Icahn Mount Sinai, sauf indication contraire, sont Samarth Hegde, PhD ; Matthew D. Park, candidat MD/PhD ; Barbara B. Maier, PhD, Icahn Mount Sinai et Académie autrichienne des sciences, Vienne ; Léanna Troncoso ; Jessica Le Bérichel ; Pauline Hamon, PhD, Meriem Belabed, PhD ; Raphaël Mattiuz, PhD ; Clotilde Hennequin ; Théodore Chin ; Amanda M. Reid ; Ivan Reyes-Torres, PhD ; Erika Nemeth, MD, candidate au doctorat ; Ruiyuan Zhang (Université de Colombie); Oakley C. Olson, PhD (Université Columbia); Deborah B. Doroshow, MD, PhD ; Nicolas C. Rohs, MD ; Jorge E. Gomez, MD; Rajwanth Veluswamy, MD, MSCR ; Salle Nicole ; Nicholas Venturini, candidat MD/PhD ; Florent Ginhoux, PhD (Agence pour la Science, la Technologie et la Recherche, Singapour ; Campus du Cancer Gustave Roussy, France; École de médecine de l’Université Jiao Tong de Shanghai, Chine ; et SingHealth Duke–Institut d’immunologie translationnelle NUS, Singapour); Zhaoyuan Liu, PhD (École de médecine de l’Université Jiao Tong de Shanghai, Chine) ; Mark Buckup, candidat MD/PhD ; Igor Figueiredo; Vladimir Roudko, PhD ; Kensuke Miyake, PhD (Université médicale et dentaire de Tokyo, Japon) ; Hajime Karasuyama (Université médicale et dentaire de Tokyo, Japon) ; Edgar Gonzalez-Kozlova, PhD ; Sacha Gnjatic, Ph.D. ; Emmanuelle Passegué, Ph.D. (Université Columbia); Seunghee Kim-Schulze, PhD, Brian D. Brown, PhD ; Fred R. Hirsch, MD, PhD ; Brian S. Kim, MD, MTR, FAAD ; et Thomas U. Marron, MD, PhD.
L’étude a été financée par Instituts nationaux de la santé subventions CA257195, CA254104, CA154947, CA224319, DK124165, CA263705, CA196521, K00 CA223043, U01CA282114 et les subventions du Cancer Research Institute CRI3931 et CRI3617, ainsi que par une bourse de recherche Bristol Myers Squibb Irvington (CRI3 931) et un AACR-AstraZeneca Immuno 2021 -Bourse de recherche en oncologie (21-40-12-MATT).