L'eau est partout et se présente sous de nombreuses formes: neige, grésil, grêle, soarfrost, etc. Cependant, bien que l'eau soit si courante, les scientifiques ne comprennent toujours pas complètement le processus physique prédominant qui se produit lorsque l'eau se transforme du liquide en solide.
Maintenant, dans un article publié dans le Journal of Colloïd and Interface Sciencedes chercheurs de l'Institut des sciences industriels de l'Université de Tokyo, ont réalisé une série de simulations à l'échelle moléculaire pour découvrir pourquoi la glace se forme plus facilement sur les surfaces que dans les plans d'eau.
Bien qu'il soit de notoriété publique que l'eau gèle à 0 ° C (32 ° F), l'eau ne se transforme pas instantanément en glace au moment où cette température est atteinte. Au lieu de cela, les cristaux de glace commencent à se former à de minuscules « noyaux » et se propagent dans le corps d'eau dans un processus appelé nucléation. Les températures plus basses favorisent les événements de nucléation et accélèrent donc le processus de congélation. Bien que, au niveau microscopique, d'autres facteurs puissent également jouer un rôle.
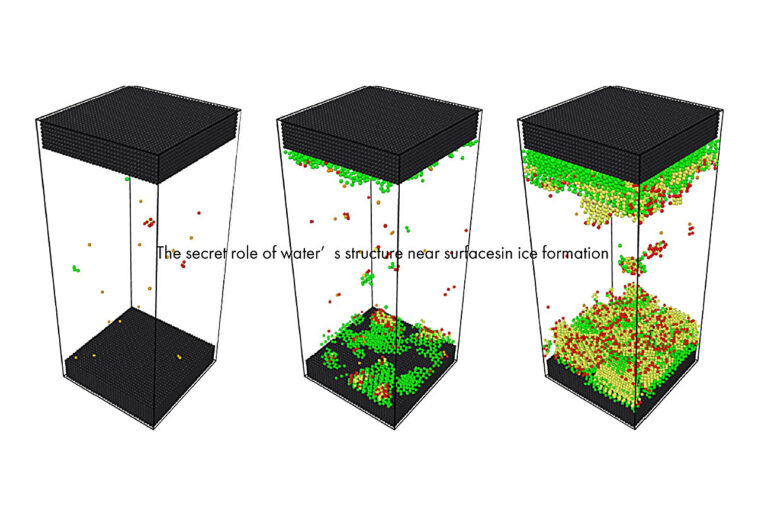
« Si vous regardez un verre de congélation d'eau, vous remarquerez que la glace se forme d'abord à l'interface eau-verre et se déplace progressivement vers l'intérieur », explique Gang Sun, auteur principal de l'étude. « Ainsi, il est clair que la façon dont les molécules d'eau interagissent avec les surfaces est importante pour le processus de nucléation. »
Pour comprendre les effets microscopiques responsables de la formation de glace, l'équipe a utilisé des simulations sophistiquées de dynamique moléculaire de pointe. Les simulations ont considéré de nombreux paramètres physiques, tels que la température et la force d'interaction intermoléculaire, mais on s'est démarqué comme particulièrement surprenant.

« La plupart des gens supposeraient que l'affinité d'une surface pour la glace dicte la voie de la nucléation », explique Hajime Tanaka, auteur principal.
« Cependant, nos simulations montrent que la disposition des molécules d'eau dans les deux couches les plus proches de la surface est encore plus importante. Cette superposition structurée favorise la formation d'un réseau de cristal hexagonal basse dimension à la surface, qui se propage ensuite en vrac. »
Cela dit, l'hydrophilie de la surface (la force avec laquelle il attire l'eau) reste un facteur clé. Une hydrophilie excessive perturbe l'ordre hexagonal bicouche des molécules d'eau, entravant la nucléation. Cependant, il existe une « zone Goldilocks » pour la formation de glace, où l'interaction de surface n'est ni trop forte ni trop faible pour interférer avec la cristallisation.
Ces connaissances confèrent aux chercheurs un outil avec lequel ils pourraient potentiellement contrôler la formation de glace, ce qui serait utile pour les revêtements anti-glace et autres matériaux. Le mécanisme proposé peut également s'appliquer à d'autres liquides avec d'autres liquides de liaison tétraédrique, tels que le silicium et le carbone.
Cela pourrait alors éclairer des domaines cruciaux tels que la science climatique et la fabrication de semi-conducteurs, où le contrôle des événements de nucléation a des applications sociétales et économiques.