Les fruits matures ou presque matures de Piper longum sont utilisés comme épices, appréciés pour leurs applications commerciales et industrielles, ainsi que dans la médecine traditionnelle chinoise pour leurs effets multiples, tels que la dissipation du froid et le soulagement des douleurs.
Compte tenu de leur longue histoire d'utilisation médicinale, les fruits de P. longum présentent une opportunité d'explorer leurs constituants thérapeutiques. Cependant, les composants chimiques des médicaments chinois traditionnels sont souvent complexes, faisant de la découverte efficace de nouveaux composés actifs une tâche difficile dans la recherche naturelle des produits.
Pour relever ce défi, une équipe de recherche dirigée par le professeur Haji Akber Aisa de l'Institut technique du Xinjiang de physique et de chimie de l'Académie chinoise des sciences isolée 12 énantiomères alcaloïdes dimériques avec des effets anti-inflammatoires et antidiabétiques de P. longum Freits utilisant une stratégie de déréplication basée sur le réseau moléculaire. Cette étude a été publiée dans le Journal of Agricultural and Food Chemistry.
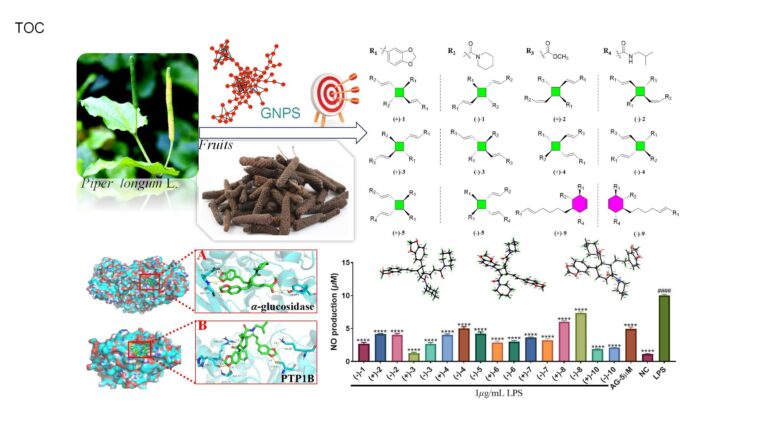
Les chercheurs ont créé un réseau moléculaire d'un extrait d'éthanol à 95% de fruits de P. longum en utilisant le module de mise en réseau moléculaire basé sur les fonctionnalités de la plate-forme GNPS (FBMN). Un cluster distinct a été identifié dans le réseau, qui comprenait des nœuds avec des poids moléculaires allant de 486.191 à 653.255 DA, mais qui ne correspondaient pas à des structures chimiques connues dans les bases de données publiques.
Un nœud spécifique dans ce cluster, avec un poids moléculaire de 627,3420 DA et correspondant à un dimère alcaloïde amide précédemment identifié de P. longum, nommé Piperchabamide H (M / Z 627.3428 (M + H) +), a servi de «molécule de graine», conduisant à l'isolement de 12 alcaloïdes amide dimère. Les chercheurs ont réussi à séparer ces 12 alcaloïdes amides dimériques en 12 paires d'énantiomères utilisant le HPLC chiral.
Les structures complètes de ces composés ont été élucidées à travers des données spectroscopiques complètes, des calculs de dichroïsme circulaire électronique (ECD) et une analyse de diffraction des rayons X. Les alcaloïdes amides dimériques identifiés comprenaient huit paires de dimères de type cyclobutane et quatre paires de dimères de type cyclohexène, avec cinq paires de nouveaux dimères de type cyclobutane et une paire d'un nouveau dimère de type cyclohexène.
Le dépistage de la bioactivité in vitro a révélé que trois composés présentaient des effets anti-inflammatoires notables dans un modèle de macrophage RAW 264.7 induit par le LPS. De plus, un composé a démontré une activité inhibitrice significative contre la α-glucosidase, tandis que trois composés ont montré une activité inhibitrice prometteuse contre la protéine tyrosine phosphatase-1B (PTP1B).
Pour étudier les mécanismes d'interaction entre ces alcaloïdes amides dimériques et les enzymes α-glucosidase et PTP1B, des études d'amarrage moléculaire ont été menées en utilisant les deux composés les plus actifs en tant que représentants. Les résultats ont indiqué que les deux composés formaient des complexes stables avec leurs protéines cibles respectives. D'autres simulations de dynamique moléculaire ont fourni des preuves supplémentaires soutenant la stabilité des complexes formés entre les composés actifs et les protéines correspondantes.
Cette étude met en évidence l'application potentielle de ces dimères alcaloïdes amides dans le développement des aliments fonctionnels et des produits pharmaceutiques, étendant ainsi les avantages favorables à la santé des fruits de P. longum.