Des chercheurs de Johns Hopkins Medicine ont identifié comment une mutation spécifique du gène de la rhodopsine provoque une cécité nocturne stationnaire congénitale en produisant un bruit électrique anormal qui désensibilise les cellules rétiniennes responsables de la vision nocturne. Leurs découvertes pourraient conduire à des traitements ciblés pour cette maladie qui intrigue les scientifiques depuis 30 ans. La recherche a utilisé des techniques d'enregistrement avancées pour surveiller les effets de la mutation à un niveau microscopique chez des souris génétiquement modifiées. Crédit : Issues.fr.com
Les scientifiques de Johns Hopkins ont identifié comment la mutation G90D du gène de la rhodopsine provoque la cécité nocturne, offrant ainsi des cibles thérapeutiques potentielles.
Dans ce qu'ils croient être une solution à un mystère biologique vieux de 30 ans, les neuroscientifiques de Johns Hopkins Medicine affirment avoir utilisé des souris génétiquement modifiées pour comprendre comment une mutation du gène de la rhodopsine, une protéine sensible à la lumière, entraîne une cécité nocturne congénitale stationnaire.
Cette maladie, présente dès la naissance, entraîne une mauvaise vision dans des environnements faiblement éclairés.
Les résultats, publiés le 14 mai dans Actes de l'Académie nationale des sciencesdémontrent que la mutation du gène de la rhodopsine, appelée G90D, produit un « bruit » électrique de fond inhabituel qui désensibilise les bâtonnets de l'œil, ces cellules de la rétine situées au fond de l'œil responsables de la vision nocturne, provoquant ainsi la cécité nocturne.
L'identification de cette activité électrique inhabituelle pourrait « fournir de futures cibles pour des interventions thérapeutiques », écrivent les auteurs de l'étude.
Ces événements électriques pourraient aider les scientifiques à mieux comprendre le fonctionnement des bâtonnets et des cônes de l'œil, explique King-Wai Yau, Ph.D., professeur au département de neurosciences de la faculté de médecine de l'université Johns Hopkins.
Méthodologie de recherche et observations
La recherche a été dirigée par Yau et le boursier postdoctoral Zuying Chai.
« On sait que la mutation G90D de la rhodopsine produit un bruit électrique de fond pour désensibiliser les bâtonnets, mais la nature du « bruit » et sa source moléculaire précise n'ont pas été résolues depuis près de 30 ans », explique Yau. « Nous avons pu contribuer à résoudre le mécanisme de cette maladie avec un modèle murin présentant un très faible niveau d’expression de rhodopsine G90D. »
En comparant le faible niveau d'expression de G90D observé chez des souris génétiquement modifiées par rapport au niveau de G90D observé chez des patients humains atteints de cécité nocturne, les auteurs ont conclu que l'activité électrique inhabituelle de faible amplitude mais de fréquence extrêmement élevée pourrait être le principal contributeur à la cécité nocturne. maladie chez les gens.
Outre le bruit électrique inhabituel, la rhodopsine est connue pour produire un autre type d'activité électrique appelé isomérisation thermique spontanée, dans laquelle l'énergie thermique à l'intérieur de la molécule de rhodopsine déclenche l'activation aléatoire de la rhodopsine. Contrairement à l'activité électrique inhabituelle observée, l'isomérisation spontanée de la rhodopsine G90D a démontré une amplitude élevée mais une fréquence basse. Dans leurs expériences, les chercheurs ont découvert que le taux d’isomérisation spontanée de la rhodopsine G90D est environ deux cents fois supérieur à celui de la rhodopsine normale, mais que leur effet d’adaptation des bâtonnets n’est pas suffisamment élevé pour contribuer de manière significative à la cécité nocturne chez l’homme.
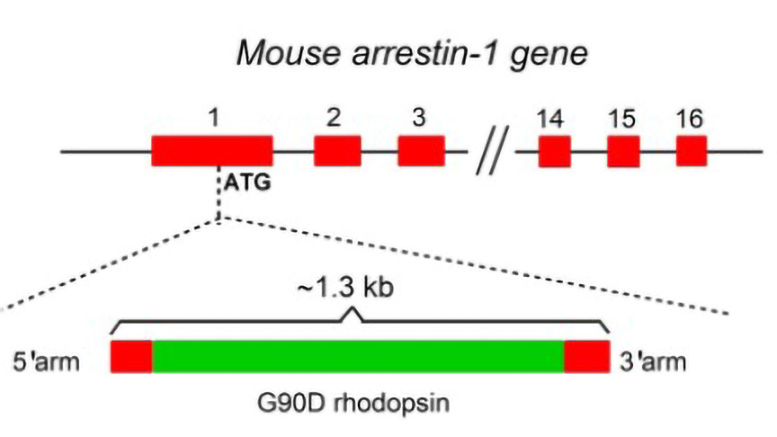
Crédit : Laboratoire King-Wai Yau
Dans la plupart des cas, les bâtonnets sont très sensibles à la lumière, mais chez les personnes atteintes de cécité nocturne, les bâtonnets ne peuvent pas détecter avec précision les changements de lumière et ne fonctionnent pas dans l'obscurité. Les personnes atteintes de cette maladie ont besoin d'une lumière plus vive pour voir dans des environnements faiblement éclairés, a déclaré Yau.
Pendant des décennies, même si les chercheurs connaissaient la mutation G90D, ils avaient du mal à déterminer comment elle provoquait la cécité nocturne, car les modèles de souris antérieurs présentant cette mutation généraient un niveau élevé de bruit de fond, produisant des effets similaires à la lumière de fond, auxquels les bâtonnets de la souris s'adaptent rapidement. . Cela a rendu difficile pour les chercheurs de mesurer avec précision les effets de signalisation de la mutation.
Pour contourner ce problème, les chercheurs de Johns Hopkins Medicine ont génétiquement modifié des souris pour avoir une faible expression de G90D, un niveau égal à 0,1 % de la rhodopsine normale trouvée dans la population naturelle de souris.
Cela a permis aux chercheurs de distinguer les différents types d’activité produits chez les souris porteuses de la mutation G90D, comme si peu ou pas de lumière de fond équivalente était présente.
Les scientifiques ont utilisé une méthode à haute résolution pour enregistrer l'activité électrique de bâtonnets individuels dans la rétine de la souris, à laquelle ils ont accédé avec une pipette en verre ultra-mince – la largeur d'environ un soixante-dixième de la taille d'un cheveu humain – remplie d'une solution saline. solution capable de conduire l’électricité.
Techniques avancées en recherche neuroscientifique
« Vous pouvez réellement voir ces événements », explique Yau. « Nous avons utilisé une technique très spéciale appelée enregistrement par aspiration pour enregistrer l'activité à une résolution si élevée que si une molécule de rhodopsine s'isomérise ou s'active, nous pouvons la voir, car elle provoque un changement de courant électrique. »
G90D est l'une des quatre mutations de la rhodopsine associées à la cécité nocturne. Le premier auteur, Chai, explique que les prochaines étapes consisteront à identifier comment d'autres mutations de la rhodopsine, T94I, A292E et A295V, conduisent à cette maladie.
« Le mécanisme à l'origine de la cécité nocturne G90D pourrait être similaire dans les trois autres mutations de la rhodopsine à l'origine de cette maladie », explique Chai.
Parmi les autres scientifiques qui ont contribué à la recherche figurent Yaqing Ye, Daniel Silverman et Randall Reed de Johns Hopkins, ainsi que Kasey Rose, Alana Madura et Jeannie Chen de l'Université de Californie du Sud. Le financement de l'étude a été assuré par le Instituts nationaux de la santé subvention EY006837, le António Champalimaud Vision Award, Portugal, le Multiphoton Imaging Core de Johns Hopkins, le Daniel Nathans Scientific Innovator Award de la faculté de médecine de l'Université Johns Hopkins et le Beckman-Argyros Vision Award de la Fondation Arnold et Mabel Beckman.




