La découverte de médicaments peut être un processus long et complexe. Les médicaments pour les maladies neurodégénératifs comme la maladie d'Alzheimer sont parmi les plus coûteux à développer, car les résultats du modèle animal ne se sont pas avérés prédictifs de l'efficacité chez l'homme. Les scientifiques doivent généralement filtrer de nombreuses cibles biologiques avant d'identifier un seul nouveau médicament potentiel.
Des chercheurs de l'Université Carnegie Mellon développent une plate-forme pour permettre le dépistage des médicaments à haut débit. Leur travail fait partie des efforts pour optimiser chaque élément du processus de découverte de médicaments, avec des impacts réels dans la course pour traiter les patients.
Anne Skaja Robinson étudie les récepteurs couplés à la protéine G (GPCR), les protéines qui résident à la surface de la cellule. Ils sont la cible de nombreux médicaments à petite molécule, y compris les thérapies pour le diabète, les allergies et le cancer. Le laboratoire Robinson se concentre sur le rôle de ces protéines transmembranaires et leurs réponses cellulaires en aval. Un côté d'un GPCR fait face à la cellule, où il est associé à une protéine G. L'autre côté d'un GPCR est à l'extérieur de la cellule, où un médicament peut se lier; Ainsi, ils servent de capteurs à l'environnement d'une cellule.
« Il y a beaucoup de potentiel thérapeutique inexploité », explique Sarah Sonbati. Il y a 800 GPCR connus, mais les médicaments actuels en ciblent moins de 15%.
L'écart dans les traitements de la maladie existe parce que les scientifiques ne savent pas encore ce qui se lie à certains GPCR. L'identification de petites molécules pour activer ces GPCR orphelins (OGPCR) est un chemin vers de nouveaux médicaments possibles.
La maladie d'Alzheimer est particulièrement intéressante car les scientifiques savent qu'il y a une régulation positive, ou une augmentation, des GPCR spécifiques chez les personnes atteintes de la maladie. Il n'y a pas non plus de remède encore. « Et si nous commençons à regarder la cause profonde de la maladie d'Alzheimer, et que nous essayons de cibler cela? » demande à Sonbati, un doctorat en génie chimique. étudiant. « La réponse peut être dans les GPCR et comprendre comment un GPCR est activé. »
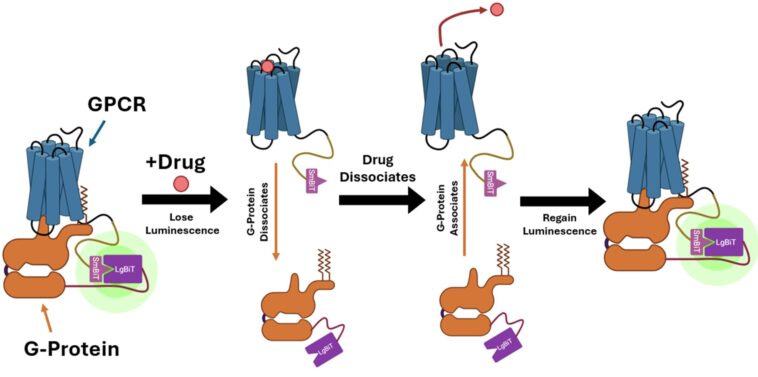
Lorsqu'un médicament se combine avec le GPCR à l'extérieur de la membrane cellulaire, la protéine G à l'intérieur de la cellule se dissocie. Sonbati a mis à profit ce changement d'association pour créer un biocapteur qui utilise la bioluminescence pour détecter le couplage des GPCR et des protéines G.
« Notre plateforme permet une détection plus spécifique de l'activation des protéines elle-même et dans un contexte cellulaire », explique Robinson, professeur de génie chimique. Robinson et Sonbati ont développé leur test basé sur les cellules à partir d'un système existant qui utilise une enzyme spécifiquement conçue pour fournir une luminescence transitoire, basée sur la lumière émise par les lucioles. L'enzyme luciférase est divisée en un peu et un grand morceau, chacune attachée à une protéine. Lorsque les deux protéines interagissent, les bits de luciférase sont suffisamment proches pour reconstituer la fonction et l'éclat.
Sonbati a optimisé l'approche en utilisant un GPCR que le laboratoire Robinson a travaillé de manière approfondie, l'adénosine A2A récepteur. « Nous devions comprendre à quoi ressemblaient les données dans un système bien caractérisé, comprendre ce qu'il nous dit sur les interactions dans la cellule, avant d'entrer dans cet espace inconnu des GPCR orphelins », explique Sonbati.
Les médicaments qui activent un2A sont connus. Sonbati a examiné deux classes de médicaments: les agonistes, qui régulent à la hausse l'activité des récepteurs; et les agonistes inverses, qui régulent à la baisse l'activité des récepteurs. Initialement, le A2A est déjà lié, ou «pré-couplé», avec la protéine G, créant une bioluminescence même dans un état de repos dans la cellule. Lorsqu'un agoniste est ajouté, le GPCR et la protéine G doivent se dissocier et le capteur ne doit plus montrer de luminescence. Les résultats de Sonbati ont confirmé ce comportement de la protéine témoin.
Lorsqu'un agoniste inverse est ajouté, la protéine G est recrutée au GPCR et la luminescence augmente à nouveau. « Ces résultats nous ont aidés à comprendre que nous ne nous attendons pas toujours à voir une diminution de la luminescence. Nous recherchons des changements par rapport à l'état initial, ce qui nous donnera plus d'informations sur notre capteur », explique Sonbati.
Après avoir optimisé le type de cellule, la densité et les méthodes de transfection, Sonbati a réussi à appliquer la plate-forme à deux GPCR orphelins qui sont régulés à la hausse dans la maladie d'Alzheimer. « Personne n'a pu les regarder avant de cette manière », dit-elle.
Le capteur a également confirmé que les deux GPCR orphelins sont pré-couplés à la protéine G, comme un2A est. Ils n'ont pas besoin d'une autre molécule pour interagir ou activer les fonctions dans la cellule. « Cela signifie tout ce que nous avons appris sur la luminescence avec un2A peut être appliqué dans cet espace « , explique Sonbati.
Le Robinson Lab teste désormais une bibliothèque de 700 drogues des National Institutes of Health (NIH) pour voir si cela active les GPCR orphelins avec lesquels ils travaillent. Sonbati a également conçu des constructions pour passer leur plate-forme des cellules de mammifères à la levure. La levure se développe plus rapidement et est plus robuste, permettant plus d'expériences et des résultats plus rapides.
La plate-forme de Robinson et Sonbati est un outil puissant pour tester et comprendre l'activation du GPCR. Il est plus rapide et moins cher que les méthodes traditionnelles.
« Notre vision est d'appliquer cela plus généralement pour le dépistage des médicaments à haut débit », explique Sonbati. « Imaginez une plaque de puits avec notre capteur dans chaque petit puits. Vous ajoutez un médicament potentiel différent à chaque puits. Tous les puits commencent à briller, ce qui signifie que les protéines interagissent, à l'exception de celle. Le médicament dans ce puits est celui que vous voulez regarder plus loin. »
En combinant ces outils avec les technologies d'apprentissage automatique émergentes, Robinson et Sonbati espèrent ouvrir de nouvelles voies pour des cibles médicamenteuses pour la maladie d'Alzheimer et d'autres maladies qui ont été moins traitables pour le traitement.