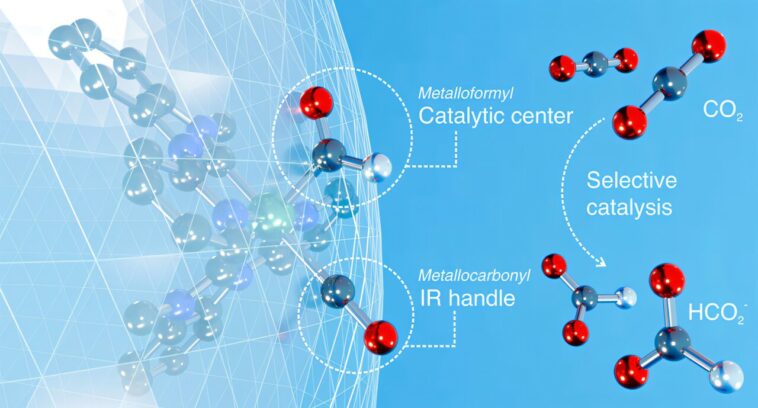
Les chimistes du laboratoire national de Brookhaven du Département américain de l'énergie (DOE) ont conçu une nouvelle façon de convertir un dioxyde de carbone abondant (CO (CO2) en formate (HCO2–), un produit chimique industriel utilisé comme carburant, comme agent antibactérien / antifongique, et pour fabriquer des produits pharmaceutiques. Leur réaction utilise un catalyseur centré sur le métal activé par la lumière pour faciliter le transfert d'électrons et de protons nécessaires à la conversion chimique.
« Nous prenons quelque chose de bon marché et d'abondant comme du CO2 et l'ajout d'électrons et de protons pour le convertir en quelque chose d'utile « , a déclaré Sai Puneet Desai, l'auteur principal d'un article décrivant la recherche qui vient de publier dans le Journal de l'American Chemical Society.
À certains égards, le processus imite la photosynthèse, la série de réactions que les plantes utilisent pour convertir CO2 et l'eau en sucre, leur principale source de carburant. « Dans notre réaction et notre photosynthèse, le transfert de protons et d'électrons est favorisé directement ou indirectement par la lumière », a déclaré Desai.
« Vous pouvez le considérer comme le stockage de l'énergie lumineuse dans les liaisons chimiques », a ajouté la co-auteur Andressa Müller.
L'ajout de ligands ajoute le contrôle
Par rapport à d'autres tentatives pour convertir CO2 Aux produits chimiques utiles, la méthode développée par Desai, Müller et d'autres membres du groupe de photosynthèse artificiel de Brookhaven Lab ont une torsion – ou plutôt une extension.
« Généralement, dans ces types de CO2 conversions, vous devez lier le CO2 à un centre métallique sur le catalyseur « , a déclaré le chef de groupe Javier Concepcion. » Cela signifie qu'il existe des espaces vides pour que d'autres molécules concurrentes entrent et réagissent avec le métal. Cela peut conduire à la décomposition du catalyseur, et cela limite la sélectivité sur le type de produits que vous pouvez fabriquer. «
Pour contrôler la sélectivité et éviter les réactions secondaires indésirables, l'équipe a entouré son centre métallique avec des ligands.
« Le catalyseur est comme une fleur: le métal est le centre de la fleur et les pétales sont les ligands », a déclaré Müller. « Nous pouvons régler les propriétés du catalyseur avec ces ligands, et toute la chimie se déroule à l'un des ligands plutôt que sur le métal. »
Dans ce nouveau mécanisme, tous les sites de liaison sur le métal sont occupés, de sorte que le métal est entièrement protégé contre les réactions secondaires indésirables. Et en concevant précisément les ligands, les scientifiques peuvent contrôler soigneusement le produit.
« Ce mécanisme est très sélectif; seul le formate est produit », a déclaré Concepcion. « Souvent, il y a une concurrence pour fabriquer de l'hydrogène et / ou la fabrication de monoxyde de carbone, et parfois il est difficile de contrôler lesquels de ces produits que vous créez. Mais pour fabriquer ces produits, vous avez besoin de sites ouverts au centre métallique. Dans ce cas, parce que le mécanisme est basé sur le ligand, il n'y a aucune chance que ces autres produits soient générés. »
De plus, Müller a noté: « Étant donné que la chimie se produit sur les ligands et non sur le métal, cela ouvre la possibilité d'utiliser d'autres métaux au cœur du catalyseur. »
Le document actuel rapporte les résultats avec un catalyseur centré sur le ruthénium. Mais les scientifiques ont essayé une approche similaire en utilisant des métaux peu coûteux comme le fer et ont constaté que cela fonctionne également bien.
« Cet article démontre que cette stratégie basée sur le ligand est généralisable à d'autres métaux », a déclaré Concepcion. « Notre objectif est de se déplacer vers les métaux abondants de la Terre. Il ne devient pas plus abondant que le fer! »
Calcul, les expériences contribuent des informations clés
Les scientifiques se sont fortement appuyés sur la théorie et la chimie informatique, à la fois au stade de conception du catalyseur et pour les aider à comprendre leur mécanisme de réaction.
« Nous avons essentiellement étudié l'ensemble du mécanisme en utilisant la théorie fonctionnelle de la densité, une technique de calcul qui utilise une série de calculs basés sur la densité électronique pour aider à déterminer les arrangements et les interactions les plus probables des atomes », a ajouté Mehmed Ertem, un chercheur principal dans le groupe qui se spécialise en chimie informatique. « La modélisation a révélé toutes les étapes par lesquelles les électrons et les protons sont capturés pour transformer le catalyseur en sa forme active et comment le catalyseur livre finalement ces électrons et protons pour transformer CO2 en formate. «
« Le mécanisme est très simple », a déclaré Desai. « Il commence par un photosensibilisateur, qui absorbe la lumière et agit comme un relais pour les électrons dans notre système catalytique. »
Le système comprend une autre molécule organique appelée organohydride, qui contribue à la fois les électrons et les protons en deux étapes distinctes. Cette étude a détecté l'existence d'un « cation radical » de l'organohydride, qui se forme comme intermédiaire après l'étape de don d'électrons. Cet intermédiaire est essentiel pour le don de protons ultérieur qui transforme le catalyseur en sa forme active.
Surtout, une fois les électrons et les protons livrés au CO2tous les composants du système peuvent revenir à leurs formulaires d'origine pour être à nouveau utilisés.
« Cette recyclabilité est vraiment importante car nous voulons rendre ce système aussi efficace que possible et nous ne voulons pas introduire les déchets », a déclaré Desai.
Les scientifiques ont également mené des expériences de laboratoire pour vérifier les prédictions basées sur la théorie et suivre les composantes de réaction en temps réel. Un résultat clé était la preuve que l'intermédiaire de cation radical « a vécu » assez longtemps pour s'engager dans la réaction. Ces résultats proviennent de l'installation de l'accélérateur d'électrons laser (FELD) dans la division de chimie de Brookhaven Lab, qui combine des impulsions très courtes d'électrons et de lumière laser pour produire, exciter et examiner les espèces moléculaires et atomiques transitoires avec une résolution temporelle élevée.
« Auparavant, les gens pensaient que les cations radicales de ces organodydrides étaient des espèces de très courte durée qui ne pouvaient pas rester trop longtemps », a déclaré Concepcion. « Nous avons utilisé des feuilles pour démontrer qu'ils peuvent survivre pour des centaines de microsecondes, ce qui semble à court d'échelles de temps ordinaires mais est plutôt longue pour la chimie. »
L'équipe a également utilisé un instrument à rayons X monocristallins dans la division de chimie pour étudier la structure des catalyseurs. Les techniques laser disponibles à la Division de la chimie ont également été utilisées pour comprendre toutes les étapes de la conversion du CO2 former.
« Ces installations et outils nous ont permis d'étudier des processus qui se déroulent sur des nanosecondes, des microsecondes et des délais encore plus longs », a déclaré Concepcion. « Nous pouvons voir ce qui se passe à partir du moment où la lumière est introduite et suivre tous les processus chimiques sur tout le cycle catalytique. »