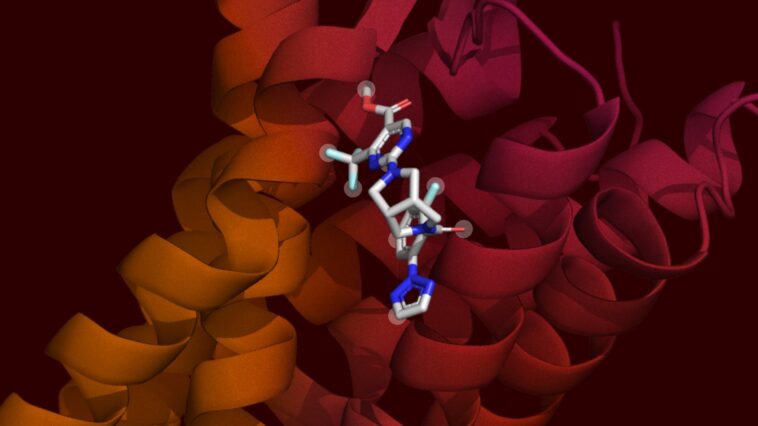
Comprendre comment les molécules interagissent est au cœur de la biologie: du décodage du fonctionnement des organismes vivants pour découvrir les mécanismes de la maladie et développer des médicaments vitaux. Ces dernières années, des modèles comme Alphafold ont changé notre capacité à prédire la structure 3D des protéines, offrant des informations cruciales sur la forme et l'interaction moléculaires.
Mais alors qu'Alphafold pouvait montrer comment les molécules s'adaptent, il ne pouvait pas mesurer la force de leur liaison – un facteur clé pour comprendre toutes les propriétés susmentionnées. Cette pièce manquante est l'endroit où le nouveau modèle d'IA du MIT, Boltz-2, entre en jeu.
Boltz-2 brise un nouveau sol en modélisant conjointement à la fois la structure et l'affinité de liaison, un paramètre critique dans la découverte de médicament à petites molécules. Le module d'affinité de Boltz-2 a été formé sur des millions de mesures de laboratoire réelles, montrant à quel point les molécules différentes se lient aux protéines. Grâce à cela, Boltz-2 peut désormais prédire la force de liaison avec une précision sans précédent dans plusieurs repères reflétant différentes étapes de découverte de médicaments réels.
Dans les références établies, les prédictions de Boltz-2 se rapprochent de celles produites par une perturbation énergétique libre à pleine physics (une simulation informatique précise qui prédit à quel point un médicament colle à sa cible, mais cela peut prendre jusqu'à une journée pour effectuer un test même sur un GPU) – à plus de 1 000 fois la vitesse. C'est le premier modèle d'apprentissage en profondeur à fournir ce niveau de précision.
« Cette augmentation des performances fait de Boltz-2 non seulement un outil de recherche, mais un moteur pratique pour le développement de médicaments réels », explique MIT CSAIL Ph.D. Étudiant Gabriele Corso. Corso, aux côtés de son collègue Jeremy Wohlwend et du chercheur de la clinique du MIT Jameel, Saro Passaro, était un chercheur principal de Boltz-1 et de Boltz-2.
« Au lieu de passer des heures à simuler l'interaction entre une seule molécule et sa cible, les scientifiques peuvent désormais dépister de vastes bibliothèques chimiques dans le même laps de temps, permettant aux équipes en démarrage de prioriser uniquement les composés les plus prometteurs pour les tests en laboratoire. »
Boltz-2 sera publié entièrement open source sous la licence MIT, y compris le code du modèle, les poids et les données de formation.
Débuts de Boltz-1
Au début de 2023, une équipe de chercheurs du MIT Computer Science and Artificial Intelligence Laboratory (CSAIL) et de la MIT Jameel Clinic for Machine Learning in Health (Jameel Clinic) a lancé une expérience ambitieuse: un modèle d'apprentissage automatique pourrait-il non seulement prédire les structures moléculaires, mais comprendre comment se comportera biomolécules – comment ils interagiront, et, plus critiques, comme ils sont les biomolécules – la conduite des médicaments dans le médicament dans les médicaments dans les médicaments dans les médicaments.
Au cœur de nombreuses maladies se trouvent des erreurs de fonction des fonctions biomoléculaires. Cela peut cependant être atténué en concevant des molécules qui peuvent se lier aux cibles impliquées. Prédire avec précision ce comportement de liaison est l'un des plus grands défis dans la conception de nouveaux médicaments efficaces.
En 2024, ce projet est devenu connu sous le nom de Boltz-1, un modèle open source conçu comme une alternative rapide et accessible à Alphafold3, la méthode de pointe sur le terrain. Depuis sa sortie, Boltz-1 a été utilisé par des milliers de scientifiques dans les principaux laboratoires universitaires, biotechnologies et sociétés pharmaceutiques, ce qui en fait le modèle le plus utilisé de son genre dans l'industrie.
Maintenant, la même équipe, en collaboration avec la société de biotechnologie Recursion, a dévoilé la prochaine étape: Boltz-2, une avance majeure dans la modélisation moléculaire alimentée par l'IA.
Boltz-2 s'améliore sur Boltz-1 de plusieurs manières clés. Le modèle a été recyclé à l'aide d'un ensemble de données beaucoup plus grand et plus diversifié, y compris des simulations informatiques de molécules en mouvement et des données synthétiques faites à partir de prédictions de la version antérieure du modèle. Il ajoute également une nouvelle fonctionnalité appelée Boltz-Stering, qui aide à affiner les résultats en utilisant des indices basés sur la physique pour rendre les structures prévues plus réalistes.
En plus de ses performances, Boltz-2 a été conçu pour la convivialité. Le modèle peut être guidé par de véritables données expérimentales, des exemples de structures ou des préférences des utilisateurs, donnant aux chercheurs plus de contrôle pour adapter les résultats à ce qu'ils savent déjà ou à ce qu'ils essaient de tester.
« Cette libération est particulièrement importante pour le domaine de la découverte de médicaments à petites molécules, où les progrès ont pris du retard sur les gains rapides observés dans les biologiques et l'ingénierie des protéines », explique Passaro. « Alors que des modèles comme Alphafold et Boltz-1 ont permis un saut significatif dans la conception de calcul des anticorps et des thérapies à base de protéines, nous n'avons pas connu une amélioration similaire de notre capacité à filtrer les petites molécules, qui constituent la majorité des médicaments dans le pipeline mondial.
« Boltz-2 rédige directement cet écart en fournissant des prévisions d'affinité de liaison précises qui peuvent réduire considérablement le coût et le temps du dépistage à un stade précoce. »
Passaro et Corso ont travaillé sur Boltz-2 aux côtés des professeurs du MIT et des chercheurs principaux de CSAIL Regina Barzilay et Tommi Jaakkola, Wohlwend, et une équipe de chercheurs du MIT et de la récursivité.