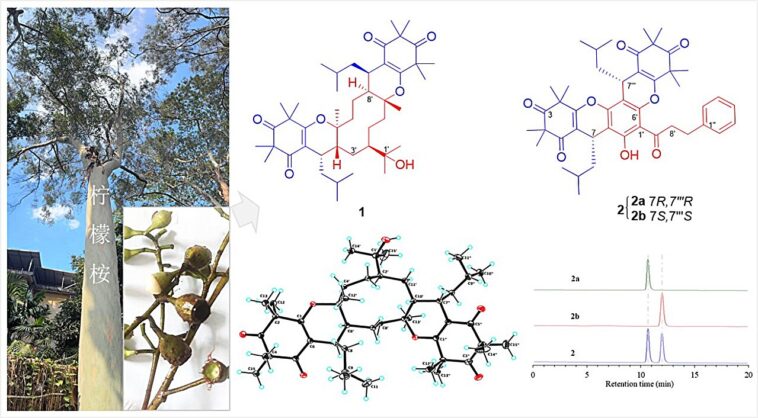
Les chercheurs ont isolé deux nouveaux hybrides Bis-β-triketone, les corymbinols A (1) et B (2a / 2b), des fruits de Corymbia citriodora. Le corymbinol A a démontré une inhibition de 31% de la cuproptose dans les cellules HepG2 à une concentration de 20 μM, suggérant son potentiel en tant qu'option thérapeutique non toxique contre le cancer du foie.
L'étude est publiée dans la revue Lettres biologiques.
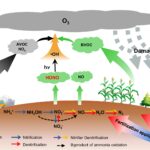
La cuproptose est un mécanisme récemment identifié de mort cellulaire qui dépend du cuivre et est étroitement associé à des maladies neurodégénératives telles qu'Alzheimer et à Huntington. Alors que les chélateurs de cuivre peuvent aider à atténuer la cuproptose, le développement d'inhibiteurs spécifiques s'est révélé difficile.
Pour aborder ce numéro, une équipe de recherche collaborative du jardin botanique national du sud de la Chine et du Kunming Institute of Botany, tous deux à l'Académie chinoise des sciences (CAS), isolé et caractérisé ces deux hybrides Bis-β-triketone – Corymbinols A et B – des fruits de Corymbia Citrodora.
Les chercheurs ont utilisé la RMN, le dichroïsme circulaire électronique (ECD) et les techniques de cristallographie aux rayons X pour élucider les structures complexes de ces composés.
CoryMbinol A présente un nouveau échafaudage pentacyclique 6/6/6/6/6 formé par une cycloaddition hétéro-diélers – Alder (HDA) entre les unités d'hédycaryol (un sesquiterpène) et des unités en double β-Triketone. En revanche, le corymbinol B se compose de conjugués énantiomériques bis-β-trikétone-dihydrochalcone.

Dans un modèle de cellule Hepg2 induit par elesclomol (ES) et CUCL2Corymbinol A a montré une inhibition modérée de la cuproptose à 20 μm, ce qui a partiellement inversé la mort cellulaire causée par l'accumulation de cuivre. Il a également restauré les niveaux d'expression des protéines de grappes mitochondriales de fer-soufre (ACO2 et SDHB), qui sont des marqueurs clés de la cuproptose.
Des études mécanistes indiquent que le corymbinol A perturbe la toxicité des protéines médiées par le cuivre sans agir comme chélateur de cuivre, offrant une stratégie thérapeutique unique.
L'étude a en outre proposé une voie de biosynthèse pour ces composés, provenant de monomères de β-trikétone trouvés dans les plantes Myrtaceae. Cette recherche améliore la diversité chimique des dérivés de phloroglucinol et souligne leur potentiel dans le ciblage des maladies basées sur le cuivre.