L'ammoniac est un produit chimique essentiel à de nombreux processus agricoles et industriels, mais son mode de production s'accompagne d'un coût énergétique incroyablement élevé. Diverses tentatives ont et sont faites pour produire de l'ammoniac plus efficacement.
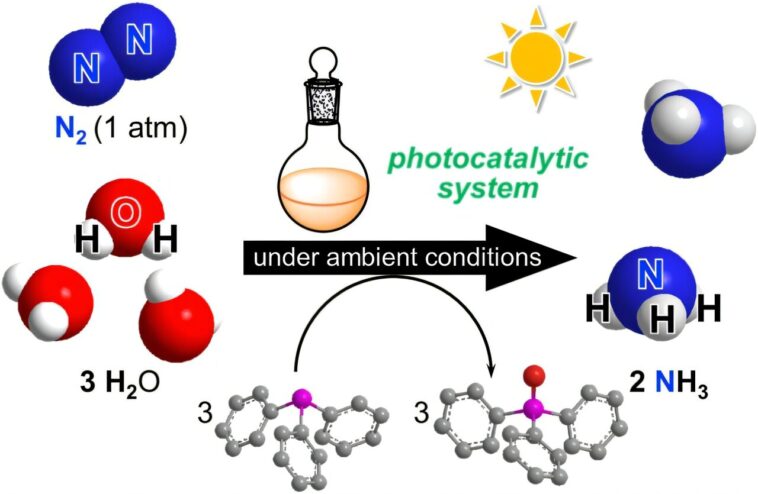
Pour la première fois, un groupe comprenant des chercheurs de l'Université de Tokyo a combiné l'azote atmosphérique, l'eau et la lumière du soleil et, en utilisant deux catalyseurs, a produit des quantités importantes d'ammoniac sans coût d'énergie élevé. Leurs processus reflètent les processus naturels trouvés dans les plantes utilisant des bactéries symbiotiques.
L'œuvre a été publiée dans Communications de la nature.
Un peu moins de 200 millions de tonnes d'ammoniac sont produites chaque année, et 80% de celles-ci sont utilisées pour les engrais. De plus, sa production représente environ 2% de la consommation d'énergie entière du monde et, en conséquence, environ 2% de l'ensemble des émissions de dioxyde de carbone du monde. Avec ces choses à l'esprit, il est compréhensible que les chercheurs du monde entier essaient de créer un moyen plus propre et plus efficace de produire de l'ammoniac.
Le professeur Yoshiaki Nishibayashi du Département de chimie appliquée de l'Université de Tokyo et de son équipe ont fait des progrès importants dans cet objectif.
Ils ont réussi à développer un nouveau système catalytique pour produire de l'ammoniac à partir de molécules abondantes trouvées sur Terre, y compris l'azote atmosphérique et l'eau. La clé réside dans une combinaison de deux types de catalyseurs, des composés intermédiaires qui permettent ou accélèrent les réactions sans contribuer au mélange final, fabriqués spécialement pour la production d'ammoniac et qui sont entraînés par la lumière du soleil.
« Il s'agit du premier exemple réussi de production d'ammoniac photocatalytique utilisant un dinitrogen atmosphérique comme source d'azote et eau comme source de protons, qui utilise également une énergie lumineuse visible et deux types de catalyseurs moléculaires », a déclaré Nishibayashi.
« Nous avons utilisé un photocatalyste d'iridium et un autre produit chimique appelé phosphine tertiaire qui a permis une activation photochimique des molécules d'eau. Les efficacités de réaction étaient plus élevées que prévu, par rapport aux rapports précédents de formation d'ammoniac photocatalytique à lumière visible à la lumière. »
La chose à propos des réactions chimiques est qu'ils ne se produisent pas toujours aussi vite que vous le souhaitez, ou dans la façon dont vous le souhaitez. Et pour contrôler le résultat, l'efficacité, le timing, etc. d'un processus, vous devez impliquer des composants supplémentaires au-delà des ingrédients bruts. C'est là que les catalyseurs entrent en jeu.
Nishibayashi et son équipe ont utilisé deux catalyseurs pour ces expériences, l'une basée sur le molybdène du métal de transition pour l'activation du dinitrogen et l'autre basé sur le métal de transition iridium pour la photoactivation des phosphines tertiaires et de l'eau. Un troisième composant appelé phosphines tertiaires est également essentiel pour aider à sortir les protons des molécules d'eau.
« Lorsque le photocatalyseur d'iridium absorbe la lumière du soleil, son état excité peut oxyder les phosphines tertiaires. Les phosphines tertiaires oxydées activent ensuite les molécules d'eau via la formation d'une liaison chimique entre l'atome de phosphore de la phosphine et l'eau, produisant des protons », a déclaré Nishibayashi.
« Le catalyseur du molybdène permet alors à l'azote de se lier avec ces protons pour devenir l'ammoniac. L'utilisation de l'eau pour produire des atomes de dihydrogène ou d'hydrogène est l'un des processus les plus importants pour atteindre la production d'ammoniac vert. »
L'équipe a réussi à produire cette réaction à une échelle 10 fois celle des expériences précédentes, suggérant qu'elle est prête pour les essais à plus grande échelle, bien qu'il y ait encore des problèmes qui pourraient améliorer davantage la sécurité et l'efficacité.
Certains des composants tels que les phosphines tertiaires pourraient être fabriqués à l'aide de l'énergie solaire ou recyclés à partir d'oxydes de phosphine. Et bien que stables eux-mêmes, ils peuvent être toxiques s'ils sont ingérés par les gens, il serait donc idéal de trouver un moyen responsable de les éliminer ou de les recycler.
« Dans les plantes, l'ammoniac est formé par fixation biologique à l'azote à l'aide de cyanobactéries et est lié à la photosynthèse », a déclaré Nishibayashi.
« Ici, les électrons de la réaction sont fournis par la photosynthèse et les protons sont dérivés de l'eau. Par conséquent, les résultats de notre étude récente peuvent être considérés comme un exemple réussi de la photosynthèse artificielle de l'ammoniac. »