Une percée réalisée par des scientifiques du MIT et de Harvard permet une conversion efficace du dioxyde de carbone en formiate stable et sûr, remplaçant potentiellement les combustibles fossiles et adapté au stockage à long terme et à la production d’électricité.
Cette approche convertit directement les gaz à effet de serre en formiate, un combustible solide qui peut être stocké indéfiniment et pourrait être utilisé pour chauffer des maisons ou alimenter des industries.
Des recherches sont en cours dans le monde entier pour trouver des moyens d’extraire le dioxyde de carbone de l’air ou des gaz d’échappement des centrales électriques, puis d’en faire quelque chose d’utile. L’une des idées les plus prometteuses consiste à en faire un combustible stable, capable de remplacer les combustibles fossiles dans certaines applications. Mais la plupart de ces processus de conversion ont rencontré des problèmes de faible efficacité carbone ou produisent des carburants difficiles à manipuler, toxiques ou inflammables.
Percée dans la conversion du CO2 en carburant
Maintenant, les chercheurs de MIT et l’Université Harvard ont développé un procédé efficace permettant de convertir le dioxyde de carbone en formiate, un matériau liquide ou solide pouvant être utilisé comme l’hydrogène ou le méthanol pour alimenter une pile à combustible et produire de l’électricité. Le formiate de potassium ou de sodium, déjà produit à l’échelle industrielle et couramment utilisé comme dégivrant pour les routes et les trottoirs, est non toxique, ininflammable, facile à stocker et à transporter, et peut rester stable dans des réservoirs en acier ordinaires pour être utilisé des mois, voire des années. , après sa production.

Le rendu montre 3 parties comme sur une table grise : une maison modèle blanche sur le dessus ; une pile à combustible prise en sandwich entre deux plaques métalliques avec des molécules sphériques flottant autour d’elle ; et en bas se trouve l’électrolyseur, qui ressemble à la pile à combustible et est entouré de molécules flottantes. Crédit : Shuhan Miao, École supérieure de design de Harvard
Le nouveau processus, développé par les doctorants du MIT, Zhen Zhang, Zhichu Ren et Alexander H. Quinn ; Dawei Xi, doctorant à l’Université Harvard ; et le professeur Ju Li du MIT, est décrit récemment dans un article en libre accès dans Rapports de cellules Science physique. L’ensemble du processus – y compris la capture et la conversion électrochimique du gaz en poudre de formiate solide, qui est ensuite utilisée dans une pile à combustible pour produire de l’électricité – a été démontré à petite échelle en laboratoire. Cependant, les chercheurs s’attendent à ce qu’il soit évolutif afin de pouvoir fournir de la chaleur et de l’électricité sans émissions aux maisons individuelles et même être utilisé dans des applications industrielles ou à l’échelle du réseau.
Efficacité et praticité améliorées
D’autres approches pour convertir le dioxyde de carbone en carburant, explique Li, impliquent généralement un processus en deux étapes : d’abord, le gaz est chimiquement capturé et transformé en une forme solide sous forme de carbonate de calcium, puis plus tard, ce matériau est chauffé pour éliminer le dioxyde de carbone et le convertir. à une matière première combustible telle que le monoxyde de carbone. Cette deuxième étape a une très faible efficacité, convertissant généralement moins de 20 % du dioxyde de carbone gazeux en produit souhaité, explique Li.
En revanche, le nouveau procédé atteint une conversion bien supérieure à 90 pour cent et élimine le besoin d’une étape de chauffage inefficace en convertissant d’abord le dioxyde de carbone en une forme intermédiaire, le bicarbonate de métal liquide. Ce liquide est ensuite converti électrochimiquement en formiate de potassium ou de sodium liquide dans un électrolyseur qui utilise de l’électricité à faible teneur en carbone, par exemple l’énergie nucléaire, éolienne ou solaire. La solution liquide de potassium ou de formiate de sodium hautement concentrée produite peut ensuite être séchée, par exemple par évaporation solaire, pour produire une poudre solide très stable et pouvant être stockée dans des réservoirs en acier ordinaires pendant des années, voire des décennies, explique Li.
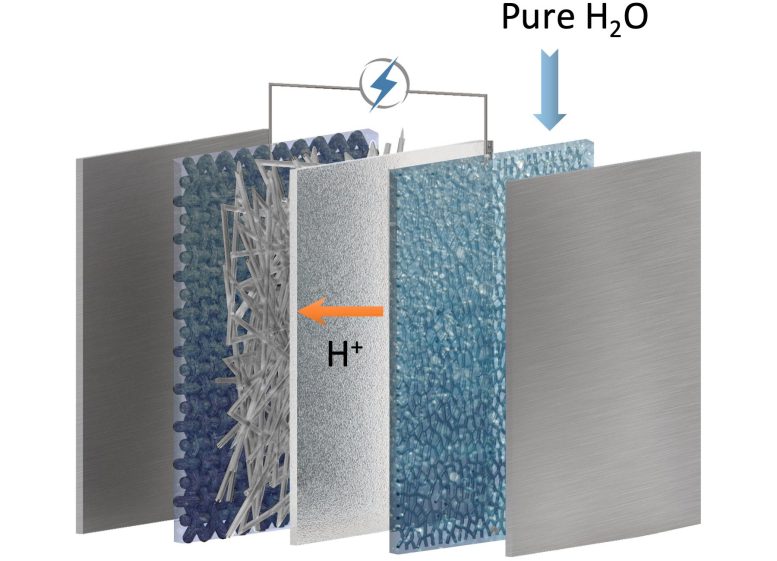
Une configuration électrolytique avec une cathode de bicarbonate, une couche tampon intermédiaire, une membrane échangeuse de cations et une anode à eau. Crédit : Shuhan Miao, École supérieure de design de Harvard
Plusieurs étapes d’optimisation développées par l’équipe ont fait toute la différence pour transformer un processus de conversion chimique inefficace en une solution pratique, explique Li, qui occupe des postes conjoints dans les départements de science et d’ingénierie nucléaires et de science et d’ingénierie des matériaux.
Processus de conversion et applications
Le processus de captage et de conversion du carbone implique d’abord un captage à base de solution alcaline qui concentre le dioxyde de carbone, soit à partir de flux concentrés tels que les émissions des centrales électriques, soit à partir de sources à très faible concentration, même à l’air libre, sous la forme d’un métal liquide. solution de bicarbonate. Ensuite, grâce à l’utilisation d’un électrolyseur à membrane échangeuse de cations, ce bicarbonate est converti électrochimiquement en cristaux de formiate solide avec une efficacité en carbone supérieure à 96 %, comme l’ont confirmé les expériences en laboratoire de l’équipe.
Ces cristaux ont une durée de conservation indéfinie et restent si stables qu’ils pourraient être stockés pendant des années, voire des décennies, avec peu ou pas de perte. En comparaison, même les meilleurs réservoirs de stockage d’hydrogène disponibles permettent au gaz de s’échapper à un taux d’environ 1 % par jour, ce qui exclut toute utilisation qui nécessiterait un stockage d’un an, explique Li. Le méthanol, une autre alternative largement explorée pour convertir le dioxyde de carbone en carburant utilisable dans les piles à combustible, est une substance toxique qui ne peut pas être facilement adaptée pour être utilisée dans des situations où une fuite pourrait présenter un risque pour la santé. Le formiate, en revanche, est largement utilisé et considéré comme inoffensif, selon les normes de sécurité nationales.
Améliorations techniques
Plusieurs améliorations expliquent l’efficacité grandement améliorée de ce processus. Premièrement, une conception minutieuse des matériaux de la membrane et de leur configuration surmonte un problème rencontré par les tentatives précédentes d’un tel système, où une accumulation de certains sous-produits chimiques modifie le pH, entraînant une perte constante d’efficacité du système au fil du temps. «Traditionnellement, il est difficile de parvenir à une conversion stable et continue des matières premières à long terme», explique Zhang. « La clé de notre système est d’atteindre un équilibre de pH pour une conversion à l’état stable. »
Pour y parvenir, les chercheurs ont effectué une modélisation thermodynamique pour concevoir le nouveau procédé de manière à ce qu’il soit chimiquement équilibré et que le pH reste à un état stable sans changement d’acidité au fil du temps. Il peut donc continuer à fonctionner efficacement sur de longues périodes. Lors de leurs tests, le système a fonctionné pendant plus de 200 heures sans diminution significative du rendement. L’ensemble du processus peut être réalisé à des températures ambiantes et à des pressions relativement basses (environ cinq fois la pression atmosphérique).
Un autre problème était que des réactions secondaires indésirables produisaient d’autres produits chimiques inutiles, mais l’équipe a trouvé un moyen de prévenir ces réactions secondaires en introduisant une couche « tampon » supplémentaire de laine de verre enrichie en bicarbonate qui bloquait ces réactions.
L’équipe a également construit une pile à combustible spécialement optimisée pour l’utilisation de ce combustible formiate pour produire de l’électricité. Les particules de formiate stockées sont simplement dissoutes dans l’eau et pompées dans la pile à combustible selon les besoins. Bien que le combustible solide soit beaucoup plus lourd que l’hydrogène pur, lorsque l’on prend en compte le poids et le volume des réservoirs de gaz à haute pression nécessaires pour stocker l’hydrogène, le résultat final est une production d’électricité proche de la parité pour un volume de stockage donné, explique Li.
Applications potentielles
Le combustible formiate peut potentiellement être adapté à tout, depuis les unités de taille domestique jusqu’aux utilisations industrielles à grande échelle ou aux systèmes de stockage à l’échelle du réseau, affirment les chercheurs. Les premières applications domestiques pourraient impliquer un électrolyseur de la taille d’un réfrigérateur pour capturer et convertir le dioxyde de carbone en formiate, qui pourrait être stocké dans un réservoir souterrain ou sur le toit. Ensuite, si nécessaire, le solide en poudre serait mélangé à de l’eau et introduit dans une pile à combustible pour fournir de l’électricité et de la chaleur. « C’est pour des manifestations communautaires ou domestiques », dit Zhang, « mais nous pensons qu’à l’avenir également, cela pourrait être bénéfique pour les usines ou le réseau. »
« L’économie du formiate est un concept intrigant car les sels de formiate métalliques sont très inoffensifs et stables, et constituent un vecteur d’énergie incontournable », explique Ted Sargent, professeur de chimie et de génie électrique et informatique à l’Université de New York. Université du nord-ouest, qui n’était pas associé à ce travail. « Les auteurs ont démontré une efficacité accrue dans la conversion liquide-liquide de la matière première bicarbonate en formiate, et ont démontré que ces carburants peuvent être utilisés plus tard pour produire de l’électricité », dit-il.
Les travaux ont été soutenus par l’Office of Science du Département américain de l’énergie.