Représentation de complexes d’europium changeant de structure lors de leur interaction avec une cellule tumorale. Crédit : Mengfei Wang, et al. Rapports scientifiques. 22 janvier 2024
Un complexe d’europium soluble dans l’eau et luminescent permet d’évaluer le degré de malignité des cellules tumorales de gliome modèle.
Un élément important du choix du traitement anticancéreux le plus approprié consiste à comprendre la malignité de la tumeur ; cependant, les méthodes actuelles d’évaluation de la malignité des tumeurs cérébrales sont invasives et présentent un risque élevé de complications.
Recherche collaborative dirigée par le professeur Yasuchika Hasegawa et le professeur Shinya Tanaka de l’Institute for Chemical Reaction Design and Discovery (WPI-ICReDD) à Université d’Hokkaido a développé un système de sondage non destructif pour le cancer (GPS) pour évaluer le degré de malignité de cellules tumorales de gliome modèles à l’aide d’un complexe d’europium soluble dans l’eau et luminescent. Cette méthode pourrait conduire à des tests non invasifs pour la détermination de la malignité d’une tumeur chez les patients.
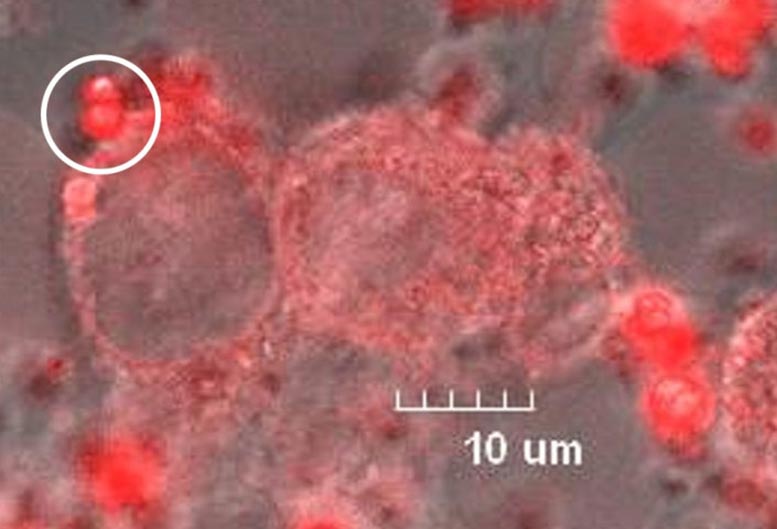
Image au microscope confocal montrant l’émission de lumière rouge des complexes d’europium à l’intérieur de cellules modèles de gliome. Le cercle blanc désigne une agrégation du complexe europium. Crédit : Mengfei Wang, et al. Rapports scientifiques. 22 janvier 2024
Tests de malignité non invasifs
L’équipe a évalué la malignité d’une tumeur en introduisant le complexe europium pour modéliser des cellules qui imitent le gliome, un type courant de tumeur qui représente 26,3% des cancers du cerveau (Source : CBTRUS). Trois cellules modèles différentes imitant différents degrés de malignité ont été testées et les chercheurs ont mesuré les changements dans la durée de vie de l’émission de lumière rouge caractéristique du complexe europium. Les chercheurs ont découvert qu’au cours des trois premières heures suivant l’ajout du complexe d’europium, des changements plus importants dans la durée de vie de l’émission lumineuse se produisaient dans les cellules les plus malignes.
« La visualisation de cellules cancéreuses à l’aide de complexes luminescents a déjà été rapportée, mais notre hypothèse était que les signaux photophysiques envoyés par de tels complexes dans les cellules cancéreuses pourraient refléter les informations internes des cellules cancéreuses », a déclaré Hasegawa.

Membres de l’équipe de recherche de l’Institute for Chemical Reaction Design and Discovery (WPI-ICReDD), Université d’Hokkaido. De gauche à droite : Mengfei Wang, Masumi Tsuda, Shinya Tanaka, Yasuchika Hasegawa. Crédit : WPI-ICReDD
Percée dans l’analyse des tumeurs
Pour parvenir à ce résultat, les chercheurs ont d’abord modifié le complexe de l’europium afin qu’il soit soluble dans l’eau et stable parmi les acides aminés dans le milieu de culture cellulaire. Lors de son addition au milieu de culture cellulaire, le complexe d’europium forme initialement un agrégat avec lui-même. L’interaction avec des cellules tumorales modèles entraîne la rupture des agrégats en molécules uniques, qui sont ensuite rapidement absorbées par les cellules. Ce processus favorise des changements structurels dans le complexe europium, qui entraînent des modifications dans la durée de vie de l’émission de lumière rouge du complexe.
Ces différences dans les durées de vie des émissions ont été attribuées aux variations de l’activité tumorale et aux processus de croissance des différents grades de malignité, qui pourraient provoquer différents changements structurels à différentes échelles de temps dans le complexe de l’europium. L’équipe prévoit que l’utilisation de cette méthode pourrait permettre une détection continue de l’activité tumorale et fournir aux médecins des informations clés pour décider du traitement approprié.
« Les tumeurs cérébrales surviennent chez 4,6 personnes sur 100 000 au Japon, et le taux de survie à 5 ans est de 16 % pour le type de glioblastome de grade 4 le plus malin, qui est un type agressif de tumeur cérébrale de gliome », a expliqué Tanaka. « La méthode d’évaluation de la malignité que nous avons développée pourrait bénéficier à ces patients à l’avenir. »