Les chercheurs ont étudié une molécule C60, également appelée buckyball, pour comprendre comment elle pouvait briser l’ergodicité. Crédit : Steven Burrows/Jun Ye et David Nesbitt
Les scientifiques ont observé des comportements uniques de rupture d’ergodicité dans les rotations de la molécule C60 sans rompre la symétrie grâce à la spectroscopie infrarouge avancée. Cette découverte offre de nouvelles perspectives sur la dynamique des systèmes quantiques et promet de nouvelles investigations moléculaires.
Des chercheurs dirigés par Jun Ye, membre du JILA et du NIST, ainsi que David Nesbitt, chercheur du JILA et du NIST, et des scientifiques de l’Université du Nevada, de Reno et de l’Université Harvard, ont observé une nouvelle rupture d’ergodicité dans C60, une molécule hautement symétrique composée de 60 atomes de carbone. disposés sur les sommets d’un motif « ballon de football » (avec 20 faces hexagonales et 12 faces pentagonales). Leurs résultats ont révélé une rupture d’ergodicité dans les rotations du C60. Remarquablement, ils ont découvert que cette rupture d’ergodicité se produit sans rupture de symétrie et peut même s’activer et se désactiver à mesure que la molécule tourne de plus en plus vite. Comprendre la rupture d’ergodicité peut aider les scientifiques à concevoir des matériaux mieux optimisés pour le transfert d’énergie et de chaleur. L’étude a été publiée le 17 août dans la revue Science.
De nombreux systèmes courants du quotidien – tels que la chaleur se propageant dans une poêle à frire et la fumée remplissant une pièce – présentent une « ergodicité ». En d’autres termes, la matière ou l’énergie se propage uniformément dans le temps à toutes les parties du système, dans la mesure où les économies d’énergie le permettent. D’un autre côté, comprendre comment les systèmes peuvent violer (ou « briser ») l’ergodicité, comme les aimants ou les supraconducteurs, aide les scientifiques à comprendre et à concevoir d’autres états exotiques de la matière.
Dans de nombreux cas, la rupture d’ergodicité est liée à ce que les physiciens appellent la « rupture de symétrie ». Par exemple, les moments magnétiques internes des atomes dans un aimant pointent tous dans une direction, soit « vers le haut », soit « vers le bas ». Bien qu’elles possèdent la même énergie, ces deux configurations distinctes sont séparées par une barrière énergétique. La « rupture de symétrie » fait référence au système supposant une configuration avec une symétrie inférieure à celle que les lois physiques régissant son comportement le permettraient, comme tous les moments magnétiques pointant « vers le bas » comme état par défaut. Dans le même temps, puisque l’aimant s’est installé de manière permanente dans l’une des deux configurations à énergie égale, il a également rompu l’ergodicité.
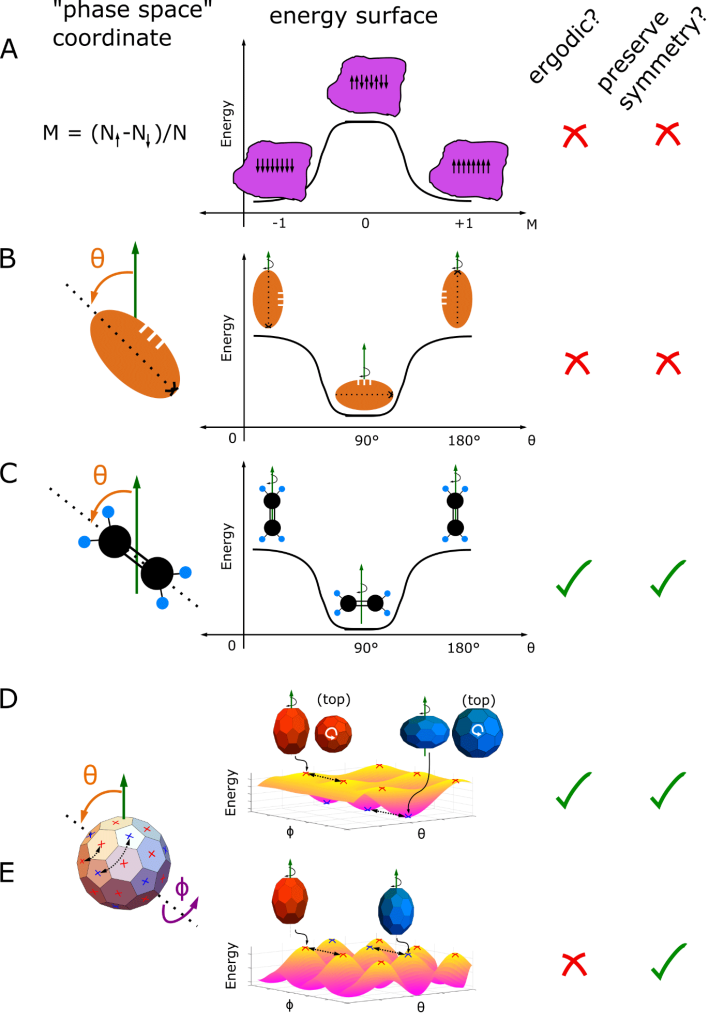
Figure 1. A) Un aimant brise l’ergodicité en brisant également la symétrie. Les deux configurations ferromagnétiques à énergie égale mais distinctes (magnétisation totale M = +1 ou -1) sont stabilisées par une barrière énergétique. B) Un ballon de football en rotation brise l’ergodicité en brisant également la symétrie. L’axe θ représente l’orientation angulaire (polaire) du ballon par rapport au vecteur moment cinétique (flèche verte), qui est fixe. Un « X » distingue une extrémité du ballon de football, même s’il y a une infime différence, même un seul atome. Crédit : JILA
Briser la symétrie : aimants et ballons de football
Pour comprendre la rupture de l’ergodicité rotationnelle, Lee Liu, chercheur postdoctoral et auteur principal, a expliqué : « Considérons un ballon de football lancé dans une spirale serrée dans le sens des aiguilles d’une montre. Vous ne verriez jamais le ballon se retourner spontanément à 180 degrés en plein vol, passant d’une configuration à 90 degrés à faible consommation d’énergie à une configuration à 180 degrés ! Ceci est illustré sur les figures 1B et 1C. Cela nécessiterait de surmonter une barrière énergétique. Ainsi, un ballon de football en spirale maintient son orientation de bout en bout en vol libre, brisant l’ergodicité et la symétrie comme le fait un aimant.
Cependant, contrairement aux ballons de football, les molécules isolées doivent obéir aux règles de la mécanique quantique. Plus précisément, les deux extrémités d’une molécule d’éthylène (un analogue quantique d’un ballon de football) sont indiscernables (figure 1C). Ainsi, réorienter une molécule d’éthylène en rotation de 180 degrés d’un bout à l’autre implique également de surmonter une barrière énergétique ; les états initial et final sont indiscernables. La molécule n’a pas le choix entre deux orientations distinctes de bout en bout, et la symétrie et l’ergodicité sont restaurées, ce qui signifie que l’état fondamental de la molécule est une combinaison, ou la superposition, des états final et initial.
Buckyballs C60
Le C60, communément appelé Buckminsterfullerène ou simplement «buckyball», est une molécule composée de 60 atomes de carbone disposés dans une sphère creuse, ressemblant à une structure de ballon de football. Cette configuration se compose de 20 anneaux hexagonaux et 12 anneaux pentagonaux reliés entre eux pour former une forme sphérique sans soudure. Nommé d’après l’architecte Buckminster Fuller en raison de sa ressemblance avec ses dômes géodésiques, le C60 fait partie de la famille des structures en carbone fullerène, qui comprend également des nanotubes de carbone cylindriques. La découverte du C60 dans les années 1980 a ouvert de nouvelles voies dans le domaine des nanotechnologies et a valu aux chercheurs le prix Nobel de chimie en 1996.
Spectroscopie infrarouge du C60
Pour sonder la dynamique de rotation de la molécule C60, les chercheurs se sont tournés vers une technique mise au point par le groupe Ye en 2016 : combinant le refroidissement par gaz tampon avec la spectroscopie infrarouge sensible améliorée par cavité. Grâce à cette technique, les chercheurs ont mesuré le spectre infrarouge du C60 avec une sensibilité 1 000 fois supérieure à celle obtenue auparavant. Il s’agissait d’éclairer une lumière laser sur des molécules C60 et d’« écouter » les fréquences de lumière qu’elles absorbent.
« Tout comme le son d’un instrument peut vous renseigner sur ses propriétés physiques, les fréquences de résonance moléculaire, codées dans son spectre infrarouge, peuvent nous renseigner sur la structure et la dynamique de rotation de la molécule », a déclaré Liu. Plutôt que de faire tourner physiquement la molécule de plus en plus vite, les chercheurs ont sondé un échantillon en phase gazeuse de nombreuses molécules C60 dans lequel certaines tournaient rapidement et d’autres lentement. Le spectre infrarouge résultant contenait des instantanés de la molécule à différentes vitesses de rotation.
« L’assemblage de ces traces a généré le spectre complet, révélant l’image complète de l’évolution (ou de la rupture) de l’ergodicité de la molécule », a élaboré Dina Rosenberg, chercheuse postdoctorale dans le groupe de Ye.
Grâce à ce processus, les chercheurs ont découvert un comportement étonnant du C60 : le faire tourner à 2,3 GHz (milliards de rotations par seconde) le rend ergodique. Cette phase ergodique persiste jusqu’à 3,2 GHz lorsque la molécule rompt l’ergodicité. À mesure que la molécule tourne plus vite, elle redevient ergodique à 4,5 GHz. Ce comportement de commutation particulier a surpris les chercheurs, car les transitions d’ergodicité ne se produisent généralement qu’une fois que l’énergie augmente et dans une seule direction. Curieuse, l’équipe a approfondi le spectre pour comprendre l’origine de ce comportement.
Briser l’ergodicité : football quantique, frisbee et football
En analysant le spectre infrarouge, les chercheurs pourraient déduire des déformations de la molécule induites par sa rotation. Comme Liu l’a expliqué : « Tout comme les pneus des voitures de course d’accélération se gonflent davantage lorsqu’ils tournent à un rythme plus rapide, le taux de rotation du C60 dicte sa déformation structurelle. Les spectres infrarouges impliquent que deux possibilités se produisent lorsque la vitesse de rotation du C60 atteint 2,3 GHz : il peut s’aplatir en forme de frisbee ou s’allonger en forme de ballon de football. Le premier se produit s’il tourne autour d’un pentagone, et le second s’il tourne autour d’un hexagone (figure 1D). Lorsque C60 atteint 3,2 GHz, les rotations hexagonales et pentagonales entraînent une déformation semblable à celle d’un ballon de football (figure 1E). À 4,5 GHz, la rotation hexagonale génère une déformation semblable à celle d’un frisbee, tandis que la rotation pentagonale génère une déformation semblable à celle d’un ballon de football. Il s’avère que les transitions d’ergodicité particulières de C60 pourraient être entièrement attribuées à cette séquence de déformations induites par la rotation de la molécule.
Briser l’ergodicité mais pas la symétrie
En phase gazeuse, les molécules C60 entrent si rarement en collision qu’elles se comportent comme si elles étaient isolées, ce qui signifie que l’impossibilité de distinguer chaque carbone atome en C60 devient important. Par conséquent, faire tourner la molécule autour de n’importe quel pentagone équivaut à la faire tourner autour de n’importe quel autre pentagone (voir les X rouges sur la figure 1D). De même, faire tourner la molécule autour de n’importe quel hexagone équivaut à la faire tourner autour de n’importe quel autre hexagone (voir les X bleus sur la figure 1D). Tout comme dans l’éthylène, l’indiscernabilité quantique des atomes de carbone du C60 rétablit la symétrie des secteurs de rotation pentagonaux et hexagonaux. Néanmoins, les données des chercheurs ont montré que l’axe de rotation de la molécule ne changeait jamais de secteur.
Les données ont montré deux raisons pour cet isolement rotationnel autour d’un seul axe. À des taux de rotation inférieurs à 3,2 et supérieurs à 4,5 GHz, les secteurs de rotation pentagonaux et hexagonaux sont isolés en raison des économies d’énergie. « Il faut plus d’énergie pour faire tourner un ballon de football qu’un frisbee (en raison de sa masse) », a déclaré Liu. Dans cette gamme, les molécules C60 sont ergodiques car les secteurs pentagonaux et hexagonaux explorent tous les états possibles dans des gammes d’énergie distinctes, tout comme dans le cas de l’éthylène. Cela correspond au fait que des croix rouges et bleues sur la surface énergétique de la figure 1D existent à différentes valeurs d’énergie.
Aux taux de rotation compris entre 3,2 et 4,5 GHz, des secteurs pentagonaux et hexagonaux existent dans la même plage d’énergie. « C’est parce que faire tourner un ballon de football hexagonal et un ballon de football pentagonal peut nécessiter la même quantité d’énergie », a expliqué Liu. « Néanmoins, le C60 ne parvient toujours pas à basculer entre les deux secteurs de rotation à cause d’une barrière énergétique – la même barrière qui empêche un ballon de se retourner d’un bout à l’autre en plein vol. Dans ce régime, le C60 a donc rompu l’ergodicité sans rompre la symétrie. Ce mécanisme de rupture d’ergodicité sans rupture de symétrie, qui peut être compris simplement en termes de déformations d’une molécule en rotation, a été pour nous une surprise totale », a déclaré Liu. Ces résultats révèlent un exemple rare de rupture d’ergodicité sans rupture de symétrie, donnant ainsi un aperçu supplémentaire de la dynamique quantique du système.
Comme le supposent les chercheurs, de nombreux autres espèces attendez une enquête détaillée utilisant la nouvelle technique de l’équipe. « Les molécules recèleront probablement bien d’autres surprises, et nous sommes impatients de les découvrir. »