En fusionnant des fragments d'enzymes avec des anticorps, des chercheurs de l'Institut des sciences de Tokyo, au Japon, ont développé un commutateur enzymatique innovant appelé « Switchbody », qui est activé lorsqu'il est lié à son antigène cible. Switchbody est basé sur un système de piégeage et de libération de fragments enzymatiques qui contrôle dynamiquement l'activité enzymatique, offrant ainsi de nouvelles opportunités en matière de diagnostic, de thérapie et de bioprocédés de précision.
Les protéines qui répondent aux stimuli externes fonctionnent comme des commutateurs moléculaires, jouant un rôle essentiel dans la régulation précise des processus biologiques. Par conséquent, si les commutateurs protéiques pouvaient être artificiellement modifiés pour contrôler librement la fonction physiologique cellulaire, nous obtiendrons non seulement une compréhension plus approfondie du mécanisme des phénomènes biologiques, mais contribuerions également à l’application thérapeutique en restaurant les fonctions cellulaires altérées.
Bien que des commutateurs protéiques artificiels aient été développés, la conception rationnelle de protéines capables d’activer ou de désactiver leur activité reste un défi de longue date en biochimie.
Pour combler cette lacune, une équipe de chercheurs dirigée par le professeur agrégé Tetsuya Kitaguchi et le professeur adjoint Takanobu Yasuda du Laboratoire de chimie et des sciences de la vie, Institut de recherche intégrée, Institut des sciences de Tokyo (Science Tokyo), Japon, en collaboration avec le professeur adjoint Masahiko Taguchi de l'Université de Tohoku, Japon ; Dr Takanori Kigawa de RIKEN, Japon ; et le professeur Ryoichi Arai de l'Université de Shinshu, au Japon, ont développé le nouveau Switchbody, un commutateur enzymatique basé sur des anticorps.
L'étude a été publiée en ligne dans la revue Science avancée le 15 septembre 2025.
Comment Switchbody a été développé et testé
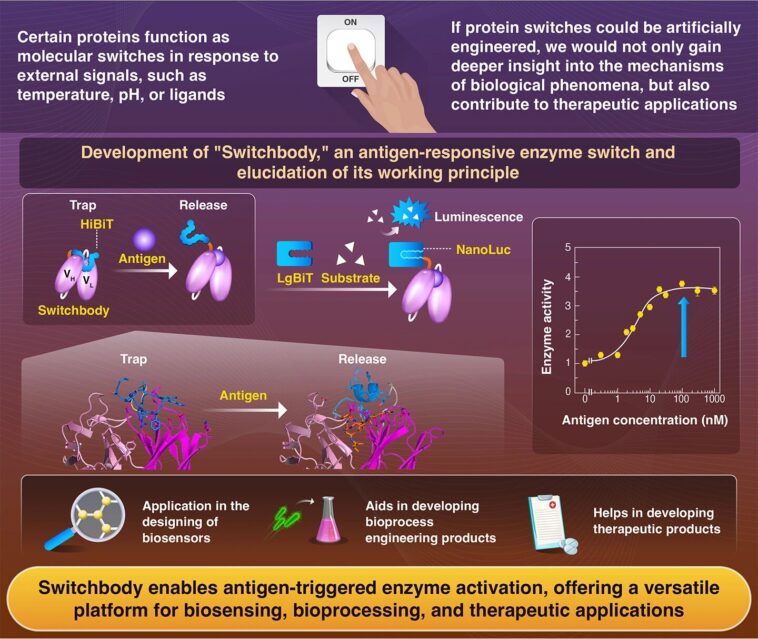
Comme élément de reconnaissance moléculaire, les chercheurs ont utilisé un anticorps qui se lie au peptide de sept acides aminés dérivé de la protéine Bone Gla. En tant que protéine permettant d'introduire la fonction de commutation, ils ont adopté le NanoLuc divisé, qui est une enzyme bioluminescente composée de deux parties ; HiBiT, un court fragment composé de 11 acides aminés, et son grand fragment complémentaire, LgBiT. Bien que chaque fragment soit inactif en soi, ils se reconstituent en un NanoLuc fonctionnel qui produit une bioluminescence lumineuse en catalysant un substrat.
Pour développer le Switchbody, les chercheurs ont fusionné un anticorps avec le HiBiT. Cette fusion a permis l'activité enzymatique lorsque l'anticorps se liait à son antigène cible. Le principe de fonctionnement sous-jacent repose sur un processus de « piégeage et libération ».
« En l'absence d'antigènes, le HiBiT fusionné est piégé dans l'anticorps », explique Kitaguchi. « La liaison à l'antigène déclenche sa libération, permettant à HiBiT de s'associer à son fragment complémentaire, LgBiT, rétablissant ainsi l'activité productrice de bioluminescence de l'enzyme. »
Mécanisme et applications potentielles
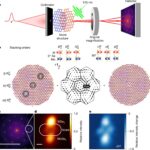
Pour comprendre le mécanisme de ce processus, l'équipe a effectué une enquête approfondie en utilisant une combinaison de techniques analytiques avancées, notamment ELISA, la cristallographie aux rayons X, la spectroscopie RMN et les simulations de dynamique moléculaire.
Ces analyses ont révélé qu'en l'absence d'antigène, le HiBiT interagit avec les acides aminés clés à proximité du site de liaison à l'antigène. Lors de la liaison à l'antigène, ces interactions sont perturbées, augmentant la motilité de HiBiT pour former un complexe enzymatique actif avec LgBiT. Ces connaissances sur son mécanisme ont ouvert la voie à la conception rationnelle de Switchbody.
Essentiellement, l’approche transforme une enzyme en un commutateur moléculaire intelligent activé par l’antigène, offrant ainsi une nouvelle stratégie puissante non seulement pour détecter des molécules biologiques, mais également pour réguler les fonctions physiologiques cellulaires en employant des enzymes impliquées dans des processus clés tels que la transduction du signal et le métabolisme.
Expansion de la technologie et orientations futures
De plus, les chercheurs ont également développé une sonde capable de s’assembler avec des anticorps non modifiés pour former un Switchbody. Cette sonde a été réalisée en fusionnant HiBiT à une protéine de liaison aux anticorps connue sous le nom de « protéine M ». Cette adaptation remarquable ouvre de nouvelles voies pour qu’un large éventail d’anticorps disponibles dans le commerce soient convertis en commutateurs enzymatiques sensibles aux antigènes.
« Nous pensons que cette technologie pourrait être appliquée aux applications de biodétection, de bioprocédés et thérapeutiques », explique Kitaguchi. « À l'avenir, nous aimerions étendre les Switchbodies pour contrôler simultanément plusieurs fonctions cellulaires, permettant ainsi une régulation en temps réel des voies biochimiques. »