En biologie, les enzymes ont évolué sur des millions d'années pour générer des réactions chimiques. Les scientifiques de l'Institut Max Planck pour la dynamique et l'auto-organisation (MPI-DS) ont désormais dérivé des règles universelles pour permettre la conception de novo d'enzymes optimales.
Le document est publié dans la revue Catalyse chimique.
Par exemple, ils ont considéré la réaction enzymatique de diviser un dimère en deux molécules monomères. Compte tenu de la géométrie d'une telle enzyme-substrat-complexe, ils ont identifié trois règles d'or qui devraient être considérées comme construisant une enzyme fonctionnelle.
Tout d'abord, l'interface de l'enzyme et de la molécule doit être située à leur extrémité plus petite respective. De cette façon, un fort couplage entre les deux peut être réalisé. Pour la même raison, le changement de conformation dans l'enzyme ne doit pas être plus petit que dans la réaction. Enfin, le changement de conformation de l'enzyme doit avoir lieu assez rapidement pour maximiser la force motrice chimique de la réaction.
« Nous avons construit nos recherches sur deux piliers principaux », décrit Ramin Golestanian, directeur de MPI-DS, décrit l'approche.
« Conservation de l'élan et du couplage entre les coordonnées de réaction », poursuit-il.
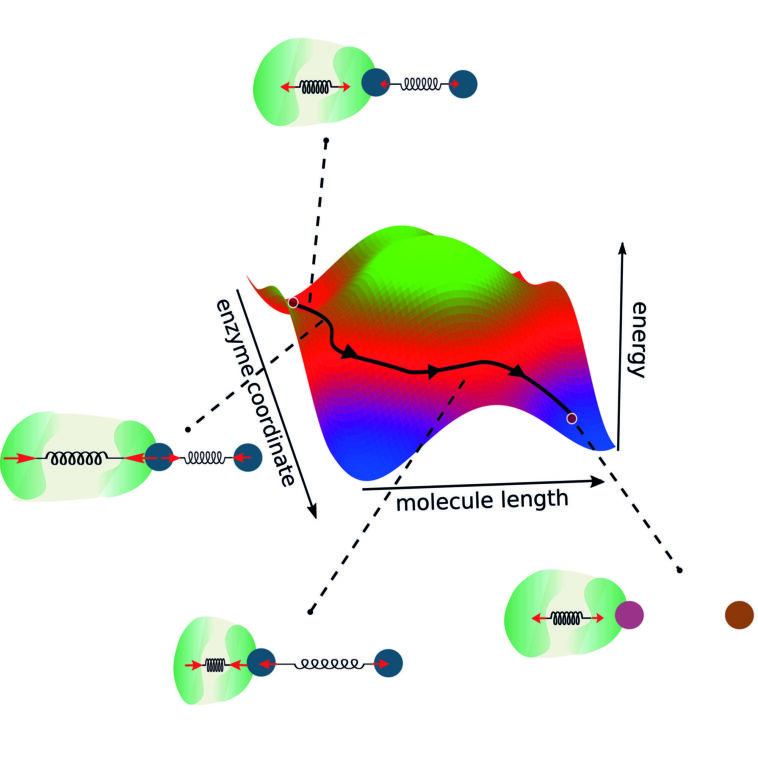
Ainsi, les chercheurs ont élargi la vision d'une coordonnée de réaction bidimensionnelle classique. En règle générale, les modèles de réactions enzymatiques définissent une barrière d'énergie qui doit être surmontée pour que la réaction ait lieu.
« Comme dans notre modèle, nous considérons également la dynamique et le couplage des enzymes, nous allons au-delà de ce concept existant, compte tenu de deux coordonnées de réaction », explique Michalis Chatzittofi, premier auteur de l'étude.
« Au lieu de surmonter une barrière énergétique, on peut maintenant imaginer d'autres moyens de le contourner en prenant des itinéraires alternatifs », conclut-il.
Ces résultats fournissent une nouvelle base pour la conception de machines moléculaires, en évitant l'approche fastidieuse et techniquement difficile pour simuler la dynamique de chaque atome individuellement.