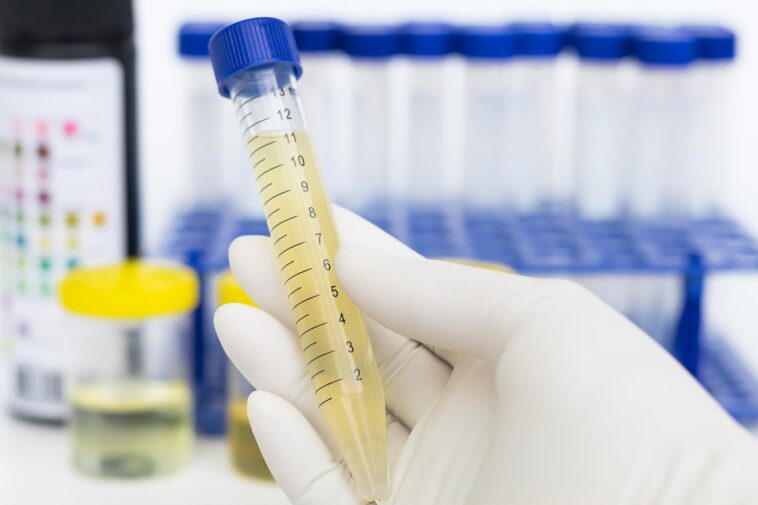
MyProstateScore 2.0, un test d'urine pour le cancer de la prostate, offre une grande précision et moins de biopsies inutiles par rapport aux tests PSA traditionnels, selon des recherches récentes.
Une étude en JAMA Oncologie révèle que MyProstateScore 2.0, un nouveau test d'urine analysant 18 gènes, surpasse le PSA dans la détection des cancers de la prostate importants et pourrait réduire jusqu'à 42 % les biopsies inutiles.
Un nouveau test d'urine mesurant 18 gènes associés au cancer de la prostate fournit des résultats plus élevés précision pour détecter les cancers cliniquement significatifs que le PSA et d'autres tests de biomarqueurs existants, selon une étude publiée le 18 avril dans JAMA Oncologie. Il a été démontré que le test d'urine, MyProstateScore 2.0 (MPS2), réduisait de manière significative les biopsies inutiles de la prostate tout en permettant une détection très précise des cancers de la prostate inquiétants, ont conclu les chercheurs.
« Chez près de 800 patients présentant un taux de PSA élevé, le nouveau test a pu exclure la présence d'un cancer de la prostate cliniquement significatif avec une précision remarquable. Cela permet aux patients d'éviter des tests plus lourds et invasifs, comme l'IRM et la biopsie de la prostate, avec la grande certitude que nous ne manquons rien », a déclaré Jeffrey Tosoian, MD, professeur adjoint d'urologie et directeur de la recherche translationnelle sur le cancer au centre médical de l'université Vanderbilt, qui est le premier auteur de l’étude.

Jeffrey Tosoian, MD, professeur adjoint d'urologie et directeur de la recherche translationnelle sur le cancer au centre médical de l'université Vanderbilt, premier auteur de l'étude. Crédit : Centre médical de l’Université Vanderbilt
Contexte du dépistage du cancer de la prostate
Le cancer de la prostate est le cancer le plus répandu et la deuxième cause de décès par cancer chez les hommes aux États-Unis. Le test sanguin PSA a été largement utilisé comme première étape du dépistage du cancer de la prostate. Bien que le PSA soit élevé chez la grande majorité des hommes atteints d’un cancer de la prostate, il l’est également chez une proportion significative d’hommes sans cancer.
En conséquence, l’utilisation d’un taux de PSA élevé seul pour provoquer une biopsie de la prostate entraîne de nombreuses biopsies inutiles. Bien que généralement sans danger, les biopsies de la prostate sont invasives, inconfortables et comportent un risque de complications inquiétantes. Par conséquent, pour les patients présentant un taux de PSA élevé, il existe un grand besoin d’un test de deuxième intention afin de mieux identifier quels hommes ont réellement besoin d’une biopsie et lesquels n’en ont pas besoin.
Développement de MPS2
Étant donné que certains cancers de la prostate de bas grade ne nécessitent pas de traitement et peuvent être surveillés en toute sécurité grâce à une approche appelée surveillance active, le test MPS2 a été développé pour détecter plus spécifiquement les cancers de grade supérieur, « cliniquement significatifs », nécessitant une détection et un traitement précoces. .
Pour ce faire, l’équipe de recherche a analysé des tumeurs de la prostate partout aux États-Unis afin d’identifier de nouveaux gènes plus souvent détectés en présence de cancers importants. Les 18 gènes les plus informatifs ont été combinés dans le test MPS2, qui a ensuite été testé dans le cadre d'un essai du National Cancer Institute portant sur des hommes présentant un taux de PSA élevé.
Fait unique, les auteurs ont pu comparer le nouveau test à d’autres tests du cancer de la prostate, y compris le test MPS original à deux gènes.
Résultats de l'étude et comparaison
L'étude a porté sur 743 hommes avec un âge médian de 62 ans et un taux médian de PSA de 5,6. Alors que les tests de biomarqueurs existants auraient pu éviter 15 à 30 % des biopsies inutiles (c'est-à-dire des biopsies négatives ou révélant des cancers de bas grade ne nécessitant pas de traitement), l'utilisation du MPS2 aurait évité 35 à 42 % de biopsies inutiles sans manquer d'éléments supplémentaires. diagnostics de cancer cliniquement significatif.
L'amélioration a été encore plus prononcée chez les hommes ayant des antécédents de biopsie négative, réduisant le taux de biopsies inutiles de 46 % à 51 % avec l'utilisation du MPS2, contre 9 % à 21 % pour les tests existants.
Recherches futures et limites
L'imagerie par résonance magnétique multiparamétrique (IRMmp) est un autre test de deuxième intention utilisé, mais même s'il peut améliorer la détection du cancer de la prostate cliniquement significatif, l'interprétation des résultats peut être subjective et varier considérablement. Les auteurs ont également noté que l’IRMmp n’est pas disponible dans certains milieux communautaires et ne constitue pas une option pour certains patients. L’étude actuelle n’a pas été conçue pour comparer les biomarqueurs à l’IRMmp, mais les chercheurs mènent actuellement un essai prospectif multicentrique à cette fin.
Chez les patients qui ne présentaient pas de cancer de la prostate cliniquement significatif selon le nouveau test, les auteurs ont conclu que « les performances validées en externe du MPS2 soutiennent son efficacité à exclure avec précision la nécessité d’une IRMmp et d’une biopsie ». Ils ont noté une limite de l’étude : seulement 13 % des participants étaient afro-américains. Le cancer de la prostate étant plus répandu chez les hommes afro-américains, l’équipe de recherche poursuit actuellement des analyses plus approfondies auprès de populations plus diversifiées sur le plan racial.
Pour en savoir plus sur cette recherche, voir Un nouveau test urinaire détecte le cancer de la prostate de haut grade.
Tosoian est co-premier auteur avec Yuping Zhang, PhD, et Lanbo Xiao, PhD, professeurs à l'Université du Michigan, où Tosoian et Arul Chinnaiyan, MD, PhD, ont lancé l'étude. Chinnaiyan et John T. Wei, MD, sont les auteurs principaux de l'étude. Les autres chercheurs de Vanderbilt qui ont contribué à l'étude sont Nathan Samora, MD, et Hunter Robinson, MD.
L’étude a reçu le soutien financier du Prostate Cancer Foundation Young Investigator Award (Tosoian), du Michigan-Vanderbilt EDRN Biomarker Characterization Center (U2C CA271854) et de l’EDRN DMCC (U24 CA086368).