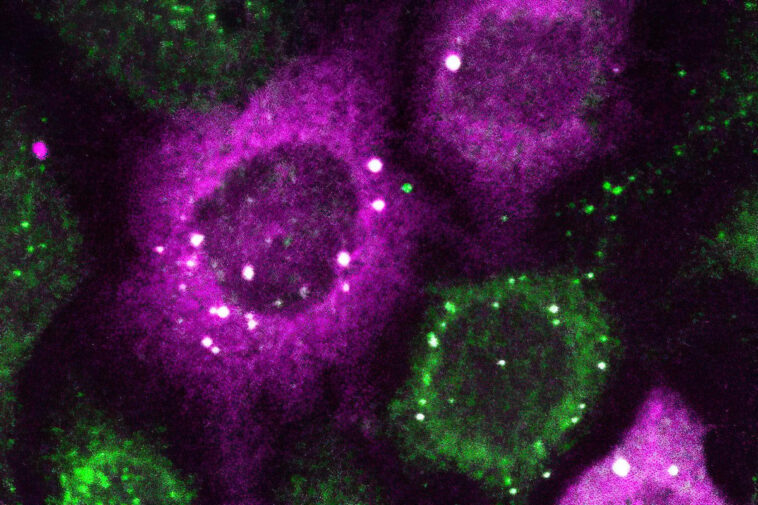
Les scientifiques ont introduit CluMPS, un nouvel outil moléculaire qui simplifie la détection de minuscules amas de protéines impliqués dans des maladies comme la maladie d’Alzheimer. Cette technique permet une visualisation facile avec des microscopes de laboratoire standards, surmontant les limites de la microscopie optique et facilitant l’évaluation de l’efficacité des médicaments et la découverte de nouveaux traitements. Le développement de CluMPS représente une avancée significative dans la compréhension de la fonction des protéines et du traitement des maladies. Les points blancs brillants représentent de minuscules amas de protéines détectées par CluMPS. Crédit : Thomas R. Mumford
Les chercheurs mettent l’accent sur les plus petits amas de protéines.
Les ingénieurs de Penn ont mis au point une nouvelle façon de visualiser les plus petits amas de protéines, contournant les limites physiques des microscopes alimentés par la lumière et ouvrant de nouvelles voies pour détecter les protéines impliquées dans des maladies telles que Alzheimer et tester de nouveaux traitements.
Dans un article en Systèmes cellulaires, Lukasz Bugaj, professeur adjoint en bioingénierie, décrit la création de CluMPS, ou Clusters Magnified by Phase Separation, un outil moléculaire qui s’active en formant des blobs visibles en présence d’amas de protéines cibles aussi petits que quelques nanomètres. Essentiellement, CluMPS fonctionne comme un interrupteur marche/arrêt qui répond à la présence d’amas de protéines qu’il est programmé pour détecter.
Normalement, explique Bugaj, la détection de tels clusters nécessite des techniques laborieuses. « Avec CluMPS, vous n’avez besoin de rien d’autre qu’un microscope de laboratoire standard. » L’outil fusionne avec la protéine cible pour former des condensats d’un ordre de grandeur plus grand que les amas de protéines eux-mêmes qui ressemblent aux gouttes colorées d’une lampe à lave. « Nous pensons que la simplicité de l’approche est l’un de ses principaux avantages », déclare Bugaj. « Vous n’avez pas besoin de compétences ou d’équipements spécialisés pour voir rapidement s’il y a de petits amas dans vos cellules. »
Potentiel dans le traitement des maladies et la découverte de médicaments
Pour traiter des maladies comme la maladie d’Alzheimer, la SLA et même le cancer, la capacité de détecter des amas de protéines aussi petits promet d’être une avancée fondamentale, permettant aux chercheurs de déterminer si les médicaments éliminent réellement les amas pathogènes d’une protéine cible dans une cellule.
« Il faut un signal très clair », explique Bugaj, pour savoir si un traitement a fonctionné ou non. « C’est très évident lorsqu’on a un cluster gigantesque, mais s’il y a de petits clusters, c’est beaucoup plus difficile. Nous pouvons désormais amplifier ce signal et voir quels médicaments dissolvent réellement les clusters.
Les points rouges et cyan représentent des groupes de protéines détectées par CluMPS. Crédit : Thomas R. Mumford
En plus d’ouvrir de nouvelles voies pour la découverte de médicaments, CluMPS permettra aux chercheurs de comprendre le fonctionnement des protéines de nouvelles manières, conduisant à un rendu plus profond et plus sophistiqué des cellules elles-mêmes. « Il existe tout un paysage de regroupement de protéines qui se produit à petite échelle, c’est important, mais nous ne le savons pas encore », explique Bugaj.
Surmonter les défis techniques
L’un des défis surmontés par CluMPS est que les ondes lumineuses elles-mêmes sont plus grandes que les plus petits amas de protéines, ce qui rend très difficile la visualisation de ces amas sans techniques spécialisées. « La longueur d’onde de la lumière bleue est d’environ 400 nanomètres », explique Bugaj. « Vous ne pouvez pas réellement déterminer l’emplacement de quelque chose de plus petit que la moitié de cette longueur d’onde avec un microscope conventionnel », ce qui rend les amas de protéines de plusieurs dizaines de nanomètres de large presque invisibles.
Pour développer CluMPS, Bugaj et son laboratoire se sont associés à Elizabeth Rhoades, professeur de chimie à Penn Arts & Sciences, dont le laboratoire a contribué à valider que CluMPS détectait effectivement des groupes de protéines cibles au lieu de générer de faux positifs. « Ce fut une collaboration très enrichissante pour nous », explique Rhoades, « car elle nous a permis d’appliquer les méthodes couramment utilisées par notre laboratoire pour valider ce nouvel outil puissant dans les cellules vivantes. C’était passionnant de voir à quel point nous pouvions différencier les clusters et les protéines uniques.
Thomas R. Mumford, doctorant au Bugaj Lab et auteur principal de l’article, a joué un rôle clé dans le brainstorming et la réalisation des expériences nécessaires. « Il était crucial de caractériser la façon dont les caractéristiques sous-jacentes des groupes de protéines interagissaient avec CluMPS pour déclencher la condensation », explique Mumford, afin de permettre aux futurs utilisateurs de la technologie de comprendre précisément son fonctionnement. « Il nous incombait de démontrer que nous détections effectivement de petits clusters », ajoute Bugaj. « L’un des aspects les plus gratifiants a été de travailler avec Tom et le laboratoire Rhoades pour réfléchir à de nouveaux types d’expériences qui permettraient de faire valoir ce point de manière convaincante. »
Cette étude a été menée à l’École d’ingénierie et de sciences appliquées de l’Université de Pennsylvanie et financée par des subventions du The Instituts nationaux de la santé décerné à Bugaj (R35GM138211) et au collaborateur Juan Guan (R35GM146877). Les autres co-auteurs incluent Diarmid Rae, Abbas Idris, David Gonzalez-Martinez et Ayush Aditya Pal de Penn Engineering ; Emily Brackhahn à Penn ; et Michael C. Chung et Juan Guan au Université de Floride.