Des chercheurs ont décodé le génome de Épulopiscium viviparus, une bactérie géante vivant chez le poisson chirurgien, révélant des adaptations métaboliques et des méthodes de production d’énergie uniques. Cette étude offre des applications potentielles dans la nutrition et l’énergie à base d’algues. Crédit : Issues.fr.com
Une étude révolutionnaire sur la bactérie géante Épulopiscium viviparus montre sa production d’énergie unique, prometteuse de futures applications dans l’utilisation des algues.
Toutes les bactéries ne sont pas créées égales.
La plupart sont unicellulaires et minuscules, mesurant quelques dix millièmes de centimètre de long. Mais les bactéries de la famille des Epulopiscium sont suffisamment grosses pour être visibles à l’œil nu et représentent 1 million de fois le volume de leurs cousines plus connues, E. coli.
Découverte et étude d’une bactérie géante
Dans une étude publiée récemment dans Actes de l’Académie nationale des sciencesdes chercheurs du laboratoire national Cornell et Lawrence Berkeley ont décrit pour la première fois le génome complet d’un espèces de la famille des géants, qu’ils ont nommé Épulopiscium viviparus.
« Cette incroyable bactérie géante est unique et intéressante à bien des égards : sa taille énorme, son mode de reproduction, les méthodes par lesquelles elle répond à ses besoins métaboliques et bien plus encore », a déclaré Esther Angert, professeur de microbiologie au Collège d’agriculture et de vie. Sciences, et auteur correspondant de l’étude. « Révéler le potentiel génomique de cet organisme nous a en quelque sorte époustouflé. »
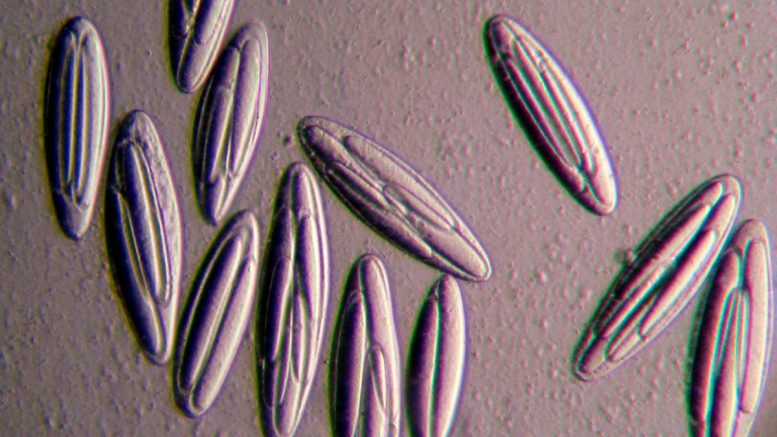
Micrographie d’un groupe de Épulopiscium viviparus bactéries. Crédit : Esther Angert
Habitat et caractéristiques
Le premier membre de la famille des Epulopiscium a été découvert en 1985. Tous les membres de l’espèce vivent en symbiose dans le tractus intestinal de certains poissons-chirurgiens dans les récifs coralliens marins tropicaux, comme la Grande Barrière de corail et la mer Rouge.
En raison de sa taille gargantuesque, les scientifiques ont d’abord cru qu’il s’agissait d’un type distinct de protozoaire, a expliqué Angert. Le nom Epulopiscium vient des racines latines epulo, qui signifie « un invité » et piscium, « d’un poisson ». Alors que la plupart des bactéries se reproduisent en se divisant en deux pour créer deux descendants, E. viviparus créer jusqu’à 12 copies d’eux-mêmes, qui grandissent à l’intérieur d’une cellule mère puis sont libérées, « actives et nageant – viviparus signifie « naissance vivante » », a déclaré Angert.
Méthodologie de recherche
L’étude de ces bactéries géantes nécessite de capturer les poissons dans lesquels elles vivent et d’en préserver les cellules ou d’en extraire ADN et ARN aussi rapidement et soigneusement que possible, a déclaré Angert, qui collabore depuis des décennies avec des biologistes des poissons de la station de recherche de Lizard Island en Australie pour collecter et étudier des échantillons.
Informations métaboliques
Les chercheurs étaient particulièrement intéressés de savoir comment E. viviparus alimente ses besoins métaboliques extrêmes. Les bactéries qui se nourrissent des nutriments présents dans leur environnement, plutôt que de créer leur propre énergie à partir de la lumière du soleil, se répartissent généralement en deux camps : celles qui ont accès à l’oxygène et celles qui n’y ont pas accès. Sans oxygène, les bactéries utilisent souvent la fermentation pour extraire de l’énergie, et « les organismes en fermentation n’en ont tout simplement pas pour leur argent en termes de nutriments », a déclaré Angert.
Vu que E. viviparus est en effet un fermenteur qui vient d’agrandir le puzzle, car sa taille énorme, sa reproduction extrême et sa capacité à nager nécessiteraient toutes plus d’énergie, pas moins.
Adaptations génétiques et production d’énergie
Les chercheurs ont découvert que E. viviparus a modifié son métabolisme pour tirer le meilleur parti de son environnement, en utilisant une méthode rare pour produire de l’énergie et se déplacer (la même méthode de nage est utilisée par les bactéries responsables du choléra), et en consacrant une grande partie de son code génétique à fabriquer enzymes capables de récolter les nutriments disponibles dans l’intestin de son hôte. Parmi les enzymes les plus produites figurent celles utilisées pour fabriquer l’ATP, la monnaie énergétique de toutes les cellules. Une membrane très pliée qui s’étend le long du bord extérieur de E. viviparus fournit un espace important pour les protéines productrices et transporteuses d’énergie, avec des similitudes surprenantes avec le fonctionnement des mitochondries dans les cellules d’organismes plus complexes, a déclaré Angert.
« Nous connaissons tous cette expression » les mitochondries sont le moteur de la cellule « », a déclaré Angert, « et étonnamment, ces membranes dans E. viviparus ont en quelque sorte convergé vers le même modèle que les mitochondries : elles ont une membrane hautement pliée qui augmente la surface sur laquelle ces pompes productrices d’énergie peuvent fonctionner, et cette surface accrue crée une centrale d’énergie.
Applications potentielles et recherches futures
Cette recherche fondamentale a de nombreuses applications futures potentielles, notamment E. viviparus dispose de stratégies très efficaces pour utiliser les nutriments présents dans les algues, a déclaré Angert. Les algues constituent une cible croissante pour l’alimentation du bétail, les énergies renouvelables et la nutrition humaine, car leur croissance ne concurrence pas l’agriculture terrestre.
Le premier auteur de l’étude est David Sannino, Ph.D. ’17, ancien associé postdoctoral dans le laboratoire d’Angert. Les autres co-auteurs sont Francine Arroyo, Ph.D. ’19 et anciens chercheurs postdoctoraux Charles Pepe-Ranney et Wenbo Chen ; et Jean-Marie Volland et Nathalie Elisabeth, tous deux du Lawrence Berkeley National Laboratory.
Cette recherche a été soutenue par la National Science Foundation et le ministère de l’Énergie.