Une étude a révélé que le virus SARS-CoV-2 peut rester dans les poumons jusqu’à 18 mois après l’infection, remettant en question l’idée selon laquelle il est indétectable après la guérison initiale. Cette persistance est liée à une défaillance du système immunitaire inné. La recherche, confirmant l’existence de « réservoirs viraux » similaires à ceux du VIH, met en évidence le rôle des cellules NK dans le contrôle de ces réservoirs. Cette découverte est cruciale pour comprendre le long COVID et les mécanismes de persistance virale.
Une étude révolutionnaire révèle que SRAS-CoV-2 peut persister dans les poumons pendant des mois, échappant à la détection et pouvant conduire à un long COVID, en raison de défaillances du système immunitaire inné.
Une à deux semaines après avoir contracté le COVID, le SARS-CoV-2 virus devient généralement indétectable dans les voies respiratoires supérieures. Mais cela signifie-t-il qu’il n’est plus présent dans l’organisme ? Pour le savoir, une équipe de l’Institut Pasteur spécialisée dans le VIH, en collaboration avec un institut de recherche public français, le Commissariat aux énergies alternatives et à l’énergie atomique (CEA), a mené une étude sur des cellules pulmonaires dans un modèle animal. Les résultats montrent non seulement que le SARS-CoV-2 est retrouvé dans les poumons de certains individus jusqu’à 18 mois après l’infection, mais aussi que sa persistance semble être liée à une défaillance de l’immunité innée (la première ligne de défense contre les agents pathogènes). ). Cette recherche a été publiée dans la revue Immunologie naturelle.
Découverte de réservoirs viraux dans le COVID-19
Certains virus persistent dans l’organisme de manière discrète et indétectable après avoir provoqué une infection. Ils restent dans ce que l’on appelle des « réservoirs viraux ». C’est le cas du VIH, qui reste latent dans certaines cellules immunitaires et peut se réactiver à tout moment. Cela pourrait également être le cas du virus SARS-CoV-2 qui provoque COVID 19. C’est du moins l’hypothèse avancée par une équipe de scientifiques de l’Institut Pasteur en 2021, et qui vient d’être confirmée dans un modèle préclinique de primate non humain.
« Nous avons observé que l’inflammation persistait pendant de longues périodes chez les primates infectés par le SRAS-CoV-2. Nous avons donc soupçonné que cela pouvait être dû à la présence du virus dans l’organisme», explique Michaela Müller-Trutwin, responsable de l’unité VIH, inflammation et persistance de l’Institut Pasteur.
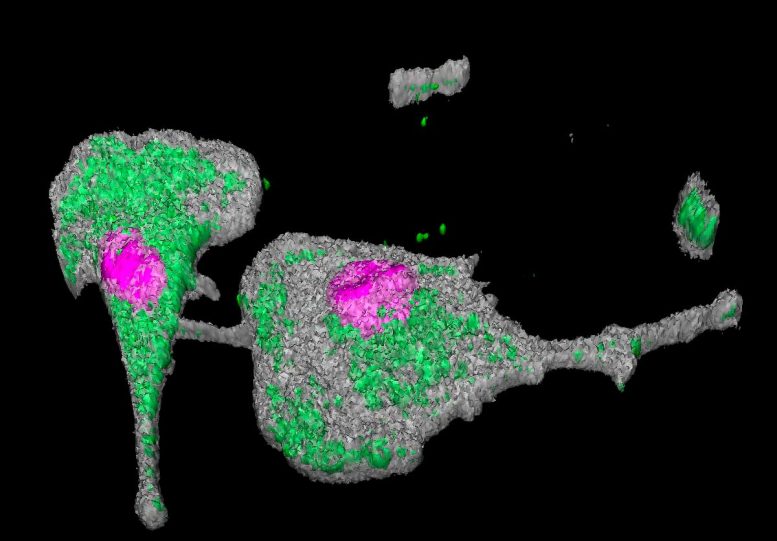
L’étude a montré que le virus SARS-CoV-2 se transmet d’un macrophage à un autre via des projections cellulaires en forme de pont, lui permettant de se propager. Le noyau cellulaire est surligné en rose et la protéine virale NSP3 est surlignée en vert. Crédit : © Marie Lazzerini, Nicolas Huot, Institut Pasteur
Résultats de l’étude
Pour étudier la persistance du virus SARS-CoV-2, des scientifiques de l’Institut Pasteur, en collaboration avec le centre IDMIT (Modèles de maladies infectieuses pour des thérapies innovantes) du CEA, ont analysé des échantillons biologiques issus de modèles animaux infectés par le virus. Les premiers résultats de l’étude indiquent que des virus ont été détectés dans les poumons de certaines personnes 6 à 18 mois après l’infection, même si le virus était indétectable dans les voies respiratoires supérieures ou dans le sang. Une autre découverte était que la quantité de virus persistant dans les poumons était plus faible pour la souche Omicron que pour la souche originale du SRAS-CoV-2.
« Nous avons été très surpris de retrouver des virus dans certaines cellules immunitaires – les macrophages alvéolaires – après une si longue période et alors que les tests PCR réguliers étaient négatifs », souligne Nicolas Huot, premier auteur de l’étude et chercheur à l’Institut Pasteur VIH, Inflammation et Unité de persistance. « De plus, nous avons cultivé ces virus et avons pu observer, grâce aux outils que nous avons développés pour étudier le VIH, qu’ils étaient encore capables de se répliquer. »
Pour comprendre le rôle de l’immunité innée dans le contrôle de ces réservoirs viraux, les scientifiques se sont ensuite tournés vers les cellules NK (natural killer). «La réponse cellulaire de l’immunité innée, qui constitue la première ligne de défense de l’organisme, a jusqu’à présent été peu étudiée dans les infections par le SRAS-CoV-2», explique Michaela Müller-Trutwin. « Pourtant, on sait depuis longtemps que les cellules NK jouent un rôle important dans le contrôle des infections virales. » L’étude montre que chez certains animaux, les macrophages infectés par le SRAS-CoV-2 deviennent résistants à la destruction par les cellules NK, tandis que chez d’autres, les cellules NK sont capables de s’adapter à l’infection (appelées cellules NK adaptatives) et de détruire les cellules résistantes. cas des macrophages.
L’étude a donc mis en lumière un mécanisme qui pourrait expliquer la présence de « réservoirs viraux » : alors que les individus avec peu ou pas de virus à long terme avaient une production adaptative de cellules NK, les individus avec des niveaux plus élevés de virus n’avaient pas seulement une absence de cellules NK adaptatives. cellules, mais également une réduction de l’activité des cellules NK. L’immunité innée semble donc jouer un rôle dans le contrôle des virus SARS-CoV-2 persistants.
Orientations futures de la recherche
« Nous allons nous lancer dans une étude d’une cohorte infectée par le SARS-CoV-2 au début de la pandémie pour savoir si les réservoirs viraux et les mécanismes identifiés sont liés à des cas de COVID long. Mais les résultats ici représentent déjà une étape importante dans la compréhension de la nature des réservoirs viraux et des mécanismes qui régulent la persistance virale », explique Michaela Müller-Trutwin.
Cette recherche a été financée principalement par une famille de donateurs majeurs dans le cadre de l’appel à projets du Programme de recherche COVID.