La spiroaspertrione A est un composé polycyclique complexe produit naturellement par le champignon Aspergillus sp. TJ23. Isolé pour la première fois en 2017, il a rapidement attiré l’attention des scientifiques pour sa capacité prometteuse à combattre les bactéries résistantes aux médicaments et à restaurer leur sensibilité aux antibiotiques existants.
Les scientifiques ont désormais trouvé un moyen de réaliser la synthèse totale de la molécule en 16 étapes, à partir d'un élément constitutif du pool chiral appelé (+)-énoxolone qui coûte moins d'un euro par gramme. La technique de synthèse est présentée dans Science.
Staphylococcus aureus (staphylocoque) est un type de bactérie qui vit tranquillement sur notre peau et dans notre nez. Cela ne fait généralement pas de mal, mais lorsqu’il devient invasif, il déclenche des infections dangereuses comme la septicémie, la pneumonie et de nombreuses infections nosocomiales. Ce qui la rend vraiment alarmante, c’est sa résistance croissante aux antibiotiques, qui peut transformer des infections traitables en menaces mortelles.
Rien qu’en 2021, le staphylocoque résistant à la méthicilline ou SARM a entraîné 130 000 décès dans le monde. Un moyen prometteur de lutter contre la résistance aux antibiotiques consiste à utiliser de petites molécules comme la (-)-spiroaspertrione A qui peuvent rendre le SARM à nouveau sensible aux médicaments existants.
Depuis la découverte de ses propriétés thérapeutiques, les scientifiques tentent de développer des stratégies efficaces pour synthétiser la molécule en laboratoire.
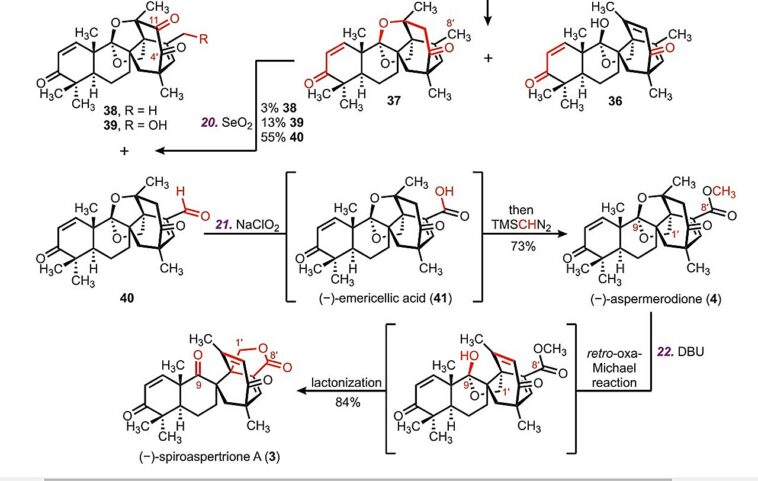
Le principal goulot d’étranglement a été la formation du noyau spirobicyclo(3.2.2)nonane de la molécule. Pour construire l'échafaudage spirobicyclique, des centres quaternaires doivent être formés en C8 et C2'. Cependant, la nature hautement fonctionnalisée du squelette polycyclique qui compose la molécule forme une structure en forme de cage serrée qui empêche d’autres modifications. Il empêche les groupes chimiques d’accéder aux sites réactifs et de déclencher la réaction.
Pour surmonter les obstacles structurels, les chercheurs ont effectué une cycloaddition Diels – Alder suivie d'un réarrangement clé du divinylcyclopropane (DVCPR). Au lieu d’ajouter des groupes à un squelette déjà encombré, ils ont créé une molécule précurseur flexible et l’ont chauffée à 180°C. Ce chauffage a déclenché la réorganisation des atomes et la formation du noyau de spirobicyclo(3.2.2)nonane en forme de cage en une seule étape, un mécanisme soutenu en outre par les calculs de la théorie fonctionnelle de la densité (DFT).
Une fois la structure centrale de la molécule cible en place, les chercheurs ont soigneusement ajouté de l’oxygène et d’autres groupes fonctionnels à des positions précises. Grâce à une série de réactions d’oxydation, ils ont produit un aldéhyde, qui a ensuite été transformé en (-)-aspermérodione. Lorsque ce composé a été chauffé avec une base, il a subi un réarrangement moléculaire qui a fermé le cycle et donné le produit final : la (-)-spiroaspertrione A.
Bien que le rendement soit de 2,3 %, ce qui est assez faible, l’étude a réussi à synthétiser complètement un composé anti-SARM à partir d’un précurseur peu coûteux et disponible dans le commerce.
Les chercheurs ont noté que grâce à ce processus, ils devaient mieux comprendre les structures d’autres molécules au sein de la famille des produits naturels. Ces résultats pourraient guider la conception de nouveaux composés capables de resensibiliser les bactéries résistantes aux antibiotiques aux médicaments existants.
Écrit pour vous par notre auteur Sanjukta Mondal, édité par Stephanie Baum, et vérifié et révisé par Robert Egan, cet article est le résultat d'un travail humain minutieux. Nous comptons sur des lecteurs comme vous pour maintenir en vie le journalisme scientifique indépendant. Si ce reporting vous intéresse, pensez à faire un don (surtout mensuel). Vous obtiendrez un sans publicité compte en guise de remerciement.