Des chercheurs du Fritz Haber Institute de la Max Planck Society ont dévoilé de nouvelles perspectives sur l'activité des catalyseurs utilisés dans la production d'hydrogène vert.
Leur étude, publiée dans Chimie de la natureexplore comment la cinétique du catalyseur est liée à une interaction complexe entre le solvant interfacial et les changements chimiques sur la surface du catalyseur, ouvrant potentiellement la voie à des technologies de conversion d'énergie plus efficaces.
Le Département des sciences de l'interface de l'Institut Fritz Haber a fait des progrès importants dans la compréhension du fonctionnement des catalyseurs dans des environnements aqueux. Cette recherche est cruciale pour faire progresser les technologies comme la production d'hydrogène vert, qui repose sur des catalyseurs efficaces pour diviser les molécules d'eau.
L'étude, dirigée par le Dr Martinez-Hincapié et le Dr Oener au sein du département FHI du professeur Roldán Cuenya, utilise une électrochimie dépendante de la température et une spectroscopie d'opérando pour étudier la réaction d'évolution de l'oxygène (OER). Cette réaction est un goulot d'étranglement de l'électrolyse d'eau, où la cinétique OER lente peut entraver la production d'hydrogène. Les chercheurs ont découvert un point de transition clé dans la cinétique dépendante du biais où l'activité du catalyseur passe de la limite par l'accumulation d'une charge excessive à devenir très active.
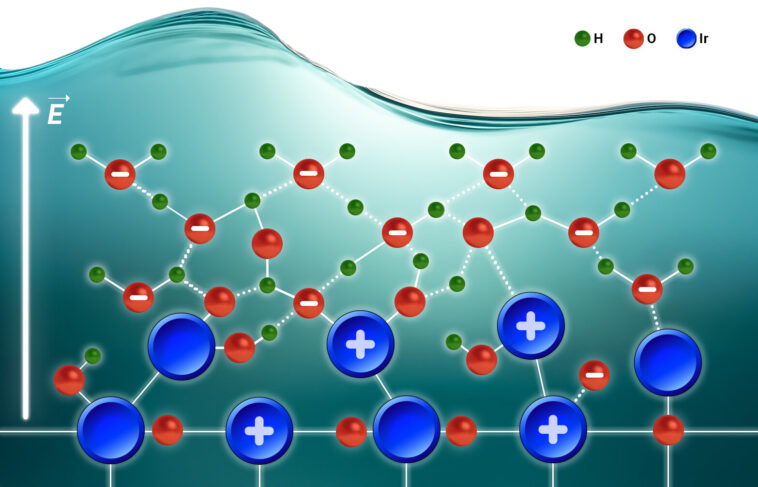
Une découverte critique de l'étude est le rôle de la solvatation interfaciale – un processus par lequel les ions perdent ou gagnent des molécules de solvant. Cette étape initiale semble être cruciale pour l'activité intrinsèque du catalyseur.
Le Dr Oener explique: « Nous devons vraiment réfléchir à l'interphase catalyseur-électrolyte dans son ensemble, pas en termes distincts. Nous ne pouvons pas comprendre la stabilisation de la charge excessive du côté solide sans la réponse du solvant et nous ne pouvons pas comprendre la solvation des ions interfaciaux sans considérer soigneusement ce qui se passe du côté solide.
« Cela est particulièrement critique car l'interface solide connaît également des changements structurels et chimiques drastiques au cours de la réaction. C'est une interphase qui donne naissance à l'activité observée. »

En termes plus techniques, l'étude révèle que la cinétique du catalyseur est régie par une interaction complexe entre l'adaptation chimique et structurelle de la surface de l'oxyde et la réponse des molécules d'eau interfaciales. En utilisant la spectroscopie aux rayons X de l'Operando, l'équipe a observé des adaptations structurelles et chimiques des catalyseurs d'oxyde juste à un potentiel de transition important dans la cinétique.
Surtout, ce potentiel de transition ne dépend pas de la charge de catalyseur (la quantité de matériau utilisée), ni de sa surface. Cela indique que l'activité du catalyseur est intrinsèquement liée à sa capacité à développer une charge excessive pour interagir avec les ions solvatés à partir de l'électrolyte liquide.
Le professeur Beatriz Roldán Cuenya souligne l'importance de combiner différentes techniques d'opérando spectro-microscopie qui informent la surface du catalyseur, le solvant et la cinétique fondamentale. Cela est nécessaire pour mieux comprendre le comportement du catalyseur.
La recherche fait non seulement progresser notre compréhension de l'activité du catalyseur, mais est également prometteuse pour améliorer les technologies de conversion d'énergie. L'équipe s'est engagée à explorer davantage ces résultats, avec le potentiel d'avoir un impact significatif sur les domaines de la technologie de conversion énergétique et chimique.