Les chercheurs de l'UC San Diego ont lié les modifications du métabolisme lipidique à la progression de la maladie d'Alzheimer, identifiant de nouveaux traitements potentiels en ciblant l'enzyme AMPK pour perturber un cycle d'inflammation cérébrale.
Les chercheurs de l'UC San Diego ont utilisé des techniques d'imagerie avancées pour explorer les processus métaboliques à l'origine de la maladie d'Alzheimer, conduisant ainsi à de nouvelles stratégies potentielles de traitement.
Alzheimer La maladie, le type de démence le plus courant, altère considérablement la mémoire, la pensée et le comportement, touchant plus de 50 millions de personnes dans le monde chaque année. Les projections suggèrent que ce nombre triplera d’ici 2050.
En utilisant leurs propres technologies d'imagerie de pointe, des scientifiques de l'Université de Californie à San Diego ont révélé comment le métabolisme des lipides, une classe de molécules qui comprend les graisses, les huiles et de nombreuses hormones, est modifié dans la maladie d'Alzheimer. Ils ont également révélé une nouvelle stratégie visant à cibler ce système métabolique avec des médicaments nouveaux et existants. Les résultats sont publiés dans Métabolisme cellulaire.
« Les lipides sont associés à la maladie d'Alzheimer depuis aussi longtemps que nous connaissons la maladie », a déclaré l'auteur principal et co-correspondant Xu Chen, Ph.D., professeur adjoint au département de neurosciences de la faculté de médecine de l'UC San Diego. , faisant référence au rapport original d'Alois Alzheimer de 1907 qui décrivait la présence inhabituelle de dépôts graisseux dans le cerveau de la première personne à qui la maladie a été diagnostiquée. « Depuis lors, l’accent a été tellement mis sur la protéine Tau et d’autres protéines que la communauté des chercheurs a, jusqu’à la dernière décennie, largement négligé cet aspect important de la maladie. »
Techniques d'imagerie innovantes
« Poussés par un vif intérêt pour les fonctions des gouttelettes lipidiques dans le vieillissement et la maladie, nous avons lancé cette collaboration fructueuse pour exploiter la technologie SRS de pointe pour étudier le métabolisme lipidique dans les cerveaux de souris tauopathie. » A déclaré Yajuan Li, MD, Ph.D., chercheur postdoctoral au département de bio-ingénierie Shu Chien-Gene Lay de la Jacobs School of Engineering de l'UC San Diego. L'imagerie SRS est une approche qui analyse la manière dont les molécules d'un échantillon interagissent avec la lumière laser.
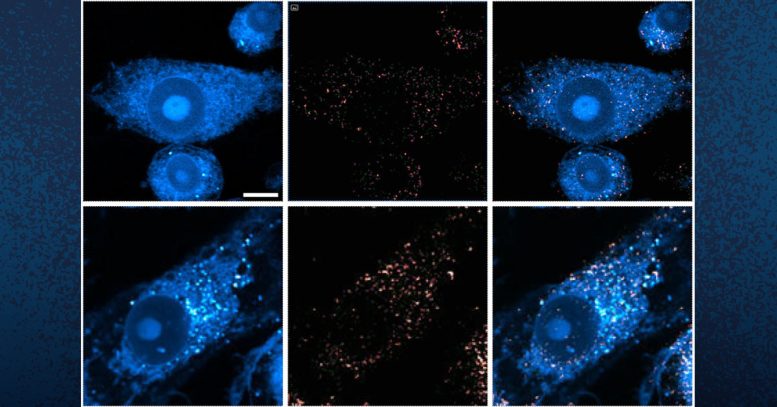
Ces images montrent des microglies contenant des gouttelettes lipidiques (taches blanches). Des chercheurs de l'UC San Diego ont révélé que dans les cerveaux atteints de la maladie d'Alzheimer et de maladies apparentées, les neurones déchargent les gouttelettes lipidiques en excès vers la microglie, ce qui déclenche une inflammation supplémentaire. Crédit : Sciences de la santé de l’UC San Diego
Dans le cerveau, les lipides se présentent sous la forme de minuscules gouttelettes qui contrôlent divers processus, tels que le stockage d’énergie et les réponses cellulaires au stress. Ces processus sont étroitement régulés dans le cerveau typique, mais dans la maladie d'Alzheimer ou des maladies similaires, le métabolisme des gouttelettes lipidiques peut mal fonctionner. Bien que les scientifiques comprennent qu'il existe une relation entre la maladie d'Alzheimer et le métabolisme des lipides, la manière exacte dont ils s'influencent mutuellement reste un mystère.
Pour répondre à cette question, l’équipe a examiné directement les gouttelettes lipidiques présentes dans le cerveau de souris présentant un excès de protéine tau. Ils ont utilisé une plate-forme d'imagerie SRS de pointe développée dans le laboratoire de Lingyan Shi à la Jacobs School of Engineering. La plateforme permet de prendre des images microscopiques de gouttelettes lipidiques dans les cellules sans utiliser de colorants chimiques, qui peuvent altérer les molécules délicates et compromettre les résultats.
Mécanismes et implications
« Curieusement, les gouttelettes lipidiques inertes observées dans les cerveaux de tauopathie présentent un comportement similaire à ceux trouvés dans les cerveaux vieillissants », a déclaré l'auteur co-correspondant Lingyan Shi, Ph.D., professeur adjoint de bio-ingénierie à l'école Jacobs. « Nous nous concentrons désormais sur la compréhension des mécanismes sous-jacents en combinant l’imagerie SRS avec d’autres techniques multidisciplinaires. Notre approche est biologiquement neutre, nous pouvons donc observer ce qui se passe dans le cerveau au niveau moléculaire avec le moins d'interférences possible.
Shi et son équipe, dont Li, ont été les pionniers de cette nouvelle approche, qui utilise une version spécialement modifiée de l'eau, appelée eau lourde, comme sonde métabolique.
« Au lieu d'utiliser un colorant chimique classique pour colorer les lipides, nous utilisons de l'eau lourde qui participe naturellement aux activités métaboliques qui nous intéressent », a ajouté Shi. « Cela nous donne une image beaucoup plus claire de la façon dont les lipides se forment dans l’espace et dans le temps, ce qui ne serait pas possible avec d’autres approches. Notre objectif actuel est de comprendre les mécanismes sous-jacents de ces changements dynamiques du métabolisme lipidique dans le contexte du vieillissement et des maladies.
Les chercheurs ont découvert que dans les cerveaux atteints de tauopathie, les neurones accumulent un excès de lipides en raison du stress ou de dommages. Cet afflux oblige les neurones à décharger l’excédent vers les cellules immunitaires du cerveau, appelées microglies. Ces microglies déclenchent alors une réponse inflammatoire qui provoque un stress supplémentaire sur les neurones, déclenchant un cycle répété et aggravé.
En plus de caractériser ce processus, ils ont également pu identifier une enzyme essentielle, appelée protéine kinase activée par l'adénosine monophosphate (AMPK), qui orchestre le cycle. Selon les chercheurs, briser ce cycle pourrait ouvrir la voie à de nouvelles options de traitement pour la maladie d'Alzheimer. Chen est particulièrement optimiste quant à la possibilité de réutiliser les médicaments existants qui modifient le métabolisme des lipides.
« Nous ne pensons pas qu'il s'agisse d'un phénomène fortuit », a déclaré Chen. « Les preuves suggèrent que le métabolisme des lipides est un mécanisme moteur de la maladie d'Alzheimer. Il existe de nombreux médicaments qui ciblent le métabolisme des lipides dans d’autres systèmes du corps, comme dans le foie, nous pourrions donc être en mesure de modifier ce système de manière assez radicale en utilisant les outils dont nous disposons déjà.
Ce travail a été financé en partie par le Instituts nationaux de la santé (subventions R01AG074273, R01AG078185, 1R01GM149976-01, R01NS111039 R21NS125395) et par le fonds de démarrage du département des neurosciences de l'UC San Diego et de la Jacob School of Engineering.