Une étude récente de Scripps Research a identifié les structures détaillées des PLD3 et PLD4, des enzymes essentielles à la dégradation des acides nucléiques et à la régulation immunitaire. La découverte, permettant de comprendre des maladies comme le lupus, la polyarthrite rhumatoïde et la maladie d'Alzheimer, révèle de nouvelles fonctions enzymatiques et constitue une base pour de futures approches thérapeutiques ciblant ces enzymes.
Les scientifiques de Scripps Research ont développé des modèles structurels au niveau atomique d'enzymes liées à des maladies auto-immunes et inflammatoires, telles que le lupus et la maladie d'Alzheimer.
Lorsque les acides nucléiques, tels que ADN ou ARN, s'accumulent dans le cytoplasme d'une cellule, ils déclenchent une alerte du système immunitaire. Dans des circonstances normales, les enzymes sont chargées d’éliminer ces acides nucléiques pour éviter les problèmes. Cependant, si ces enzymes ne fonctionnent pas correctement et que le système immunitaire intervient, cela peut entraîner des maladies auto-immunes et inflammatoires.
Dans une nouvelle étude récemment publiée dans la revue Structureles scientifiques de Scripps Research présentent la structure jusqu'alors non décrite de deux de ces éléments nucléiques. acide-enzymes dégradantes – PLD3 et PLD4. Comprendre les structures et les détails moléculaires de ces enzymes constitue une étape importante vers la conception de traitements pour les diverses maladies qui surviennent en cas de dysfonctionnement de celles-ci, notamment le lupus érythémateux, la polyarthrite rhumatoïde et Alzheimer maladie.
« Ces enzymes sont importantes pour nettoyer l'environnement cellulaire, et elles fixent également le seuil de ce qui est considéré ou non comme une infection », explique l'auteur principal David Nemazee, PhD, professeur au Département d'immunologie et de microbiologie de Scripps Research. « J'espère qu'un jour nous pourrons aider les patients sur la base de ces informations. »
Fonctionnalité des enzymes et techniques d'analyse
Les enzymes sont des protéines qui accélèrent les réactions chimiques en se liant et en réagissant à des molécules spécifiques appelées substrats. Dans le cas des PLD3 et PLD4, le substrat est un brin d'ARN ou d'ADN, que les enzymes décomposent nucléotide par nucléotide.
L’équipe a utilisé la cristallographie aux rayons X pour construire des modèles à l’échelle atomique des PLD3 et PLD4 dans plusieurs états ou situations, leur permettant ainsi d’examiner comment leurs formes ont changé au cours de la réaction catalytique. Cela incluait le moment où les enzymes étaient au repos ou lorsqu'elles étaient activement liées à un substrat.
« Ces modèles nous permettent de visualiser les PLD3 et PLD4 très clairement et avec une haute résolution, nous savons donc exactement comment chaque atome interagit, ce qui signifie que nous pouvons déduire le fonctionnement des enzymes », explique le premier auteur Meng Yuan, scientifique au Département de biologie structurale et computationnelle intégrative de Scripps Research.
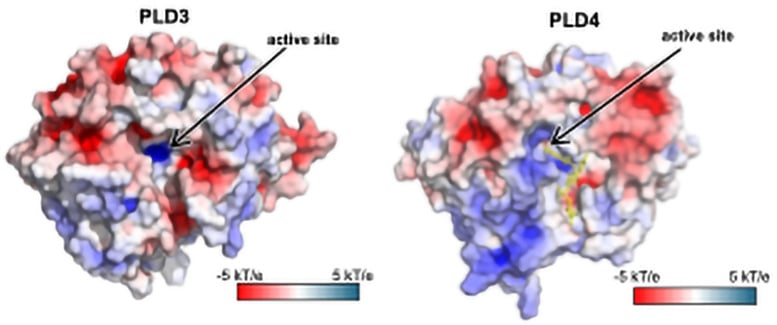
Modèles structurels de PLD3 et PLD4, enzymes qui dégradent les acides nucléiques dans le cytoplasme. Les sites actifs (ou de liaison) des enzymes sont indiqués par des flèches noires. Crédit : Recherche Scripps
Les analyses structurelles ont révélé que PLD3 et PLD4 sont structurellement similaires et qu'elles dégradent l'ADN et l'ARN de manière très similaire, même si PLD4 est une protéine plus grosse. Les deux enzymes dégradent les acides nucléiques via un processus en deux étapes.
« Nous appelons ce processus une catalyse en deux étapes : mordre et relâcher », explique Yuan. « Dans la première étape, l'enzyme mord le brin d'ADN et sépare une seule « brique » ou nucléotide du reste du brin, et dans la deuxième étape, elle ouvre sa « bouche » et libère la brique à recycler. »
Parce que la réaction enzymatique se produit si rapidement (en quelques millisecondes), les chercheurs ont dû utiliser un substrat alternatif pour visualiser la structure des enzymes pendant la catalyse. Pour ce faire, ils ont incubé les enzymes avec une molécule qui ressemble beaucoup à l'ADN que l'enzyme dégrade habituellement, mais que les enzymes se dégradent beaucoup plus lentement.
Découvrir de nouvelles fonctions enzymatiques
Cette méthode a révélé une fonction jusqu'alors inconnue de l'une des enzymes : en plus de mordre les nucléotides de l'ARN et de l'ADN simple brin, le PLD4 a également montré une activité phosphatase, ce qui signifie qu'il pourrait également être impliqué dans la dégradation du squelette phosphate de l'ADN.
« Je pense qu'il est étonnant que la structure cristalline nous ait informé de cette activité phosphatase », explique Nemazee. «Découvrir une nouvelle activité enzymatique est du jamais vu en biologie structurale. C’est uniquement parce que Meng a été capable de résoudre une structure aussi incroyablement précise et détaillée qu’il a pu nous informer de cette activité enzymatique supplémentaire dont nous n’avions aucune idée.
Après avoir élucidé la structure habituelle de PLD3 et PLD4, les chercheurs ont examiné la structure des variantes associées à des maladies, notamment la maladie d'Alzheimer et l'ataxie spinocérébelleuse. Ces analyses ont révélé que certaines de ces variantes avaient une capacité enzymatique réduite, tandis que d'autres, notamment une mutation associée à la maladie d'Alzheimer à apparition tardive, semblaient être plus actives.
« Certaines de nos données suggèrent que l'une de ces variantes enzymatiques associées à la maladie d'Alzheimer pourrait mieux fonctionner, ce qui m'a surpris, mais elle pourrait également être moins stable et plus facilement agrégée », explique Nemazee.
Les chercheurs prévoient de continuer à étudier la structure et la fonction de ces enzymes. Leurs prochaines étapes consistent à explorer les moyens possibles d'inhiber les enzymes dans des scénarios où elles sont hyperactives, et ils prévoient également d'étudier la possibilité de remplacer les enzymes chez les personnes porteuses de versions non fonctionnelles (ou inopérantes).
Cette étude a été soutenue par le Instituts nationaux de la santé (subventions R01AI142945 et RF1AG070775) et Institut Skaggs de biologie chimique à Scripps Research.




