Les chercheurs de Caltech ont développé un système d’administration de médicaments activé par ultrasons pour le traitement du cancer, promettant une thérapie ciblée avec des effets secondaires minimes. Cette avancée combine des vésicules de gaz et des mécanophores pour activer avec précision les médicaments, réduisant ainsi les dommages causés aux tissus sains. Crédit : Issues.fr.com
Le traitement innovant du cancer de Caltech utilise des médicaments activés par ultrasons pour une thérapie ciblée, réduisant les effets secondaires et améliorant l’efficacité.
La chimiothérapie comme traitement du cancer est l’une des plus grandes réussites médicales du 20e siècle, mais elle est loin d’être parfaite. Quiconque a subi une chimiothérapie ou a fait subir une chimiothérapie à un ami ou à un proche connaîtra ses nombreux effets secondaires : perte de cheveux, nausées, affaiblissement du système immunitaire, voire infertilité et lésions nerveuses.
C’est parce que les médicaments de chimiothérapie sont toxiques. Ils sont censés tuer les cellules cancéreuses en les empoisonnant, mais comme les cellules cancéreuses dérivent de cellules saines et leur sont sensiblement similaires, il est difficile de créer un médicament qui les tue sans également nuire aux tissus sains.
Percée dans l’administration ciblée de médicaments
Mais maintenant, deux équipes de recherche de Caltech ont créé un tout nouveau type de système d’administration de médicaments, qui, selon elles, pourrait enfin donner aux médecins la possibilité de traiter le cancer de manière plus ciblée. Le système utilise des médicaments activés par ultrasons et uniquement là où ils sont nécessaires dans le corps.
Le système a été développé dans les laboratoires de Maxwell Robb, professeur adjoint de chimie, et de Mikhail Shapiro, professeur Max Delbrück de génie chimique et de génie médical et chercheur au Howard Hughes Medical Institute. Dans un article publié dans la revue Actes de l’Académie nationale des sciences, les chercheurs montrent comment ils ont combiné des éléments de chacune de leurs spécialités pour créer la plateforme.
Travaillant en collaboration, les deux équipes de recherche ont associé des vésicules de gaz (capsules de protéines remplies d’air présentes dans certaines bactéries) et des mécanophores (molécules qui subissent une modification chimique lorsqu’elles sont soumises à une force physique). Le laboratoire de Shapiro a déjà utilisé des vésicules de gaz en conjonction avec des ultrasons pour imager des cellules individuelles et déplacer avec précision les cellules. Le laboratoire de Robb, pour sa part, a créé des mécanophores qui changent de couleur lorsqu’ils sont étirés, ce qui les rend utiles pour détecter les contraintes dans les structures, ainsi que d’autres mécanophores capables de libérer une molécule plus petite, notamment un médicament, en réponse à un stimulus mécanique. Pour ce nouveau travail, ils ont imaginé un moyen d’utiliser les ondes ultrasonores comme stimulus.
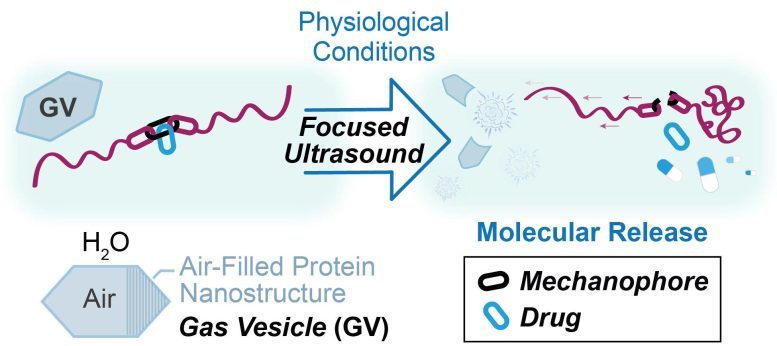
En présence d’ultrasons, les vésicules de gaz se rompent et, ce faisant, brisent des molécules appelées mécanophores qui libèrent une molécule plus petite et souhaitée. Crédit : Caltech
Mécanophores activés par ultrasons
« Nous y réfléchissons depuis très longtemps », explique Robb. « Cela a commencé lorsque je suis arrivé à Caltech et que Mikhail et moi avons commencé à avoir des conversations sur les effets mécaniques des ultrasons. »
Alors qu’ils commençaient à étudier la combinaison des mécanophores et des ultrasons, ils ont découvert un problème : les ultrasons pouvaient activer les mécanophores, mais seulement à une intensité si forte qu’ils endommageaient également les tissus voisins. Ce dont les chercheurs avaient besoin, c’était d’un moyen de concentrer l’énergie des ultrasons là où ils le souhaitaient. Il s’est avéré que la technologie des vésicules de gaz de Shapiro constituait la solution.

Les vésicules de gaz dans un flacon apparaissent blanches en solution et deviennent transparentes lorsqu’elles sont rompues par ultrasons. Crédit : Caltech
Dans ses travaux précédents, Shapiro utilisait la tendance des vésicules à vibrer ou à « sonner » comme une cloche lorsqu’elles sont bombardées d’ondes ultrasonores. Cependant, dans les recherches actuelles, les vésicules sonnent si fort qu’elles se brisent, ce qui concentre l’énergie ultrasonore. Les vésicules deviennent en effet de minuscules bombes dont les explosions activent le mécanophore.
« L’application d’une force par ultrasons repose généralement sur des conditions très intenses qui déclenchent l’implosion de minuscules bulles de gaz dissous », explique Molly McFadden (PhD ’23), co-auteur de l’étude. « Leur effondrement est la source d’une force mécanique qui active le mécanophore. Les vésicules ont une sensibilité accrue aux ultrasons. En les utilisant, nous avons découvert que la même activation mécanophore peut être obtenue sous des ultrasons beaucoup plus faibles.
Potentiel futur et implications
Yuxing Yao, chercheur postdoctoral associé au laboratoire de Shapiro, affirme que c’est la première fois que les ultrasons focalisés sont capables de contrôler une réaction chimique spécifique dans un contexte biologique.
«Auparavant, les ultrasons étaient utilisés pour perturber ou déplacer des objets», explique Yao. « Mais maintenant, cela nous ouvre cette nouvelle voie en utilisant la mécanochimie. »
Jusqu’à présent, la plateforme n’a été testée que dans des conditions contrôlées en laboratoire, mais les chercheurs prévoient de la tester sur des organismes vivants à l’avenir.
Les co-auteurs supplémentaires sont Stella M. Luo, étudiante diplômée en chimie, et Ross W. Barber (PhD ’23) ; Elin Kang (BS ’23); Avinoam Bar-Zion, anciennement de Caltech et maintenant du Technion-Israel Institute of Technology ; Cameron AB Smith, stagiaire postdoctoral en génie chimique ; Zhiyang Jin, étudiant diplômé en génie médical (MS ’18); Mark Legendre, étudiant diplômé en génie chimique; Bill Ling (PhD ’23), chercheur postdoctoral associé en génie chimique ; Dina Malounda de l’Institut médical Howard Hughes ; Andrea Torres et Tiba Hamza, étudiants de premier cycle à Caltech ; et Chelsea ER Edwards, anciennement de Caltech, maintenant à l’UC Santa Barbara.
Le financement de la recherche a été assuré par la Fondation Arnold et Mabel Beckman, la Fondation David et Lucile Packard, le Resnick Sustainability Institute, l’Institute for
Biotechnologies Collaboratives, et l’Institut National des Sciences Médicales Générales du Instituts nationaux de la santé.
Mikhail Shapiro est membre affilié du corps professoral de l’Institut de neurosciences Tianqiao et Chrissy Chen.