Des chercheurs de l’Université de Kumamoto ont étudié le processus de vieillissement cellulaire chez des rats-taupes nus (RMN), découvrant un mécanisme « sénolytique naturel » spécifique à la RMN qui élimine les cellules sénescentes, contribuant potentiellement à leur résistance au vieillissement. La recherche, utilisant des méthodes in vitro et in vivo, a identifié le rôle du métabolisme de la sérotonine et de l’enzyme MAO dans ce processus, offrant ainsi un aperçu des stratégies anti-âge et des traitements contre les maladies liées à l’âge.
Des chercheurs japonais ont découvert un mécanisme unique, spécifique à l’espèce, utilisé par les rats-taupes nus pour résister à la détérioration et aux maladies liées à l’âge.
Le rat-taupe nu (RMN), ou Glaber hétérocéphale, est un rongeur originaire d’Afrique de l’Est qui possède une espérance de vie remarquable de plus de 37 ans. Cela en fait les rongeurs qui vivent le plus longtemps. Leur remarquable résistance au vieillissement et à des maladies comme le cancer a suscité l’intérêt de la communauté scientifique, conduisant les chercheurs à espérer élucider les mécanismes contribuant à leur longévité.
Comprendre le vieillissement dans les RMN
Des études antérieures ont exploré le rôle de ADN mécanismes de réparation, stabilité des protéines et traduction précision (conversion précise de ARN aux protéines) à cet égard, mais les mécanismes/facteurs moléculaires à l’origine de leur résistance au vieillissement restent largement flous. De plus, la contribution de la sénescence cellulaire à leur résistance au vieillissement est mal comprise.
La sénescence cellulaire (vieillissement cellulaire) se caractérise par l’arrêt irréversible de la division cellulaire, qui progresse avec l’âge. Les cellules sénescentes sont moins sujettes à la mort cellulaire et s’accumulent dans les tissus à mesure qu’elles vieillissent, favorisant ainsi l’inflammation chronique et compromettant le fonctionnement de ces tissus. Bien que la sénescence cellulaire joue un rôle important dans le vieillissement, on sait peu de choses sur sa fonction dans les RMN.

Un rat-taupe nu élevé au laboratoire Miura de l’université de Kumamoto. Crédit : Yoshimi Kawamura et Kyoko Miura de l’Université de Kumamoto, Japon
Recherche sur la sénescence cellulaire en RMN
À cette fin, une équipe de chercheurs japonais dirigée par le professeur Kyoko Miura du Département de recherche sur le vieillissement et la longévité de l’Université de Kumamoto a mené une série d’expériences in vitro et in vivo pour comprendre comment la sénescence cellulaire se produit dans les RMN et s’il y en a. espèces-des mécanismes spécifiques qui contribuent à supprimer l’accumulation de cellules sénescentes et leur vieillissement retardé. Le Département de recherche sur le vieillissement et la longévité de l’Université de Kumamoto est le seul centre au Japon à produire des RMN et à mener des recherches sur leur résistance au vieillissement et au cancer.
Expliquant la justification de leur étude récemment publiée dans La revue EMBO, le professeur Miura déclare : « Il a été démontré que la sénolyse ou l’élimination ciblée des cellules sénescentes inhibe le déclin lié au vieillissement chez la souris. Cependant, la question de savoir si les résultats obtenus chez la souris sont généralisables reste ouverte. Dans cette étude, nous avons découvert un mécanisme « sénolytique naturel » spécifique à la RMN qui pourrait fournir une justification évolutive pour l’élimination des cellules sénescentes comme stratégie thérapeutique pour prévenir le vieillissement.
Résultats et méthodologie
L’équipe de recherche a utilisé de faibles concentrations de doxorubicine (DXR) – un agent endommageant l’ADN – pour induire in vitro la sénescence cellulaire dans les fibroblastes cutanés dérivés de la RMN et de la souris. Ils ont observé que l’induction de la sénescence cellulaire entraînait l’arrêt de la prolifération cellulaire en raison de l’arrêt du cycle cellulaire avec l’activation de INK4a et RB (facteurs importants pour l’induction de la sénescence cellulaire), à la fois dans les fibroblastes RMN et dans les fibroblastes de souris. Cependant, seules les cellules RMN ont activé progressivement et de manière significative la mort cellulaire, ce qui suggère que l’accumulation de cellules sénescentes dans les RMN pourrait être supprimée par leur élimination.
Grâce à d’autres expériences, les chercheurs ont observé une accumulation de sérotonine (un neurotransmetteur qui envoie des signaux entre les cellules nerveuses) dans les fibroblastes RMN non sénescents, mais pas dans les fibroblastes de souris. Lors de l’induction de la sénescence, dans les cellules RMN, la sérotonine a été métabolisée par la monoamine oxydase (MAO ; une enzyme hautement activée dans les fibroblastes RMN sénescents après l’induction de la sénescence cellulaire) et convertie en 5-hydroxyindole acétique. acide (5-HIAA ; un métabolite), libérant de grandes quantités de peroxyde d’hydrogène (H2O2).
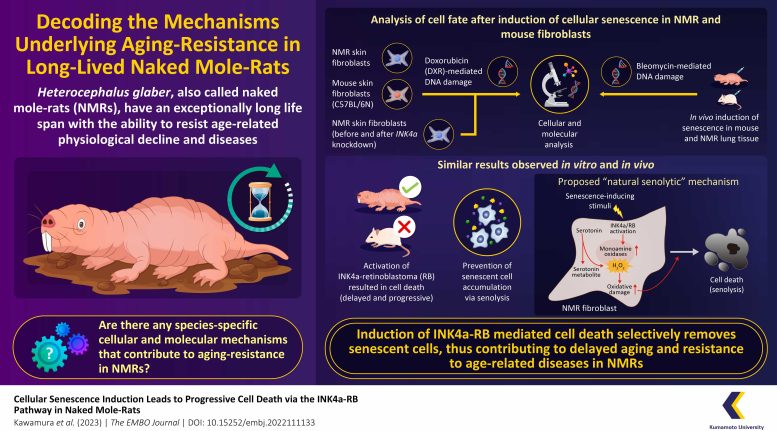
Une infographie illustrant un mécanisme unique d’élimination des cellules « sénolytiques naturelles » ou sénescentes naturelles identifié par des chercheurs japonais chez des rats-taupes nus, l’espèce de rongeur qui vit le plus longtemps. Ils ont proposé un mécanisme spécifique à l’espèce impliquant l’activation de la signalisation INK4a-RB et du métabolisme de la sérotonine, qui augmente les dommages oxydatifs intracellulaires et provoque la mort ultérieure des cellules RMN sénescentes. Crédit : Yoshimi Kawamura et Kyoko Miura de l’Université de Kumamoto, Japon
L’équipe a proposé que le stress oxydatif dû à la production intracellulaire de H2O2 prédispose les fibroblastes sénescents RMN à la voie de la mort cellulaire, conduisant ainsi à la sénolyse (élimination sélective des cellules sénescentes). Ceci a été confirmé par l’observation selon laquelle l’ajout d’inhibiteurs de la MAO et d’antioxydants inhibait la mort cellulaire dans les fibroblastes RMN.
Pour confirmer si un mécanisme similaire était également répandu in vivo, l’équipe a induit une sénescence cellulaire dans les poumons de souris et des RMN à l’aide de bléomycine (un agent endommageant l’ADN). Ils ont observé que la mort cellulaire, probablement due à une réponse aiguë à des dommages à l’ADN, augmentait initialement au deuxième jour dans les cellules pulmonaires de souris et RMN. Cependant, après une augmentation initiale au jour 2, une baisse de la mort cellulaire a été observée et au jour 21, la mort cellulaire avait de nouveau augmenté, uniquement dans les cellules pulmonaires RMN.
Orientations futures et conclusion
De plus, le traitement avec l’inhibiteur de la MAO a supprimé de manière significative la mort cellulaire mais a augmenté le nombre de cellules sénescentes uniquement dans le poumon RMN au jour 21. Cela suggère que la MAO joue un rôle dans l’induction de la mort cellulaire et la réduction du nombre de cellules sénescentes suite à l’induction de l’activité cellulaire. sénescence dans les cellules pulmonaires RMN. Ces résultats sont cohérents avec les résultats in vitro et suggèrent que la MAO contribue à supprimer l’accumulation de cellules sénescentes dans les tissus RMN.
« D’autres études axées sur le mécanisme d’élimination des cellules sénescentes dans les tissus RMN sont nécessaires pour comprendre quel type de cellules sénescentes doit être éliminé, quand et comment. De telles études pourraient contribuer au développement de médicaments sénolytiques plus sûrs et ciblés », déclare le professeur Miura en discutant des étapes futures.
Dans l’ensemble, ces résultats suggèrent que la mort cellulaire médiée par INK4a-RB pourrait faciliter l’élimination des cellules sénescentes dans les RMN, les aidant ainsi à résister à la dégénérescence liée au vieillissement. Nous sommes convaincus qu’en mettant en évidence un mécanisme sénolytique naturel chez cette espèce à longue durée de vie, cette étude contribuerait au développement de stratégies anti-âge et de thérapies ciblées contre les maladies liées à l’âge comme le cancer.
L’étude a été financée par l’Agence japonaise pour la science et la technologie, l’Agence japonaise pour la recherche et le développement médical, la Société japonaise pour la promotion de la science, la Fondation scientifique Takeda, la Fondation Mitsubishi, la Fondation Kanzawa pour la recherche médicale et la Fondation japonaise pour le vieillissement. et santé, la KOSE Cosmetology Research Foundation, le Princess Takamatsu Cancer Research Fund, la Fondation Nakatomi, la Fondation Naito, la Fondation pour la promotion de la recherche sur le cancer, la Kato Memorial Bioscience Foundation, la MSD Life Science Foundation, la Fondation Inamori, le SGH Foundation, la Fondation Terumo pour les sciences de la vie et les arts, la Fondation Ichiro Kanehara pour la promotion des sciences médicales et des soins médicaux et la Fondation Frontier Salon.




