Des chercheurs de l'Institut néerlandais du cancer ont découvert un nouveau mécanisme de mort des cellules cancéreuses impliquant le gène Schlafen11, qui pourrait révolutionner la compréhension et le traitement du cancer. Ce gène aide à arrêter la production de protéines en réponse aux dommages à l'ADN, offrant ainsi une nouvelle cible pour les thérapies contre le cancer, en particulier dans les cas où les voies traditionnelles de la protéine p53 sont inefficaces. Crédit : Issues.fr.com
Les scientifiques ont découvert que la façon dont les cellules cancéreuses meurent suite à la chimiothérapie semble être différente de ce que l’on pensait auparavant. Une nouvelle recherche met en évidence le rôle du gène Schlafen11 dans la mort des cellules cancéreuses, offrant ainsi une nouvelle approche des stratégies de chimiothérapie et de traitement du cancer.
La chimiothérapie tue les cellules cancéreuses. Mais la façon dont ces cellules meurent semble être différente de ce que l’on pensait auparavant. Des chercheurs de l'Institut néerlandais du cancer, dirigés par Thijn Brummelkamp, ont découvert une toute nouvelle façon de mourir des cellules cancéreuses : à cause du gène Schlafen11. « C’est une découverte très inattendue. Les patients atteints de cancer sont traités par chimiothérapie depuis près d’un siècle, mais cette voie menant à la mort cellulaire n’a jamais été observée auparavant. Il faudra étudier plus en détail où et quand cela se produit chez les patients. Cette découverte pourrait à terme avoir des implications pour le traitement des patients atteints de cancer. Ils ont publié leurs conclusions dans la revue Science.
Le rôle des dommages à l'ADN dans le traitement du cancer
De nombreux traitements contre le cancer endommagent les cellules ADN. Après trop de dommages irréparables, les cellules peuvent provoquer leur propre mort. La biologie au lycée nous apprend que la protéine p53 prend en charge ce processus. p53 assure la réparation de l'ADN endommagé, mais déclenche le suicide cellulaire lorsque les dommages deviennent trop graves. Cela empêche la division cellulaire incontrôlée et la formation de cancer.
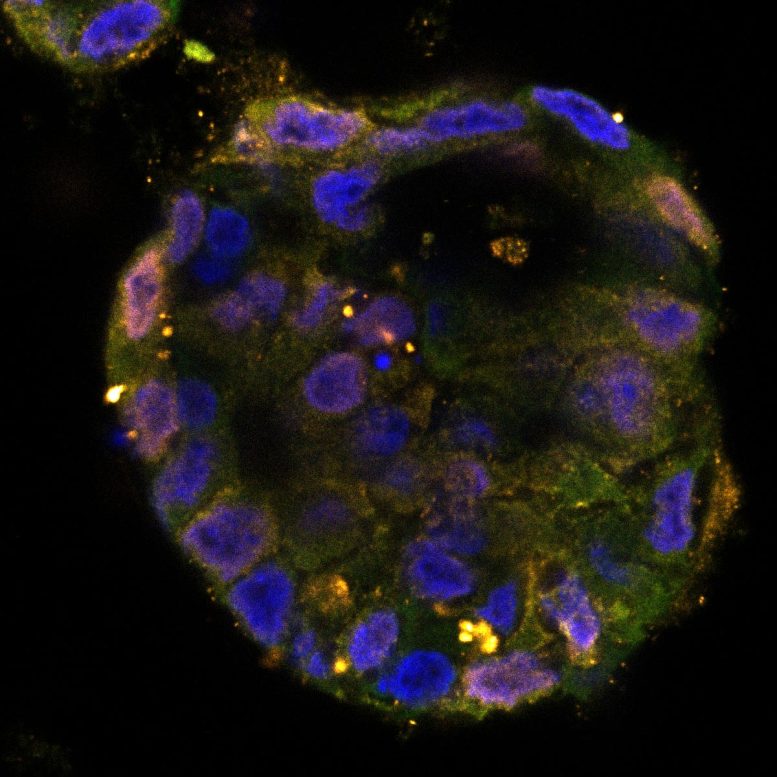
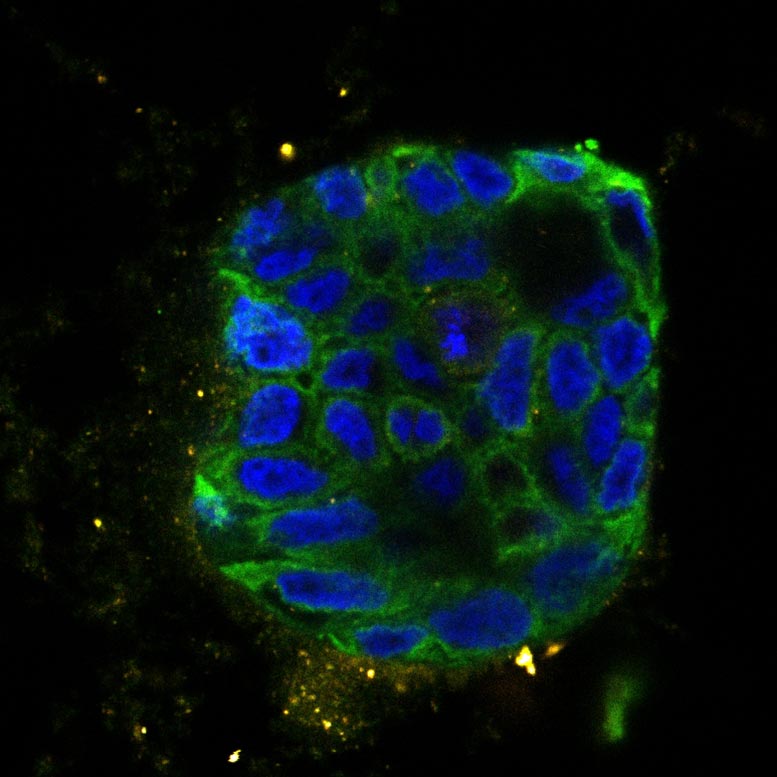
Organoïde d'un patient atteint d'un cancer du côlon, traité (en bas) et non traité par l'étoposide de chimiothérapie. Le traitement provoque des dommages à l'ADN et une réduction de la synthèse des protéines. Cela déclenche un signal de stress qui provoque la mort des cellules. Orange : marqueur des dommages à l'ADN. Vert : marqueur de la synthèse des protéines. Crédit : Institut néerlandais du cancer
Surprise : question sans réponse
Cela semble être un système infaillible, mais la réalité est plus complexe. « Dans plus de la moitié des tumeurs, p53 ne fonctionne plus », explique Thijn Brummelkamp. « L’acteur clé p53 n’y joue aucun rôle. Alors pourquoi les cellules cancéreuses sans p53 meurent-elles quand vous endommagez leur ADN par chimiothérapie ou radiothérapie ? À ma grande surprise, cette question s’est avérée être sans réponse.
Son groupe de recherche a ensuite découvert, avec le groupe de son collègue Reuven Agami, une manière jusqu'alors inconnue par laquelle les cellules meurent après des dommages à l'ADN. En laboratoire, ils ont administré une chimiothérapie à des cellules dont ils ont soigneusement modifié l’ADN. Thijn : « Nous recherchions un changement génétique qui permettrait aux cellules de survivre à la chimiothérapie. Notre groupe possède une grande expérience dans la désactivation sélective des gènes, que nous pourrions parfaitement appliquer ici.
Désactiver les gènes, un par un
Les humains possèdent des milliers de gènes, dont beaucoup ont des fonctions qui ne nous sont pas claires. Pour déterminer les rôles de nos gènes, le chercheur Thijn Brummelkamp a développé une méthode utilisant des cellules haploïdes. Ces cellules ne contiennent qu’une seule copie de chaque gène, contrairement aux cellules normales de notre corps qui en contiennent deux copies. La manipulation de deux copies peut s'avérer difficile dans les expériences génétiques, car des changements (mutations) se produisent souvent dans une seule d'entre elles. Cela rend difficile l’observation des effets de ces mutations.
En collaboration avec d’autres chercheurs, Brummelkamp découvre depuis des années des processus cruciaux dans la maladie grâce à cette méthode polyvalente. Par exemple, son groupe a récemment découvert que les cellules peuvent produire des lipides d’une manière différente de celle connue auparavant. Ils ont découvert comment certains virus, notamment le virus mortel Ebola, virus, parviennent à pénétrer dans les cellules humaines. Ils se sont penchés sur la résistance des cellules cancéreuses à des thérapies spécifiques et ont identifié des protéines qui agissent comme des freins sur le système immunitaire, ce qui est pertinent pour l'immunothérapie du cancer. Au cours des dernières années, son équipe a découvert deux enzymes restées insaisissables pendant quatre décennies et qui se sont révélées vitales pour la fonction musculaire et le développement du cerveau.
Nouvel acteur clé dans la mort cellulaire
En désactivant les gènes, le groupe de recherche a découvert une nouvelle voie menant à la mort cellulaire, dirigée par le gène Schlafen11 (SLFN11). Nicolaas Boon, chercheur principal : « En cas de dommages à l'ADN, SLFN11 arrête les usines de protéines des cellules : les ribosomes. Cela provoque un immense stress dans ces cellules, ce qui conduit à leur mort. La nouvelle route que nous avons découverte contourne complètement la p53.
Le gène SLFN11 n’est pas étranger à la recherche sur le cancer. Il est souvent inactif dans les tumeurs des patients qui ne répondent pas à la chimiothérapie, explique Thijn. « Nous pouvons désormais expliquer ce lien. Lorsque les cellules manquent de SLFN11, elles ne mourront pas de cette manière en réponse à des dommages à l'ADN. Les cellules survivront et le cancer persistera.
Impact sur le traitement du cancer
«Cette découverte soulève de nombreuses nouvelles questions de recherche, ce qui est généralement le cas en recherche fondamentale», explique Thijn. « Nous avons démontré notre découverte dans des cellules cancéreuses cultivées en laboratoire, mais de nombreuses questions importantes demeurent : où et quand cette voie se produit-elle chez les patients ? Comment cela affecte-t-il l’immunothérapie ou la chimiothérapie ? Cela affecte-t-il les effets secondaires du traitement du cancer ? Si cette forme de mort cellulaire s’avère également jouer un rôle important chez les patients, cette découverte aura des implications pour les traitements contre le cancer. Ce sont des questions importantes à approfondir.
Cette recherche a été financée par la KWF Dutch Cancer Society, l’Oncode Institute et Health Holland.