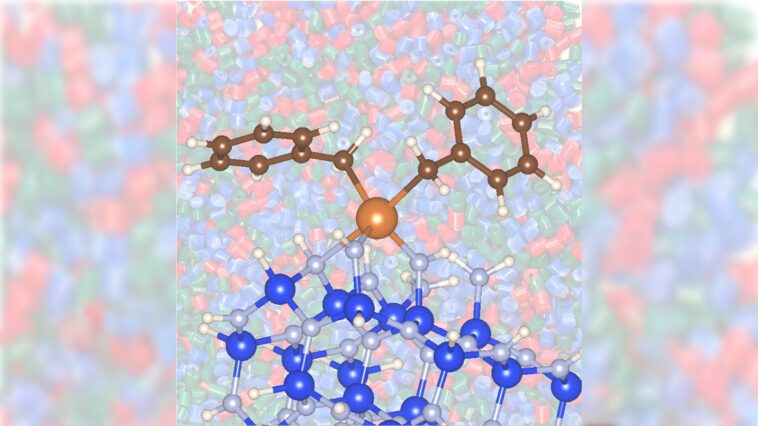
Le zirconium (atome orange brûlé plus gros), combiné au nitrure de silicium (atomes bleus et gris), améliore la transformation du propane en propylène d'une manière plus rapide et moins énergivore que les moyens plus traditionnels. Crédit : David Kaphan, Max Delferro et Yu Lim Kim/Argonne National Laboratory
L’association du zirconium et du nitrure de silicium améliore la transformation du propane, un composant du gaz naturel, en polypropylène, un plastique très recherché.
Le polypropylène est un plastique largement utilisé dans de nombreux objets du quotidien, notamment les récipients alimentaires et les appareils médicaux. En raison de sa popularité, la demande de propylène, un produit chimique essentiel à sa production, est en hausse. Le propylène est dérivé du propane, un gaz naturel couramment utilisé dans les barbecues.
Des scientifiques du laboratoire national d'Argonne et du laboratoire national d'Ames du département américain de l'énergie (DOE) signalent une méthode plus rapide et plus économe en énergie pour fabriquer du propylène que le procédé actuellement utilisé.
La conversion du propane en propylène nécessite généralement un catalyseur métallique comme le chrome ou le platine sur un matériau de support, comme l'oxyde d'aluminium ou le dioxyde de silicium. Le catalyseur accélère la réaction. Cependant, il nécessite également des températures de fonctionnement et une consommation d'énergie élevées.
Une percée dans la technologie des catalyseurs
Dans le cadre d'un projet collaboratif, des scientifiques d'Argonne et d'Ames ont découvert que le zirconium combiné au nitrure de silicium améliore la conversion catalytique du gaz propane en propylène. Il le fait d'une manière plus rapide et moins toxique et consomme moins d'énergie que d'autres métaux non précieux, comme le chrome. Il est également moins coûteux que les catalyseurs à base de métaux précieux comme le platine.
Cette découverte révèle également un moyen de réduire la température du processus catalytique, ce qui réduit à son tour la quantité de dioxyde de carbone libérée. Le dioxyde de carbone est responsable de près de 80 % des émissions de gaz à effet de serre aux États-Unis. De plus, cette recherche donne un aperçu de la réactivité réalisable avec d’autres métaux à faible coût dans la conversion catalytique du propane en propylène.
Depuis un certain temps, les chimistes d'Argonne David Kaphan et Max Delferro étudient systématiquement la manière dont les surfaces non traditionnelles influencent et favorisent la catalyse. En tant que chercheurs principaux de cette étude, ils voulaient comprendre comment un catalyseur métallique non traditionnel sur un type de support non traditionnel se compare aux matériaux traditionnellement utilisés lors de la conversion catalytique du propane.
Les matériaux de support des catalyseurs ont généralement une surface spécifique élevée et aident à répartir les catalyseurs. Ils peuvent également jouer un rôle important dans la promotion de la catalyse, comme le montre cette étude. L'équipe de recherche a découvert qu'un catalyseur au zirconium sur un support en nitrure de silicium produisait une catalyse nettement plus active pour la conversion du propane en propylène. À l'inverse, ce n'était pas le cas avec le support en silice.
Ils ont également découvert que le support en nitrure de silicium permettait une catalyse plus rapide et plus efficace sur le plan énergétique qu'avec les métaux traditionnels sur silice. En tant que support de catalyseur, le nitrure de silicium peut améliorer les réactions chimiques à la surface des métaux par rapport aux oxydes plus traditionnellement utilisés. Les scientifiques ont réussi la conversion catalytique du propane à une température de 842 degrés F. C'est légèrement inférieur aux 1 022 degrés F généralement requis pour la catalyse utilisant des matériaux traditionnels.
Implications générales et outils de recherche
De plus, lorsqu'ils sont utilisés à la même température que les catalyseurs traditionnels pour cette transformation, les taux de réaction sont significativement plus rapides que ceux de matériaux similaires avec des supports en oxyde. Cette découverte apporte également la preuve que ce concept peut être généralisé à d'autres réactions importantes.
« Cela ouvre une fenêtre sur la réactivité des métaux supportés par les nitrures. Nous voyons des promesses dans l’utilisation d’autres métaux de transition où nous pouvons exploiter cette différence dans l’environnement local de la surface des nitrures pour améliorer la catalyse », a déclaré Kaphan.
Cette recherche a bénéficié de l'Advanced Photon Source (APS) d'Argonne, une installation utilisateur du DOE Office of Science. Sur la ligne de faisceau 10-BM, les chercheurs ont utilisé la spectroscopie d'absorption des rayons X pour comprendre en quoi l'interaction du catalyseur au zirconium avec le matériau nitrure diffère de celle du matériau oxyde.
Les chercheurs d'Argonne ont également collaboré avec Frédéric Perras, scientifique au laboratoire national Ames, pour mieux comprendre la structure du catalyseur zirconium/nitrure de silicium. Il a utilisé une technique de résonance magnétique nucléaire améliorée par polarisation nucléaire dynamique pour analyser la façon dont le nitrure de silicium réagit avec les sites métalliques.
« La composition de la surface du nitrure de silicium est largement inconnue, et c’est ce que j’ai trouvé le plus passionnant dans ce travail », a déclaré Perras, qui est également professeur associé adjoint à l’Université d’État de l’Iowa.
Selon Delferro, la combinaison des techniques de caractérisation des matériaux disponibles à Argonne et à Ames et l'expertise des personnes qui ont travaillé sur cet article sont ce qui a contribué au succès de cette expérience.
« Une seule personne ne peut pas tout faire. Il s’agit vraiment d’un travail d’équipe, et chacun a apporté son expertise pour atteindre cet objectif », a-t-il déclaré.
Le soutien à la recherche est venu du Bureau des sciences énergétiques fondamentales du DOE, Division des sciences chimiques, des géosciences et des biosciences, programme de sciences de la catalyse.