Les produits naturels issus de micro-organismes constituent une source prometteuse de nouveaux principes actifs, mais ne sont souvent produits qu’en très petites quantités. Une équipe de recherche de l'Institut Helmholtz de recherche pharmaceutique de la Sarre (HIPS) dirigée par Tobias Gulder a réussi à établir une plateforme chimio-enzymatique pour la production de furanolides, une classe de produits naturels à large spectre d'activité.
Cette stratégie permet non seulement de produire des furanolides de manière rentable, mais également d’apporter des modifications structurelles. Les molécules nouvellement générées sont capables de lutter efficacement contre les bactéries pathogènes et les cellules cancéreuses. L'équipe a maintenant publié ses conclusions dans le Journal de l'American Chemical Society.
Les furanolides constituent une classe de produits naturels présentant une grande diversité structurelle et un large spectre d’activités biologiques. Si certains membres de ce groupe sont très efficaces contre les bactéries, d’autres sont capables de tuer les algues ou même les cellules humaines. Les furanolides offrent ainsi une base prometteuse pour le développement de nouveaux médicaments.
Outre les cyanobactéries et les myxobactéries, les sources naturelles de furanolides comprennent certains animaux marins tels que les ascidies. Leur point commun est qu’ils ne produisent des furanolides qu’en très petites quantités, ce qui les rend difficiles à étudier en détail en termes de structure et d’activité.
Grâce à une plateforme chimio-enzymatique nouvellement développée, une équipe de recherche dirigée par les chefs du département HIPS, Gulder et Rolf Müller, a réussi à produire un grand nombre de furanolides différents en plus grandes quantités et à caractériser leur activité biologique. HIPS est un site du Centre Helmholtz pour la recherche sur les infections (HZI) en collaboration avec l'Université de la Sarre.
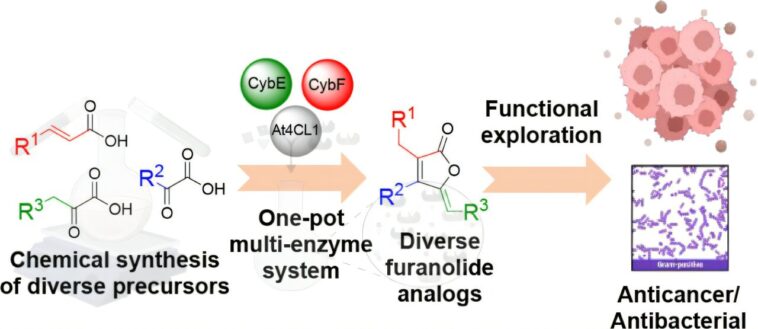
Outre la production de furanolides par des micro-organismes, il est également possible de les produire entièrement par synthèse chimique. Cependant, les voies de synthèse connues à ce jour souffrent de faibles rendements et sont très coûteuses. Pour contourner ces problèmes, Gulder et Müller ont développé une approche qui utilise des enzymes individuelles issues de la biosynthèse du furanolide pour assembler les produits naturels dans un tube à essai.
Les connaissances sur les enzymes concernées proviennent d'une étude menée par l'équipe de Gulder en 2022, dans laquelle les chercheurs ont découvert avec succès la biosynthèse de la précyanobactérine, un membre de la famille des furanolides.
La stratégie nouvellement développée utilise les deux enzymes CybE et CybF découvertes précédemment pour assembler le squelette du furanolide à partir d’une série de molécules précurseurs simples. Afin de pouvoir produire des représentants de furanolides jusqu'alors inconnus en plus de la précyanobactérine, l'équipe a compilé une série de molécules précurseurs modifiées et testé si celles-ci pouvaient également être converties par CybE et CybF.
« Nous avons pu identifier des dizaines de molécules précurseurs différentes qui peuvent être converties de manière assez efficace par notre système CybE/F. En combinant ces substrats de différentes manières, nous avons pu générer une bibliothèque de substances avec un total de 385 dérivés de furanolides, pour la plupart nouveaux », explique Gulder, chef du département Biotechnologie des produits naturels.
« Par la suite, en optimisant l'approvisionnement en substances précurseurs, nous avons pu réduire considérablement les coûts de production du furanolide dans notre système. Cela nous a permis de produire des dérivés individuels dans les quantités nécessaires pour tester leurs propriétés biologiques. »
Sur la base des propriétés structurelles des nouveaux furanolides, l’équipe a sélectionné 17 des 385 dérivés possibles pour caractériser plus en détail leur activité biologique contre les agents pathogènes bactériens et les cellules cancéreuses. Jennifer Herrmann, scientifique principale du département Müller, déclare : « Tous les furanolides testés étaient capables de tuer les cellules cancéreuses humaines en laboratoire, certains d'entre eux encore plus efficacement que les médicaments déjà utilisés en clinique. Nous avons observé que nos substances pouvaient même éliminer efficacement les cellules souches cancéreuses.
« De plus, certains dérivés du furanolide sont capables d'inhiber la croissance de plusieurs agents pathogènes à Gram positif tels que Staphylococcus aureus. Cette classe de substances offre ainsi de nombreuses possibilités de développement futur. »
L’équipe utilise actuellement les connaissances acquises sur les relations entre la structure et l’activité des furanolides pour optimiser davantage les dérivés sélectionnés. À long terme, l’objectif est de déterminer si la classe de substances est adaptée au développement de substances actives destinées au traitement de maladies infectieuses ou du cancer.