Les scientifiques notent depuis longtemps avec intérêt que dans l’une des réactions chimiques cruciales de la nature – la réaction de dégagement d’oxygène – c’est le manganèse, plutôt que des éléments similaires plus abondants tels que le fer, qui agit comme catalyseur clé.
Maintenant, dans une recherche publiée dans Durabilité de la natureun groupe de recherche dirigé par Ryuhei Nakamura du RIKEN Center for Sustainable Resource Science (CSRS) au Japon a découvert que le manganèse a une capacité unique à agir même en cas de fluctuations de tension électrique, et que cette capacité est essentielle à son succès en tant que catalyseur.
Cela signifie également qu'artificiellement, le manganèse est un bon candidat pour des applications, comme dans l'énergie éolienne et solaire, dans lesquelles la production électrique fluctue.
La réaction de dégagement d'oxygène, qui utilise de l'énergie pour libérer des protons et des électrons de composés tels que l'eau, libérant ainsi de l'oxygène, est essentielle à la vie sur Terre car elle fonctionne au cœur de la photosynthèse. C’est l’oxygène libre produit lors de cette réaction qui nous permet, ainsi qu’à d’autres formes de vie, d’obtenir de l’énergie en respirant.
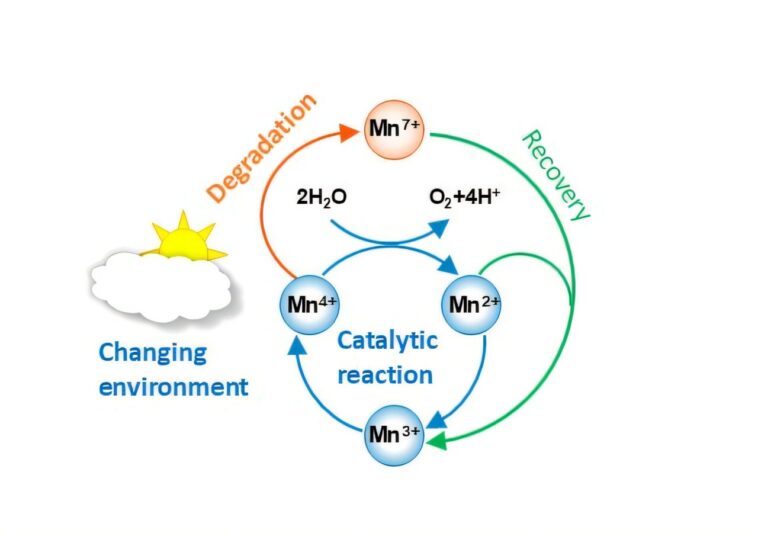
Le manganèse agit comme le principal catalyseur de cette réaction, sous la forme d’un amas de manganèse semblable à un oxyde, qui peut exister dans divers états d’oxydation. Lorsque l’énergie solaire ou électrique fluctue, l’état d’oxydation du manganèse change, ce qui lui permet de piloter la réaction de manière répétée.
La nature cyclique de ce processus est une caractéristique clé pour des réactions durables, car elle permet d’utiliser les catalyseurs à plusieurs reprises. Pour un catalyseur idéal, ce processus serait répété indéfiniment.
Cependant, les véritables catalyseurs se désactivent avec le temps, par exemple en raison de la dissolution d'ions métalliques tels que le manganèse. Normalement, il s’agit d’un chemin à sens unique et les ions perdus ne retournent pas au catalyseur.
Cependant, pour la présente étude, les chercheurs ont incorporé la réaction de Guyard, dans laquelle un ion manganèse avec un état d'oxydation de 7 est converti en un ion avec un état de 3. Les chercheurs ont découvert que même si le catalyseur se décompose comme prévu lorsque la tension devient trop élevée, avec l'incorporation de la réaction de Guyard, il est régénéré lorsque l'excès de tension est supprimé.
Plus précisément, lorsque les chercheurs ont commuté la tension à plusieurs reprises entre 1,68 volts et 3,00 volts, le catalyseur a pu maintenir un courant de 250 milliampères par centimètre carré à un pH de 2 pendant plus de 2 000 heures, soulignant l'importance de la conception de voies de conversion d'énergie durable à partir de sources renouvelables intermittentes.
Cette régénération est unique au manganèse, car les éléments chimiques similaires du « bloc 3D », tels que le cobalt, le fer et le nickel, ne peuvent pas se régénérer dans les mêmes conditions expérimentales. Les auteurs pensent que c’est un facteur majeur expliquant pourquoi le manganèse est devenu le catalyseur clé de la photosynthèse.
En termes d'impact, selon Nakamura, « Nous avons montré qu'il est possible de développer des matériaux résistants aux fluctuations de tension, avec le potentiel de développer à terme des matériaux pouvant être utilisés dans les électrolyseurs d'eau – des appareils qui convertissent l'eau en oxygène et en hydrogène – connectés directement à des sources d'énergie renouvelables ».
En effet, les sources d’énergie renouvelables, telles que l’énergie solaire et éolienne, fluctuent sur des échelles de temps allant de quelques secondes à quelques heures.
Pour aller de l'avant, Nakamura déclare : « Il s'agit d'un travail important, mais pour créer des applications industrielles, nous devrions être en mesure de prolonger la durée de vie d'au moins un ordre de grandeur. Nous abordons ce problème maintenant. »