Des chercheurs de l'Université de l'Illinois Urbana-Champaign ont découvert de nouveaux indices importants dans le mystère de la façon dont une enzyme ancienne peut transformer le carbone atmosphérique en biomolécules, un processus naturel qui pourrait être utile pour développer de nouvelles méthodes pour convertir les gaz à effet de serre comme le dioxyde de carbone en produits chimiques utiles.
Comme la déforestation et l'utilisation de combustibles fossiles provoquent des gaz atmosphériques, comme le dioxyde de carbone (CO2), pour atteindre des niveaux sans précédent, de nombreux scientifiques se sont tournés vers la biologie ancienne à la recherche de solutions pour lutter contre le déséquilibre de ces gaz dans l'atmosphère. Dès le début de la vie sur terre, les organismes microscopiques ont trouvé des moyens de convertir le dioxyde de carbone atmosphérique (CO2) et le monoxyde de carbone (CO) dans des biomolécules utiles.
Ces organismes utilisent des catalyseurs biologiques spécialisés, ou enzymes, pour « réparer » ces gaz dans des blocs de construction moléculaires. Les scientifiques ont été particulièrement intéressés à comprendre comment une enzyme ancienne spéciale Ni – Acétyl-CoA synthase (ACS) – se porte dans le dioxyde de carbone et le monoxyde de carbone et les convertit en acétyl-CoA, qui est une biomolécule clé qui métabolise les sucres, les lipides et les protéines à l'intérieur des cellules.
Cela se produit dans un processus appelé Wood-Ljungdahl Pathway (WLP), et ACS catalyse la dernière étape de cet ensemble de réactions biochimiques. Mais exactement le fonctionnement de cette enzyme reste un mystère pour les scientifiques malgré des décennies d'étude de l'enzyme.
Il y a eu des hypothèses contradictoires proposées concernant certains aspects fondamentaux du mécanisme enzymatique. Chaque étape de la réaction chimique se produit rapidement, et les espèces intermédiaires de la voie de réaction sont si de courte durée, sensibles à l'oxygène et instables que caractérisant chaque étape et la compréhension de l'ensemble du mécanisme reste énigmatique.
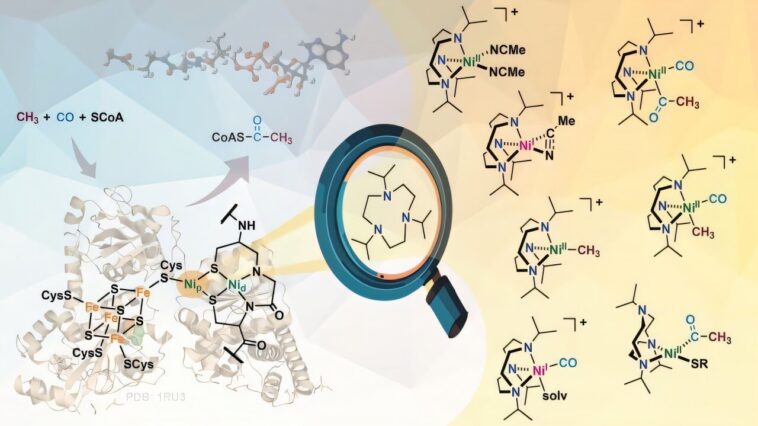
Dans une étude dirigée par le professeur de chimie de l'Illinois Liviu Mirica et l'étudiant diplômé Shounak Nath, les chercheurs ont créé un modèle fonctionnel synthétique qui imite ACS et permet une exploration approfondie du mécanisme de l'énergie, un exploit inapproprié par tous les modèles synthétiques antérieurs, selon les chercheurs. Leur enquête a dévoilé quatre informations mécanistes clés – a été comptabilisée dans leur article récemment publié dans Communications de la nature– qui sont directement pertinents pour le mécanisme de l'ACS.
Ils ont étudié en détail la plupart des intermédiaires organométalliques, y compris un intermédiaire de nickel très rare, Ni (méthyl) (CO).
Mirica et Nath ont expliqué qu'une clé du succès de leur modèle synthétique est un ligand spécial appelé jeRP3TACN (1,4,7-triisopropyl-1,4,7-triazacyclononane) qui forme une cage autour de l'atome de nickel et ralentit la vitesse de réaction juste assez pour que les intermédiaires labiles puissent être observés directement. Il permet également à certaines réactions de se produire dans des directions avant et arrière, ce qui a permis aux chercheurs de caractériser les paramètres cinétiques et thermodynamiques associés aux transformations moléculaires.
Les chercheurs ont déclaré que le tridentate volumineux jeRP3Le ligand TACN a le bon équilibre stérique et électronique pour permettre un site de liaison approprié pour les substrats et permet en même temps la stabilisation des intermédiaires Ni à haute valeur et à faible valeur. Cela permet à ce système d'accéder à toutes les étapes proposées du mécanisme enzymatique – quelque chose qui n'a pas été réalisé dans d'autres modèles synthétiques à petite molécule. Surtout, d'autres modèles n'ont pas réussi à observer les espèces intermédiaires Ni (méthyl) (CO) clés (CO) que Nath et Mirica ont identifiées.
Selon les chercheurs, ce travail peut être la clé des scientifiques concevant des catalyseurs nouveaux et améliorés pour séquestrer le dioxyde de carbone et les gaz de monoxyde de carbone hors de l'air en molécules utiles. En ayant une compréhension complète des étapes et des intermédiaires d'ACS, Mirica a déclaré que les scientifiques peuvent concevoir des catalyseurs synthétiques qui effectuent les mêmes transformations que ACS à l'aide de nickel, qui est un métal abondant de la Terre.
Nath a mené cette étude au cours de trois ans et a présenté leur travail au 6e Symposium sur la chimie inorganique biologique avancée (SABIC-2024) à Kolkata, en Inde. Nath a déclaré qu'il avait reçu des commentaires positifs de biochimistes qui recherchaient depuis des décennies des réponses au mécanisme de l'ACS.
Nath a déclaré qu'il y avait beaucoup de gens de la communauté bioinorganique lors de la session d'affiches, notamment Steve Ragsdale, l'un des scientifiques qui a lancé l'étude de cette enzyme.
« Je lui ai présenté ce travail et il était très excité à ce sujet », a déclaré Nath. « Il était enthousiasmé par le fait que nous pouvions réellement voir l'intermédiaire Ni (méthyl) (CO) qu'il a suivi depuis très longtemps dans l'enzyme indigène. »
Mirica a déclaré que cette recherche a également un impact car les étapes catalytiques de la catalyse ACS naturelle qui sont modélisées dans leur système synthétique sont fondamentalement les mêmes que les étapes de la production industrielle de produits chimiques comme le processus d'acide acétique de Monsanto. Le catalyseur de ce processus industriel est le rhodium, un métal précieux rare et coûteux, et Mirica espère que ce travail peut servir d'inspiration pour les conceptions de nouveaux catalyseurs industriels basés sur des catalyseurs de nickel plus économiques.
« Il y a un grand intérêt pour l'industrie chimique pour développer des processus catalytiques utilisant des catalyseurs de métaux de transition plus abondants et moins chers. Par exemple, il y a une pression pour potentiellement développer une transformation de type acide acétique à base de nickel », a déclaré Mirica.
« Il s'agit d'une enzyme très intéressante d'un point de vue organométallique fondamental, qui est quelque peu surprenant que nous parlions de la chimie organométallique dans le contexte d'un système biologique. Si vous regardez les étapes fondamentales de la réaction catalysée par cette enzyme, a déclaré en fait des étapes classiques impliquées dans les transformations organométalliques mimiques.
Le modèle ACS synthétique que les chercheurs ont conçu est simple contenant un seul atome de nickel qui imite le centre de nickel proximal (np) du site actif où les substrats se lient. Avoir ce centre de nickel monométallique à 3 coordonnées avec toutes les étapes caractérisées permet une étude plus approfondie où les scientifiques peuvent spéculer sur l'importance de l'atome de nickel distal (Nd) et d'autres atomes métalliques près du site actif du mécanisme ACS naturel.
Nath a déclaré que le plus grand défi était de travailler avec des composés aussi sensibles et d'apprendre à travailler avec le monoxyde de carbone en toute sécurité.
« Beaucoup de ces intermédiaires sont très sensibles à l'air et chacun d'eux a des fenêtres de stabilité thermique très différentes. Donc, en déterminant exactement les bonnes conditions dans lesquelles chaque intermédiaire est suffisamment stable pour une caractérisation complète et en même temps compétent pour réagir était la partie la plus difficile et la plus intrigante », a déclaré Nath.