Pensez à un métal avec de la peinture dessus, comme une automobile ou un pipeline transportant du gaz naturel. Le revêtement de peinture ou de polymère protège le métal en dessous de la dégradation.
Bien que le revêtement devrait idéalement protéger le métal pendant longtemps, une égratignure ou un défaut dans le revêtement peut entraîner un début précoce de la dégradation du métal. Cela se produit par un mécanisme bien établi connu sous le nom de radiographie cathodique, où la diffusion rapide de l'oxygène et de l'eau de l'atmosphère ambiante permet à la réaction de réduction de l'oxygène (ORR) d'accélérer la dégradation du revêtement par vertu des radicaux libres générés.
La signification cruciale est le taux de cet ORR car il détermine la durée de vie du métal en dessous. La mesure de ce taux de corrosion d'un métal peint est difficile car l'interface entre le revêtement et le métal est enterrée ou inaccessible.
Les techniques conventionnelles pour mesurer ce taux, comme la polarisation potentiodynamique, comptent sur la polarisation de cette interface en utilisant une électrode auxiliaire, c'est-à-dire une contre-électrode. L'idée derrière cette approche est de permettre à un courant ionique de s'écouler dans l'électrolyte entre le métal enduit et la contre-électrode afin qu'un courant électronique puisse être mesuré dans le circuit externe.
Connaître ce courant peut donner le taux de dégradation du métal revêtu. Mais voici le défi – un revêtement organique étant ioniquement imperméable ne permet pas à la polarisation du métal enduit.
Tout le courant est encore mesuré par cette technique n'est que le résultat de trous d'épingle, qui sont des pores ou des défauts introduits pendant le processus d'application de revêtement, et non le véritable taux de corrosion. Par conséquent, de nouvelles techniques électrochimiques sont nécessaires pour quantifier le taux de dégradation de ces métaux revêtus.
Récemment, nous avons introduit une nouvelle approche utilisant la potentiométrie basée sur la perméation par l'hydrogène (HPP) et la spectroscopie d'impédance électrochimique (EIS) pour mesurer ce taux. La recherche est publiée dans la revue Science de la corrosion.
Premièrement, le principe derrière HPP est d'utiliser la nature réductive électrochimique de l'hydrogène atomique comme moyen de polariser l'interface métallique enrobée de l'arrière d'une cellule électrochimique double. En règle générale, l'hydrogène atomique agit de la même manière que l'électrode auxiliaire dans la polarisation conventionnelle, c'est-à-dire qu'il polarise le métal revêtu, mais sans limitation de besoin de transport d'ions.
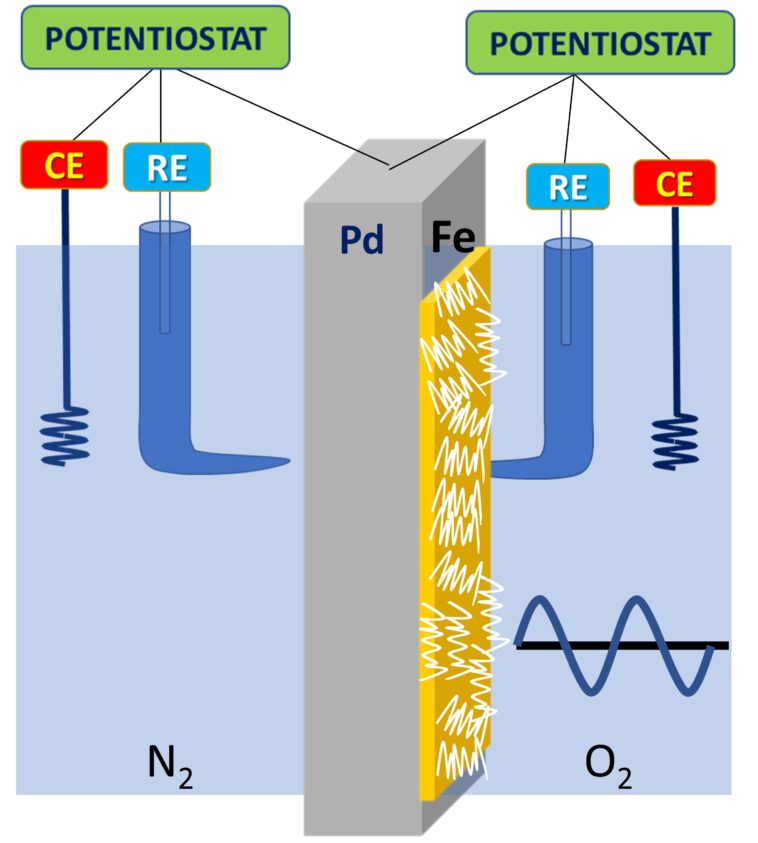
Par conséquent, nous avons d'abord généré des quantités définies d'hydrogène d'un côté de la double cellule électrochimique à l'aide d'une membrane de palladium électrocatalytique (PD) modèle. Cet hydrogène imprègne à travers la membrane PD et atteint l'autre cellule, où il réagit avec l'oxygène déjà présent et établit un potentiel d'équilibre électrochimique.
Nous avons ensuite augmenté la quantité d'hydrogène générée dans une cellule d'une manière passable, ce qui a entraîné une réduction de plus d'hydrogène et, en conséquence, de plus d'oxygène à être réduite dans l'autre cellule, ce qui s'est reflété comme une diminution du potentiel électrochimique.
En sachant combien d'hydrogène a été généré dans une cellule et en prouvant que presque tout cet hydrogène pouvait être fait quantitativement pour réagir avec l'oxygène dans l'autre cellule, le taux d'ORR pourrait d'abord être mesuré sur PD.
Nous avons ensuite utilisé cette méthode pour mesurer l'ORR sur une membrane PD recouverte d'un côté avec un polymère d'acrylate. Nous avons constaté que cette approche pouvait mesurer élégamment la cinétique de l'ORR sous ce revêtement, qui différait considérablement du courant peu ou zéro qui pourrait être mesuré avec une polarisation conventionnelle. Mais il y avait toujours la question de savoir si ce taux d'ORR mesuré est en effet la véritable cinétique de la dégradation du revêtement.
C'est à ce moment que l'idée d'utiliser une technique complémentaire telle que l'EIS classique nous a frappés. Le principe derrière l'utilisation de l'EIE était de mesurer principalement la résistance au transfert de charge pour l'ORR et les propriétés de la barrière; c'est-à-dire, résistance aux pores du revêtement de polymère.
Si l'approche HPP pouvait en effet mesurer le taux réel de dégradation du revêtement, cela doit être associé à la fois à une résistance au transfert de charge décroissante et à la résistance aux pores du revêtement avec la progression de l'ORR.
C'était exactement ce que nous avons mesuré! De plus, nous avons pu étendre avec succès cette approche combinée de l'utilisation de HPP-EIS pour mesurer le taux de dégradation d'un revêtement polymère sur une fine couche de métal industriel tel que le fer déposé sur la membrane PD.
Cette technique sera utile pour déterminer la vitesse à laquelle un revêtement polymère se désactive à partir d'un pipeline transportant de l'hydrogène mélangé au gaz naturel. Mais les implications de cette nouvelle technique HPP-EIS, à notre avis, s'étendent au-delà de la corrosion sous les revêtements dans le domaine des capteurs, des piles à combustible et des recherches fondamentales qui s'appuient sur l'exploitation des phénomènes électrochimiques interfaciaux.
Cette histoire fait partie de Science X Dialog, où les chercheurs peuvent signaler les résultats de leurs articles de recherche publiés. Visitez cette page pour plus d'informations sur la boîte de dialogue Science X et comment participer.