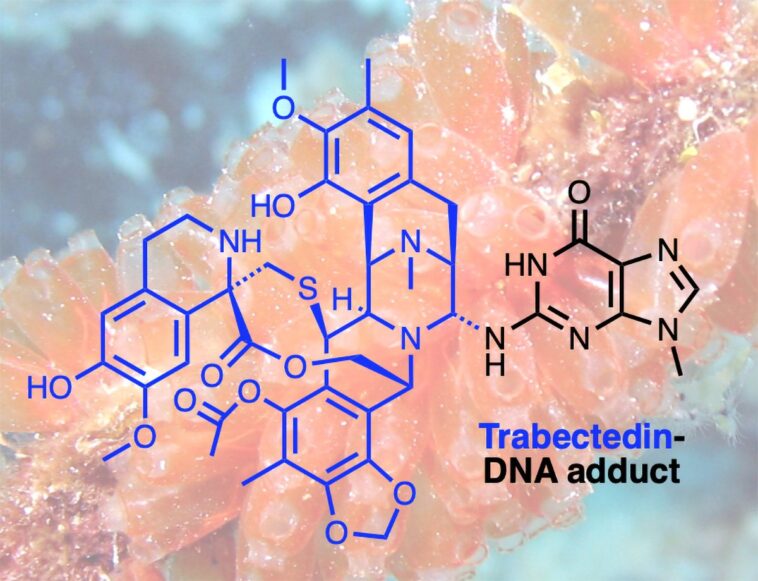
La trabectédine, un médicament anticancéreux isolé à l’origine de l’ascidie Ecteinascidia turbitana, est connue pour former des adduits cytotoxiques à l’ADN. Il est utilisé pour traiter les sarcomes et les cancers de l'ovaire et, contrairement à la plupart des agents antitumoraux, exerce sa pleine activité dans les cellules où la réparation de l'ADN est active. Crédit : Institut des sciences fondamentales
Les chercheurs ont découvert la méthode par laquelle la trabectédine contourne les mécanismes de réparation de l'ADN des cellules cancéreuses, ouvrant ainsi la voie à des traitements sur mesure.
De nombreux traitements contre le cancer agissent en attaquant le ADN des cellules cancéreuses, arrêtant leur croissance. Cependant, les cellules cancéreuses trouvent parfois des moyens de réparer les dommages causés par ces traitements, réduisant ainsi leur impact. En conséquence, les médecins se tournent de plus en plus vers une méthode innovante de traitement du cancer appelée médecine de précision.
Cette méthode consiste à sélectionner des médicaments qui correspondent précisément aux caractéristiques uniques du cancer d'un individu. La médecine de précision s’avère particulièrement bénéfique dans la lutte contre les cancers qui ont évolué pour échapper aux traitements conventionnels.
La trabectédine, un médicament prometteur dérivé de l'ascidie Ectéinascidia turbinée, a montré son potentiel dans la lutte contre les cancers résistants aux traitements conventionnels. Cependant, son mécanisme d’action précis est resté insaisissable jusqu’à présent. Un effort de collaboration dirigé par le Dr Son Kook et le professeur Orlando D. Scharer du Centre pour l'intégrité génomique de l'Institut des sciences fondamentales de Corée du Sud, ainsi que le Dr Vakil Takhaveev et le professeur Shana Sturla de l'ETH Zurich, en Suisse, a éclairé le fonctionnement interne de ce mystérieux composé.
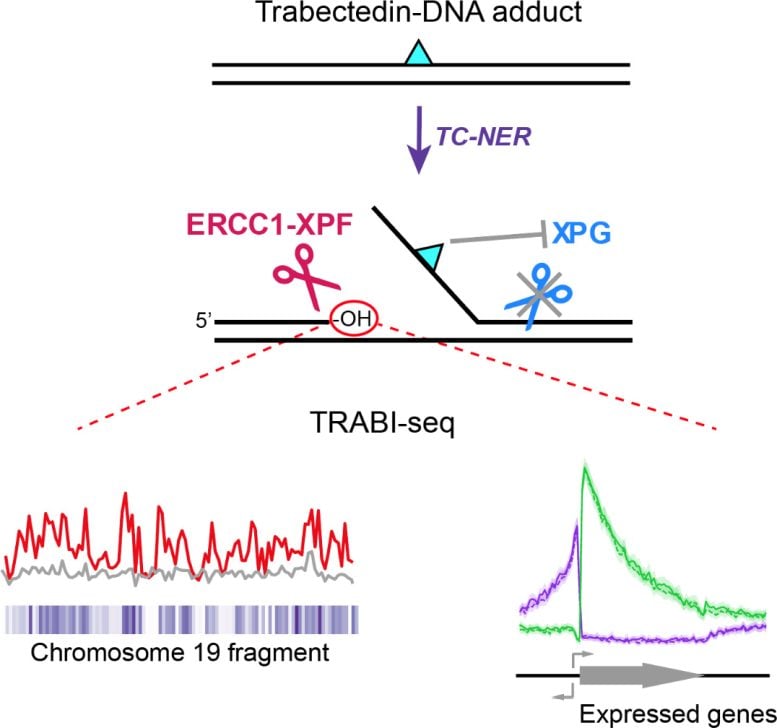
Résumé du mécanisme de formation de cassures induites par la trabectédine et de cartographie des cassures médiées par TC-NER par TRABI-Seq. Les adduits trabectédine-ADN sont reconnus par TC-NER et conduisent à une réaction avortée car ces adduits bloquent l'incision de l'endonucléase XPG, provoquant des cassures persistantes médiées par XPF. TRABI-Seq (Séquençage des cassures induites par TRABectidine) a été utilisé pour cartographier ces cassures à l’échelle du génome. La distribution de ces cassures persistantes était principalement attribuée aux régions hautement transcrites du génome. Cette approche sera désormais utilisée pour déterminer comment la trabectédine induit des cassures de l'ADN dans les génomes de diverses lignées de cellules cancéreuses afin de développer TRABI-Seq comme outil de diagnostic pour le traitement du cancer. Crédit : Institut des sciences fondamentales
Comment la trabectédine induit des cassures de l'ADN dans les cellules cancéreuses
En utilisant des tests COMET Chip très sensibles et à haut débit pour détecter les cassures formées dans le génome des cellules, les chercheurs de l'IBS ont révélé que la trabectédine induit des cassures persistantes dans l'ADN des cellules cancéreuses. Les chercheurs ont montré que ces cassures de l’ADN ne se forment que dans les cellules présentant des niveaux élevés de réparation de l’ADN, en particulier celles qui exploitent une voie appelée réparation par excision de nucléotides couplée à la transcription (TC-NER).
TC-NER est un mécanisme essentiel qui identifie les dommages à l'ADN lors de la transcription, initiant ainsi des processus de réparation impliquant deux endonucléases ERCC1-XPF et XPG. Les dommages causés à l'ADN par la trabectédine perturbent ce processus en permettant l'incision initiale par ERCC1-XPF mais en bloquant l'action ultérieure de XPG, interrompant ainsi le processus TC-NER. Cette perturbation du processus de réparation entraîne des cassures durables de l’ADN qui finissent par tuer les cellules cancéreuses.
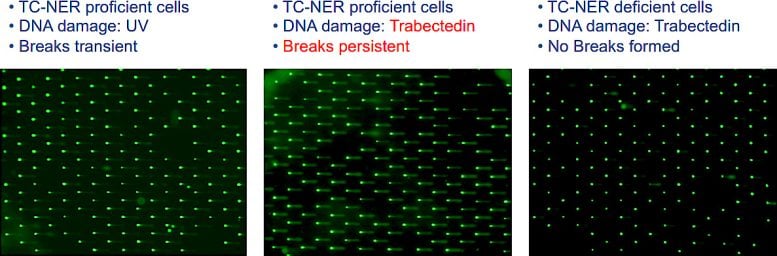
Des tests COMET Chip ont été utilisés pour mesurer les cassures cellulaires induites par la trabectédine. Chaque point vert est un noyau unique d'une cellule et la longueur de la queue ainsi que la fraction d'ADN total dans la queue (comète) émergeant de chaque noyau sont proportionnelles au nombre de cassures formées. Après le traitement UV (à gauche), quelques cassures sont visibles car les lésions UV sont excisées de l'ADN par réparation par excision de nucléotides (NER). Après un traitement à la trabectédine (au centre), des cassures de l'ADN persistent en raison d'une réaction NER avortée. Les cassures dépendent du NER car elles ne se produisent pas dans les cellules déficientes en TC-NER (à droite) avec le gène XPF inactivé. Crédit : Institut des sciences fondamentales
L'analyse des modèles de cassure de l'ADN induits par la trabectédine a révélé que des cassures se forment dans tout le génome, mais uniquement aux sites où se produit la transcription active et, avec elle, le TC-NER. En utilisant ces nouvelles connaissances sur le mécanisme d’accumulation des cassures de l’ADN, les chercheurs ont cherché à déterminer où se produisent ces cassures dans le génome. Cela a conduit au développement d'une nouvelle méthode appelée TRABI-Seq (pour TRABectedin-Induced break sequencing), qui permet l'identification précise des sites d'action de la trabectédine au sein de l'ADN des cellules tumorales.
« Cette incision par ERCC1-XPF crée un groupe hydroxyle libre marquable dans l'ADN, nous permettant de séquencer l'ADN et de localiser ces cassures », explique le Dr Son.
TRABI-Seq est testé sur diverses cellules cancéreuses pour déterminer l'efficacité de la trabectédine dans le ciblage des tumeurs dotées de capacités avancées de réparation de l'ADN, souvent associées à des niveaux de transcription élevés dus à l'activation des oncogènes. On espère que ces résultats aideront à positionner la trabectédine à la fois comme marqueur prédictif pour identifier les cancers vulnérables et comme option thérapeutique pour un traitement de précision. Grâce à sa capacité à cibler les tumeurs résistantes aux thérapies conventionnelles, la trabectédine pourrait apporter un nouvel espoir dans la lutte contre le cancer résistant aux médicaments grâce à ses capacités hautement actives de réparation de l’ADN.
L'étude a été financée par l'Institut des sciences fondamentales.