Les chercheurs ont découvert un candidat médicament, ONC201, qui a presque doublé le taux de survie des patients atteints de tumeurs cérébrales infantiles agressives connues sous le nom de gliomes diffus de la ligne médiane (DMG) ou de gliomes pontins intrinsèques diffus (DIPG).
Des études cliniques révèlent une survie prolongée chez les patients atteints de gliomes diffus de la ligne médiane recevant un traitement ONC201 ; la recherche explique également le mécanisme sous-jacent au succès du médicament.
Pour la première fois, des chercheurs ont identifié un médicament candidat potentiel qui semble prometteur pour améliorer les résultats pour les patients souffrant d’un type spécifique de tumeur cérébrale infantile pour laquelle il manque actuellement d’options de traitement efficaces. Il a été observé que le composé, nommé ONC201, double presque les taux de survie des patients diagnostiqués avec un gliome médian diffus (DMG) ou un gliome pontique intrinsèque diffus (DIPG), par rapport aux résultats antérieurs pour les patients.
Les résultats sont rapportés par une équipe internationale de chercheurs dirigée par le Rogel Cancer Center de l’Université du Michigan et le Chad Carr Pediatric Brain Tumor Center.
En plus de rendre compte des résultats de deux essais cliniques à un stade précoce, l’article révèle les mécanismes sous-jacents à l’origine du succès du composé dans ces tumeurs. L’article est publié dans Découverte du cancer, une revue de l’Association américaine pour la recherche sur le cancer.
Les gliomes diffus de la ligne médiane, notamment DIPG avec une mutation appelée H3K27M, sont particulièrement agressifs, avec un taux de survie global de 11 à 15 mois. Ces tumeurs sont plus fréquemment retrouvées chez les enfants et les jeunes adultes. Le seul traitement disponible est la radiothérapie, et même cela est difficile car les tumeurs sont situées au milieu de régions cérébrales dotées de fonctions critiques.
« C’est une tumeur incroyablement difficile à traiter », a déclaré l’auteur principal Carl Koschmann, MD, professeur agrégé de neuro-oncologie pédiatrique et directeur scientifique clinique du Chad Carr Pediatric Brain Tumor Center de Michigan Medicine. « Avant cette étude, plus de 250 essais cliniques n’ont pas permis d’améliorer les résultats. C’est une fissure majeure dans l’armure.
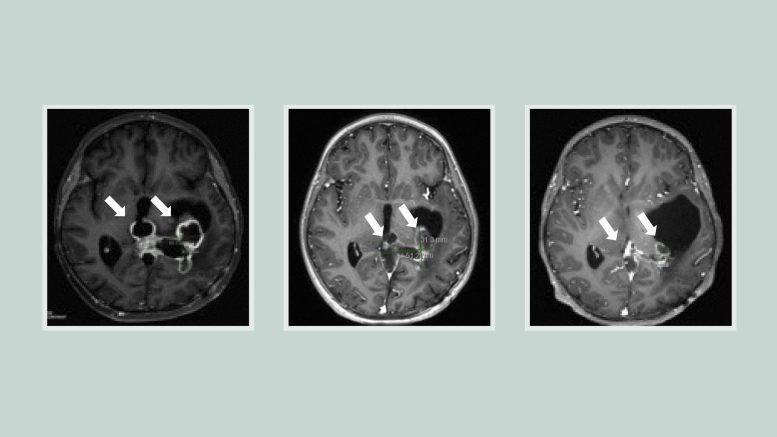
Une série d’analyses cérébrales montre une tumeur rétrécissant en réponse à ONC201. Crédit : Médecine du Michigan
Dans deux essais cliniques testant ONC201 chez un total de 71 patients atteints de gliomes diffus de la ligne médiane mutés par H3K27M, la survie globale médiane était de près de 22 mois pour les tumeurs qui n’avaient pas récidivé au moment de l’inscription. Près d’un tiers des patients ont vécu plus de deux ans.
ONC201 a emprunté un chemin inhabituel vers un essai clinique. Initialement conçu pour cibler les récepteurs de la dopamine, qui sont régulés positivement dans de nombreuses tumeurs différentes, les chercheurs ont constaté que le médicament traverse la barrière hémato-encéphalique, l’un des plus grands défis dans la conception de médicaments contre les tumeurs cérébrales. Les premiers essais sur le glioblastome n’ont pas abouti, mais un petit nombre de patients atteints de DMG porteurs de la mutation H3K27M ont eu des résultats plus prometteurs. Sans comprendre pourquoi cela fonctionnait mieux chez ces patients, un essai de phase 1 a été lancé chez des enfants et des jeunes adultes atteints de DMG muté par H3K27M.
Pendant ce temps, Koschmann et le co-auteur Sriram Venneti, MD, Ph.D., essayaient de comprendre ce qui se passait dans ces cellules tumorales.
Au cours de l’essai, ils ont collecté le liquide céphalo-rachidien des patients. Ils ont utilisé ce liquide pour analyser les changements métaboliques et ont découvert que l’ONC201 pénétrait dans les cellules tumorales et affectait les mitochondries. Les patients qui ont répondu au médicament ont présenté une augmentation d’un métabolite appelé L-2HG produit par les cellules tumorales.
Koschmann a qualifié cette découverte de « très inattendue ». L’équipe a découvert qu’une augmentation de la L-2HG inversait les signaux épigénétiques définissant la tumeur, amenant les cellules tumorales à se différencier davantage et à se diviser moins. Plus les patients prenaient ONC201 longtemps, plus les tumeurs présentaient ces inversions épigénétiques.
« Cela pourrait expliquer pourquoi cette population de patients répondait si bien au médicament parce qu’elle présentait cette anomalie épigénétique spécifique qui pouvait être désactivée par ONC201. Les tumeurs présentent un changement épigénétique provoqué par la mutation H3K27M et ONC201 annule métaboliquement ce changement », a déclaré Venneti, professeur agrégé de pathologie et de pédiatrie et directeur de la recherche scientifique du Chad Carr Pediatric Brain Tumor Center de Michigan Medicine.
Des essais cliniques supplémentaires sont actuellement en cours, notamment en testant ONC201 en association avec d’autres thérapies. Les chercheurs du Chad Carr Pediatric Brain Tumor Center de l’UM continuent également de chercher des moyens de surmonter la résistance à l’ONC201 en utilisant des combinaisons de médicaments.
Koschmann note que même un quasi-doublement de la survie n’est pas suffisant pour les familles de patients présentant ce diagnostic, car la tumeur reste très mortelle. Mais il espère que cette première étape mènera à de plus grands progrès à l’avenir.
« Pour l’instant, nous avons cette population de patients qui n’avait pas de médicament auparavant, et maintenant nous voyons de nombreuses tumeurs réagir. Nous disposons d’une plateforme sur laquelle nous appuyer et nous pouvons également expliquer pourquoi elle fonctionne », a-t-il déclaré.
« Nous sommes vraiment enthousiasmés par cette étude et envisageons que l’ONC201 devienne la norme de soins pour ces patients dans un avenir proche », a déclaré Venneti.
Le financement de ces travaux provient du Instituts nationaux de la santéDépartement de la Défense, Chad Carr Pediatric Brain Tumor Center de l’Université du Michigan, The Evans Family, ChadTough Defeat DIPG Foundation, Catching Up with Jack, Pediatric Brain Tumor Foundation, Prières de la Fondation Maria, Michael Miller Memorial Foundation, Morgan Behen Golf Classic, Yuvaan Fondation Tiwari, Fondation Sontag, Fondation Alex Lemonade Stand, Fondation Hyundai Hope, Conseil norvégien de la recherche, Autorité régionale de la santé du sud-est de la Norvège, The Université d’OsloOncoceutics, Inc., Chimerix, Inc., Making Headway Foundation, Gustave Roussy Foundation Pediatric Campaign, Imagine for Margo Charity, National Research Foundation of Korea, DGIST Start-up Fund et University of Michigan Taubman Institute.
Ce travail a été soutenu par ces ressources partagées du Rogel Cancer Center : Irradiation expérimentale et imagerie moléculaire préclinique