Les protéines métamorphiques peuvent être considérées comme les «métamorphes» des cellules humaines, animales et bactériennes. Leur capacité à basculer radicalement entre deux formes différentes leur permet de s'adapter aux environnements changeants et d'exécuter diverses fonctions.
On sait peu de choses sur la façon dont les protéines métamorphiques se transforment malgré leur utilité dans les organismes vivants. Pour aider à lutter contre ce mystère, un nouveau document dans la section « Perspectives » du Journal Actes de l'Académie nationale des sciences (PNA) propose une « théorie audacieuse », a déclaré le co-auteur John Orban, professeur au Département de chimie et de biochimie de l'Université du Maryland et de la recherche sur la bioscience et la biotechnologie (IBBR).
Orban et son co-auteur Andy Liwang, professeur de chimie et de biochimie à l'Université de Californie, suggèrent que de nombreuses protéines métamorphiques ont une «dépendance à la température sous-jacente». S'il est confirmé, cela signifierait que la température – et la température froide en particulier – jouent un rôle fondamental dans l'évacuation de la mise en forme dans les protéines métamorphiques.
En fin de compte, une meilleure compréhension des protéines métamorphiques pourrait faire progresser la recherche biomédicale et le développement de médicaments vitaux.
« Il peut être possible de concevoir des protéines qui sont commutables et qui ont plus d'une fonction », a déclaré Orban. « Ils pourraient potentiellement être des protéines furtives qui entrent dans une cellule cancéreuse et prétendent être un seul État, mais dans certaines conditions environnementales, passez à un état qui pourrait tuer la cellule, par exemple. »
Les protéines métamorphiques sont connues pour changer de forme en réponse à divers «déclencheurs» environnementaux – comme des changements d'acidité ou d'oxydation – mais la théorie d'Orban et de Liwang va plus loin. Leur recherche cherche à expliquer pourquoi un équilibre, ou équilibre, existe entre les différentes formes que les protéines métamorphiques peuvent prendre.
« Les protéines métamorphiques ne peuvent pas se métamorner à moins qu'il y ait un équilibre entre les deux états et notre hypothèse est que la raison sous-jacente de cet équilibre est basée sur la température », a déclaré Orban. « Nous pensons que cela peut être une sorte de mécanisme universel. »
Orban a déclaré que cette hypothèse a été inspirée par une étude antérieure qu'il a co-écrite en 2023. Ce document a révélé qu'une protéine métamorphique d'ingénierie a basculé entre les états pliés lorsque les chercheurs ont ajusté la température sur une plage « relativement étroite » entre 5 et 30 degrés Celsius.
« Il y a maintenant quelques autres exemples de protéines métamorphiques naturelles qui le font, mais c'était le premier exemple d'une protéine conçue qui change de manière réversible en utilisant uniquement la température », a déclaré Orban. « Andy et moi avons commencé à parler plus et nous nous sommes demandé si d'autres protéines métamorphiques suivaient le même schéma. »
Dans leur nouveau PNA Document, Orban et Liwang ont étudié 26 paires de protéines métamorphiques qui ont été étudiées auparavant, mais jamais avec cette théorie de la dépendance à la température. Plus précisément, les chercheurs ont analysé les différences dans les contacts hydrophobes – les zones de répartition de l'eau qui aident à maintenir les structures ensemble – d'un état protéique à l'autre.
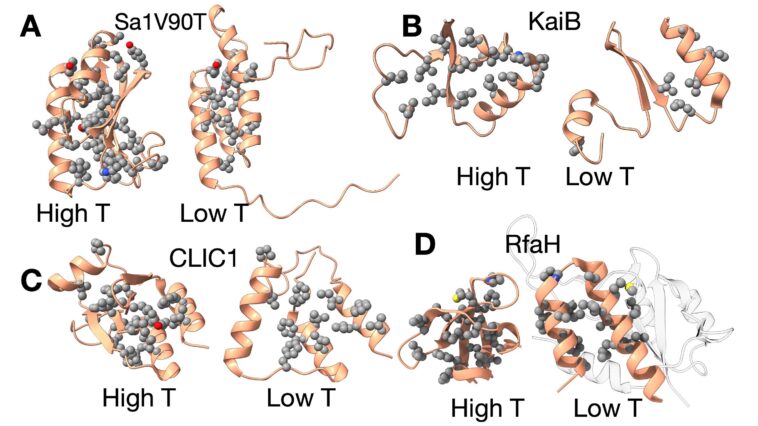
Lorsque des données expérimentales étaient disponibles, les chercheurs ont constaté que presque toutes les paires de protéines avaient des différences significatives dans les contacts hydrophobes et que ces différences étaient étroitement liées à des changements dépendants de la température. Les états à basse température étaient associés à moins de contacts hydrophobes, résultant en un état plus flexible qui peut être propice à la mise en forme.
Les preuves découvertes jusqu'à présent semblent soutenir leur théorie sur le rôle de la température dans les protéines de métamorphe.
« C'est une hypothèse de travail, mais jusqu'à présent, elle a été soutenue », a déclaré Orban. « Nous avons été surpris parce que nous pensions que c'était une idée assez audacieuse. »
À l'avenir, cette recherche pourrait être appliquée à la recherche de protéines plus métamorphiques, qui sont difficiles à identifier. La banque mondiale de données de protéines contient environ 200 000 protéines monomorphes connues – celles avec une seule structure stable – mais moins de 100 protéines métamorphiques.
En utilisant la température comme un déclencheur, Orban pense que certaines protéines considérées comme monomorphes pourraient se transformer, révélant leur vraie nature en tant que protéines métamorphiques.
Bien que la principale motivation d'Orban soit de répondre aux questions sur les mécanismes sous-jacents qui déclenchent des protéines de mise en forme, il est également optimiste quant aux applications futures.
« Notre intérêt jusqu'à présent a été surtout fondamental, mais nous parlons d'éventuelles applications de biotechnologie et je ne pense pas que ce soit une tarte dans le ciel », a déclaré Orban.
« Je pense qu'il est tout à fait possible que dans un avenir pas trop lointain, nous prédisons plus de manière fiable les protéines métamorphiques, les concevant et les mettant en place pour nous. »