La composition de la sueur en fait un précieux liquide diagnostique. Bien qu'il s'agisse principalement de l'eau, la petite fraction contenant des électrolytes, des sous-produits métaboliques et des traces chimiques peut révéler des informations importantes sur la santé d'une personne. Aujourd'hui, les capteurs commerciaux basés sur la transpiration peuvent déjà suivre la déshydratation, la perte d'électrolyte, etc. Une application émergente est la mesure de l'acide lactique dans la transpiration.
L'acide lactique, ou plus précisément L-lactate, est un sous-produit du métabolisme produit principalement dans les cellules musculaires lorsque le glucose est décomposé pour l'énergie dans des conditions à faible teneur en oxygène, comme pendant une activité physique intense. Les athlètes et les entraîneurs utilisent des mesures de lactate pour évaluer l'endurance et planifier les entraînements, mais des niveaux élevés peuvent également être un signe d'avertissement pour des conditions comme l'acidose lactique.
Les capteurs d'acide lactique utilisent généralement la lactate oxydase (LOX), une enzyme attachée à une électrode biocompatible, pour mesurer les niveaux de lactate. LOX se lie au l-lactate et catalyse son oxydation en pyruvate, produisant du peroxyde d'hydrogène comme sous-produit. Ce peroxyde d'hydrogène est ensuite oxydé ou réduit électrochimiquement à l'électrode, générant un courant mesurable qui correspond à la concentration de lactate dans la transpiration.
Cependant, LOX est sensible au pH. Il fonctionne mieux au pH neutre et perd une grande partie de son activité dans l'environnement acide de la transpiration, qui a un pH d'environ 4,0. L'une des approches pour résoudre ce problème est d'ajouter des sucres qui aident à stabiliser l'enzyme dans des conditions acides.
Dans une étude récente, des chercheurs de l'Université des sciences de Tokyo (TUS) au Japon ont constaté que le saccharose monolauré offre une protection nettement meilleure pour les sucres conventionnels que les sucres conventionnels. Dans les tests simulant le pH acide de la transpiration, les électrodes modifiées avec le monolaure de saccharose ont conservé environ 80% de l'activité LOX à pH 5,0, contre seulement 50% sans monolaure de saccharose.
Leur travail a été publié dans la revue Langmuir. L'étude a été dirigée par le professeur agrégé Isao Shitanda en collaboration avec Anton Paar Japan KK, et a inclus les contributions du professeur agrégé Taku Ogura de l'Institut de recherche pour les sciences et la technologie et Mme Chiaki Sawahara, diplômée de la maîtrise d'Anton Paar Japan KK à Tus, et le Dr Yuichi Takasaki d'Anton Paar Japan KK à Tus, et le Dr Yuichi Takasaki d'Anton Paar Japan KK à Tus, et le Dr Yuichi Takasaki d'Anton Paar Japan KK à Tus, et le Dr Yuichi Takasaki d'Anton Paar Japan KK
« La surveillance en temps réel du lactate de sueur devient de plus en plus important pour l'entraînement sportif et la gestion des coups de chaleur. Pour mesurer le lactate de sueur, l'enzyme doit rester stable sur le capteur dans des conditions acides. Dans cette étude, nous montrons que l'utilisation d'un agent stabilisant préserve l'activité enzymatique dans des solutions acides en formant une structure spéciale », explique le Dr Shitanda.
L'équipe a fabriqué des électrodes en or et en carbone sans stabilisateurs, avec du saccharose monolauré et avec du maltose (qui est également un stabilisateur). Ils ont ensuite exposé les électrodes dans des solutions neutres (pH 7,0), légèrement acides (pH 6,0) et plus acides (pH 5,0) pour tester leur fonctionnement lorsqu'elles se comporteraient à la transpiration.
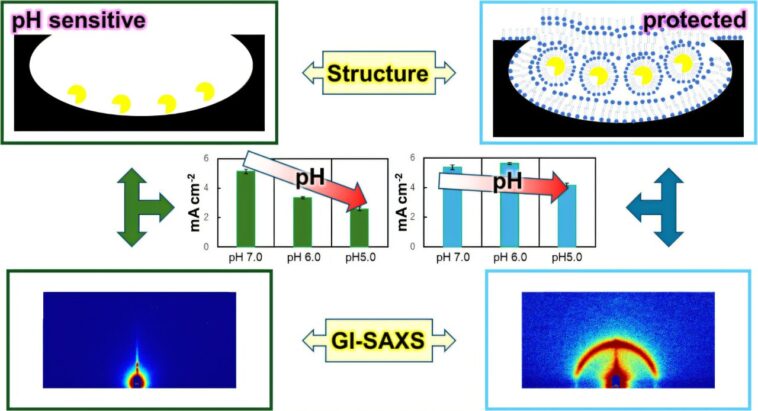
Sans stabilisateur, le courant mesuré a chuté de manière significative à mesure que le pH tombait. Les électrodes atteintes de maltose ont montré une petite amélioration à pH 6,0 mais presque aucune à pH 5,0. En revanche, les électrodes modifiées avec le monolaure de saccharose ont conservé environ 80% de leur activité à pH 5,0.
Pour étudier pourquoi le monolaure de saccharose a offert une telle protection efficace, les chercheurs ont examiné la nanostructure des surfaces d'électrodes en utilisant la diffusion des rayons X à petit angle d'incidence (GI-saxes). Cette technique consiste à diriger les rayons X à un angle très peu profond pour observer directement comment le saccharose monolauré et LOX s'organisent sur les surfaces des électrodes.
Les chercheurs ont découvert que le monolaure de saccharose formait des réseaux hexagonaux soignés avec des couches lamellaires sur des surfaces d'électrode lisse. Lorsque Lox a été ajouté, il est devenu intégré dans ces structures hexagonales et en couches.
Dans les solutions diluées, le monolaure de saccharose s'est avéré s'assembler en micelles de minuscules noyaux, qui fusionnent en formes en forme de tige et se mettent en réseaux hexagonaux. L'enzyme s'inscrit dans ces structures, créant une barrière protectrice qui bloque les ions hydrogène tout en permettant à l'eau et aux métabolites comme l'acide lactique de passer, en préservant la capacité de l'enzyme à fonctionner tout en le rendant résistant aux changements de pH.
En révélant ce mécanisme de protection, l'étude ouvre la voie à des capteurs de sueur à l'acide lactique plus durables et plus fiables pour une surveillance continue de la santé. « Comprendre ce mécanisme pourrait faciliter le développement d'électrodes enzymatiques hautement stables et de biodévices haute performance », conclut le Dr Shitanda.
De plus, le saccharose monolauré est un stabilisateur sûr, abordable et évolutif pour l'utilisation commerciale. De plus, l'approche réalisée dans cette étude pourrait être utilisée pour d'autres conditions environnementales, plutôt que pour un pH faible et pourrait également être utilisée pour stabiliser d'autres enzymes.