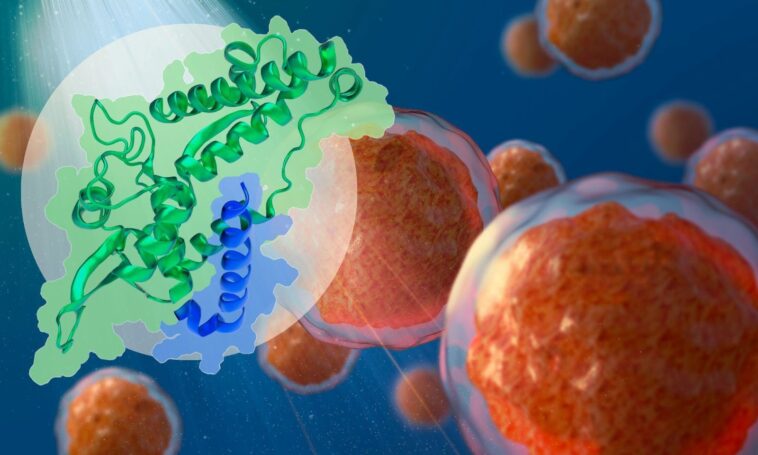
La nouvelle étude démontre la base structurelle de l'interaction entre les protéines favorisant le cancer MAGEA4 (vert) et RAD18 (bleu). Crédit : Isabel Romero Calvo/EMBL
Des recherches récentes du groupe Bhogaraju de l'EMBL Grenoble ont découvert les mécanismes par lesquels la famille de protéines MAGE, connue pour son rôle dans la promotion du cancer, s'attache à ses cibles. Cette découverte ouvre la voie à la création de médicaments anticancéreux spécifiquement conçus pour inhiber ces protéines.
Des chercheurs de l'EMBL Grenoble, dirigés par le groupe Bhogaraju, ont découvert de nouvelles façons par lesquelles une famille de protéines liées au cancer se lient à leurs cibles. Les résultats de l'étude, publiés dans La revue EMBOpourrait potentiellement contribuer au développement de médicaments contre certains cancers résistants à la chimiothérapie et à la radiothérapie.
La famille des gènes antigènes du mélanome (MAGE) comprend plus de 40 protéines chez l'homme, dont la plupart ne sont présentes dans les testicules que dans des conditions saines. Cependant, dans de nombreux cancers, ces protéines se trouvent en quantités élevées dans les tissus où elles ne sont généralement pas exprimées et on pense qu’elles jouent un rôle dans la progression du cancer.
L’une de ces protéines MAGE – MAGEA4 – est connue pour interagir avec RAD18, une protéine connue pour être abondante dans certaines cellules cancéreuses. Ce dernier fait partie de la machinerie moléculaire qui aide la cellule à réparer les dommages causés à ses cellules. ADN. Des niveaux élevés de RAD18 sont responsables de la résistance de plusieurs cancers à la chimiothérapie ou à la radiothérapie génotoxique (endommageant l’ADN).
Le rôle de RAD18 dans la résistance des cellules cancéreuses
RAD18 fonctionne en attachant de petites étiquettes moléculaires – appelées ubiquitine – à différentes protéines. Cette étiquette, comme un timbre postal, indique à la cellule quel serait le sort de cette protéine. RAD18 peut également attacher cette balise à elle-même – un processus appelé autoubiquitination. Cela la cible pour sa dégradation, c'est-à-dire indique à la cellule de se débarrasser des niveaux excédentaires de cette protéine.
Le groupe Bhogaraju de l'EMBL Grenoble utilise des approches basées sur la biologie structurelle et cellulaire pour étudier ces voies basées sur l'ubiquitine dans la physiologie normale et les maladies. L'équipe, en collaboration avec le groupe Hennig de l'EMBL Heidelberg, a décidé d'examiner plus en profondeur l'interaction entre les protéines MAGEA4 et RAD18, en utilisant AlphaFoldun outil basé sur l'intelligence artificielle qui permet aux scientifiques de prédire la structure des protéines.
L'équipe, qui comprenait Simonne Griffith-Jones, doctorante du groupe Bhogaraju, et Urbi Mukhopadhyay, postdoctorante, a découvert que MAGEA4 possède un sillon qui peut lier une section de la protéine RAD18, ce qui empêche cette dernière de s'attacher à elle-même et de se dégrader par la suite.
Fait intéressant, les chercheurs pourraient utiliser un court fragment de protéine synthétique, imitant la partie de RAD18 qui lie le sillon de MAGEA4, pour bloquer l'interaction entre les deux protéines. Cela pourrait potentiellement ouvrir la voie à la conception de médicaments ciblant ce complexe et empêchant l’accumulation de RAD18 dans les cellules cancéreuses.
Les chercheurs ont également découvert un sillon très similaire dans une autre protéine de la famille MAGE, utilisée pour réguler une autre protéine favorisant le cancer. Ils pensent que ce sillon pourrait être une caractéristique générale de la famille MAGE, utilisée pour médier la liaison aux protéines liées au cancer.
En plus du sillon, les scientifiques ont également observé que deux parties de la protéine RAD18 interagissent entre elles, ce qui l'aide à attacher l'étiquette ubiquitine à une protéine qui favorise la survie des cellules cancéreuses. Ils pourraient bloquer cette fonction à l’aide de stratégies génétiques, ce qui implique que les futurs médicaments conçus pour bloquer cette interaction pourraient potentiellement resensibiliser les cellules cancéreuses devenues résistantes aux chimiothérapies ou aux radiothérapies.
« Nous sommes enthousiasmés par ces données car nos résultats semblent applicables à de nombreux MAGE, ouvrant la voie au ciblage des MAGE responsables des cancers », a déclaré Sagar Bhogaraju, chef de groupe à l'EMBL Grenoble. « Nous travaillons actuellement sur le développement de méthodes pour cribler des composés qui lier le hotspot nouvellement découvert des MAGE.