Les protéines de liaison à l'ARN utilisent un double mécanisme de liaison impliquant des domaines de doigt du zinc (ZNF) et des régions intrinsèquement désordonnées (IDR), rapporte une nouvelle étude de l'Institut des sciences, Tokyo, Japon.
En utilisant la modélisation moléculaire avancée, l'étude analyse un complexe « FUS protéine-ARN » – révolutionnant comment la protéine utilise son domaine ZNF pour la reconnaissance de la séquence d'ARN et son domaine IDR flexible pour ses interactions non spécifiques. Cette stratégie révolutionnaire est probablement commune à la liaison à l'acide nucléique, offrant de nouvelles informations sur la science moléculaire.
Les protéines qui peuvent se lier aux acides nucléiques jouent un rôle essentiel dans divers aspects de la régulation des gènes, de la réplication de l'ADN et de la réparation au traitement et à la traduction de l'ARN.
Comprendre comment ces protéines reconnaissent et interagissent avec les acides nucléiques est la clé pour déchiffrer le mécanisme sous-jacent de la façon dont les cellules régulent l'expression des gènes et s'adaptent aux environnements changeants.
Bien que la plupart de ces protéines impliquent à la fois des domaines bien structurés et des régions flexibles et intrinsèquement désordonnées (IDR), la façon dont ces domaines fonctionnent ensemble dans la liaison à l'ARN des protéines restent flous.
Un exemple notable est la protéine « fusionnée dans le sarcome » (FUS), une protéine de liaison à l'ARN bien connue impliquée dans la régulation des gènes et les maladies neurodégénératives. Bien que largement étudiée, son mécanisme de liaison exact reste mal compris.
Pour surmonter cet écart, le professeur Akio Kitao et le doctorat. L'étudiant Soichiro Kijima de la School of Life Science and Technology de l'Institut of Science Tokyo (Science Tokyo), Japon, a utilisé des simulations moléculaires pour analyser les interactions entre les séquences de protéine FUS et d'ARN.
Les résultats ont été publiés dans le Journal of Chemical Information and Modeling.
La protéine FUS a une structure distincte avec un domaine de doigt de zinc de type RanBP2 à liaison à l'ARN (ZNF) bien structuré (ZNF), suivi de longues régions de protéines désordonnées appelées IDR.
Les ZNF sont de petits domaines protéiques contenant des ions de zinc et sont les domaines de liaison aux acides nucléiques les plus courants chez les eucaryotes.
En utilisant une combinaison de dynamique moléculaire et de techniques d'échantillonnage améliorées, l'équipe a simulé comment la protéine FUS interagit avec un brin d'ARN court contenant une séquence cible connue (GGU).
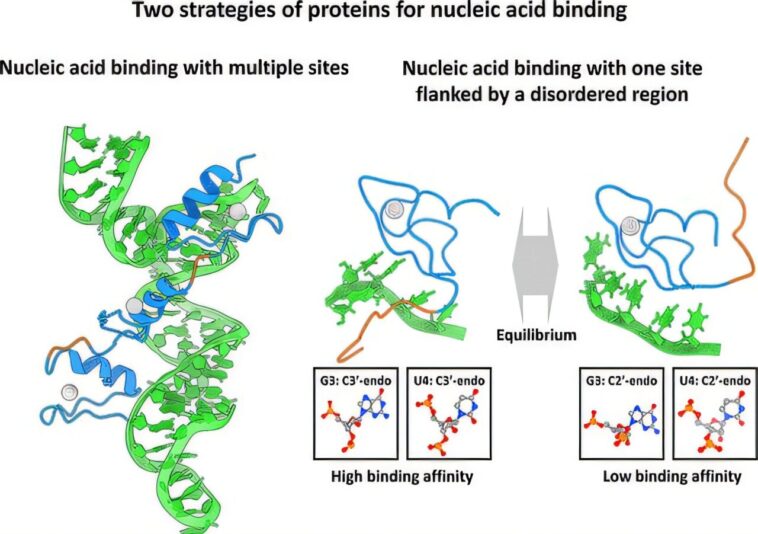
Leurs résultats ont révélé deux modes de liaison distincts: l'un impliquant uniquement la région structurée du ZNF et un deuxième mode plus stable où le domaine ZNF et la région désordonnée interagissent avec le brin d'ARN.
« Nous avons observé que le domaine ZNF structuré reconnaît des séquences d'ARN spécifiques, mais à elle seule, elle ne se lie que faiblement », explique Kitao. « Étonnamment, c'est l'IDR désordonné qui stimule cette interaction. »
Selon les résultats, la région IDR désordonnée se fixe à l'ARN de manière non spécifique à travers les interactions basées sur les charges avec les groupes de phosphate, abaissant la constante de dissociation de deux fois.
Ces interactions sont indépendantes des séquences et améliorent l'affinité globale de liaison de la protéine. De plus, il a été noté que ces régions IDR flexibles provoquent une distorsion du squelette de l'ARN qui stabilise davantage l'interface protéine-ARN. L'effet combiné de ZNF et IDR se traduit par une structure plus étroitement tenue qui est près de 10 fois plus forte que le ZNF seule.
En s'appuyant sur cela, les chercheurs ont également effectué une analyse de séquence supplémentaire d'autres protéines contenant des IDR, ce qui suggère que ce mécanisme de liaison coopératif peut être plus courant qu'on ne le connu auparavant.
« Nos résultats suggèrent que les IDR ne sont pas seulement des lieurs passifs », note Kitao. « Ils contribuent activement au mécanisme de liaison à l'ARN et peuvent avoir des implications plus larges dans la science moléculaire. »
Dans l'ensemble, l'étude fournit un nouveau cadre pour cartographier comment les protéines de liaison à l'acide nucléique atteignent à la fois la spécificité et la flexibilité, ce qui est essentiel dans la régulation des gènes. Il ouvre également des voies passionnantes pour la conception de médicaments avec une reconnaissance à double mode pour une détection biomoléculaire améliorée et un ciblage des gènes.
Pour l'avenir, les chercheurs prévoient d'explorer si ce mécanisme fonctionne dans d'autres protéines impliquées dans le métabolisme de l'ARN et comment les modifications post-traductionnelles des régions désordonnées peuvent affecter la dynamique de liaison – dans ce domaine, approfondissez notre compréhension des mécanismes moléculaires.