Un scientifique pharmaceutique de l'Université nationale de Singapour (NUS) a développé une méthode qui peut mesurer l'efficacité cinétique d'une enzyme contre plus de 200 000 substrats peptidiques potentiels dans une seule expérience.
La caractérisation des interactions entre les enzymes et leurs substrats est une tâche fondamentale en biochimie, essentielle pour l'ingénierie de nouveaux biocatalystes, la compréhension des mécanismes de la maladie et la conception de la thérapeutique. Bien que les techniques existantes puissent étudier de nombreuses réactions enzymatiques en parallèle, la mise à l'échelle de ces méthodes pour analyser de manière approfondie les préférences d'une enzyme à travers un vaste espace de substrats possibles reste un défi pratique.
Le professeur adjoint Alexander Vinogradov du Département de pharmacie et des sciences pharmaceutiques de NUS a développé une stratégie appelée Domek (mesure unique basée sur les dispositions d'ARNm de la cinétique enzymatique) qui répond à ce besoin.
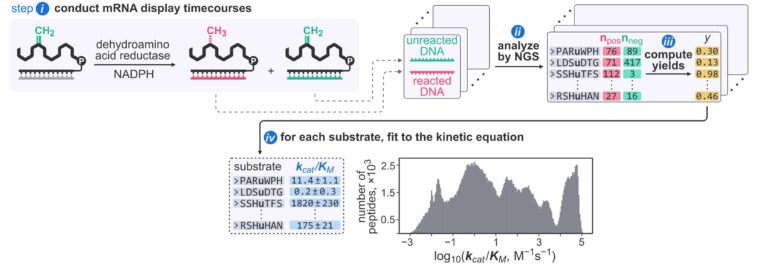
La méthode combine une technique appelée affichage d'ARNm, qui permet une préparation rapide de milliers de substrats enzymatiques, avec un séquençage de nouvelle génération pour calculer un paramètre cinétique clé, connu sous le nom de constante de spécificité (kchat/ KM), pour chaque substrat individuel dans une seule expérience.
Domek est une technique opérationnellement simple et généralisable qui repose sur des équipements de biologie moléculaire standard et ne nécessite aucune expertise en ingénierie. Ce travail de recherche a été réalisé en collaboration avec le professeur Hiroaki Suga de l'Université de Tokyo, au Japon.
Au-delà de la mesure de la cinétique, le grand ensemble de données produit par Domek a permis à l'équipe de tirer parti de la modélisation statistique pour comprendre comment une enzyme reconnaît ses substrats. Cela aide à démêler la source de l'efficacité catalytique extraordinaire des enzymes et a des applications immédiates dans l'ingénierie de nouveaux biocatalystes et thérapeutiques.
L'étude, publiée dans la revue Chemdémontre l'utilité de cette approche en effectuant un profilage unique d'une enzyme réductase bactérienne, qui peut être utilisée pour concevoir des agents thérapeutiques potentiels.
Les auteurs ont surveillé de manière fiable la cinétique enzymatique pour 285 000 substrats peptidiques distincts et ont validé les résultats avec des méthodes traditionnelles.
Le professeur adjoint Vinogradov a déclaré: « Notre approche fournit un moyen de recueillir des données cinétiques quantitatives sur une échelle difficile à réaliser précédemment. Nous travaillons maintenant pour étendre et généraliser la technique, ainsi que pour les mesurer davantage pour mesurer des millions de réactions en parallèle. »
Pour l'avenir, l'équipe vise à adapter le cadre Domek pour une utilisation avec d'autres classes d'enzymes impliquées dans les modifications post-traductionnelles des peptides et des protéines.