Les chercheurs ont développé une nouvelle technique de microscopie révélant de nouveaux détails dans les tissus cérébraux humains, montrant que certaines tumeurs cérébrales de bas grade pourraient être plus agressives qu’on ne le pensait auparavant. Cette méthode pourrait améliorer considérablement la manière dont les tumeurs sont diagnostiquées et traitées. (Concept de l’artiste.) Crédit : Issues.fr.com
Une nouvelle technique de microscopie permettant une imagerie à haute résolution pourrait un jour aider les médecins à diagnostiquer et à traiter les tumeurs cérébrales.
Grâce à une nouvelle technique de microscopie, MIT et les chercheurs du Brigham and Women’s Hospital/Harvard Medical School ont photographié le tissu cérébral humain avec plus de détails que jamais, révélant des cellules et des structures qui n’étaient pas visibles auparavant.
Parmi leurs découvertes, les chercheurs ont découvert que certaines tumeurs cérébrales « de bas grade » contiennent plus de cellules tumorales agressives que prévu, ce qui suggère que certaines de ces tumeurs pourraient être plus agressives qu’on ne le pensait auparavant.
Les chercheurs espèrent que cette technique pourra éventuellement être déployée pour diagnostiquer des tumeurs, générer des pronostics plus précis et aider les médecins à choisir des traitements.
« Nous commençons à voir à quel point les interactions des neurones et des synapses avec le cerveau environnant sont importantes pour la croissance et la progression des tumeurs. Beaucoup de ces choses que nous ne pouvions vraiment pas voir avec les outils conventionnels, mais nous disposons désormais d’un outil pour examiner ces tissus au niveau à l’échelle nanométrique et essayez de comprendre ces interactions », explique Pablo Valdes, ancien postdoctorant du MIT, aujourd’hui professeur adjoint de neurosciences à la branche médicale de l’Université du Texas et auteur principal de l’étude.
Edward Boyden, professeur Y. Eva Tan en neurotechnologie au MIT ; professeur de génie biologique, d’arts et sciences médiatiques et de sciences du cerveau et cognitives; un enquêteur du Howard Hughes Medical Institute ; et membre du McGovern Institute for Brain Research du MIT et du Koch Institute for Integrative Cancer Research ; et E. Antonio Chiocca, professeur de neurochirurgie à la Harvard Medical School et président de neurochirurgie au Brigham and Women’s Hospital, sont les auteurs principaux de l’étude, publiée récemment dans Médecine translationnelle scientifique.
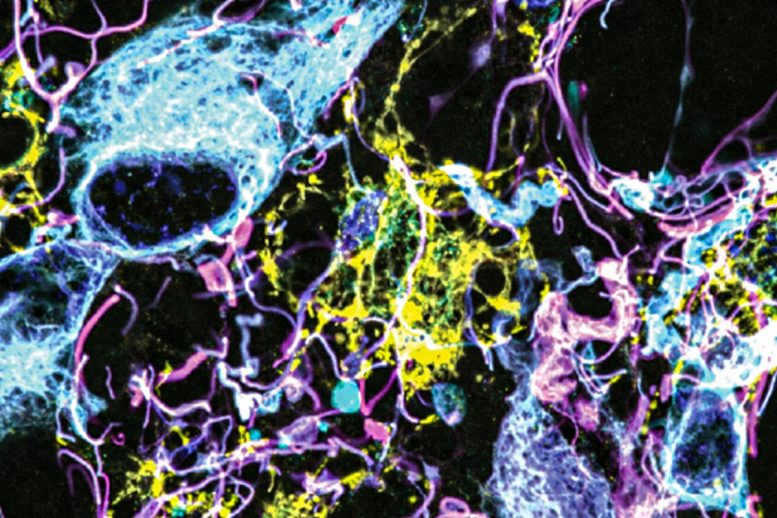
Grâce à une nouvelle technique de microscopie, les chercheurs du MIT et de la Harvard Medical School ont photographié les tissus cérébraux humains avec plus de détails que jamais. Dans cette image d’un gliome de bas grade, le bleu clair et le jaune représentent différentes protéines associées aux tumeurs. Le rose indique une protéine utilisée comme marqueur pour les astrocytes et le bleu foncé indique l’emplacement des noyaux cellulaires. Crédit : Avec l’aimable autorisation des chercheurs
Rendre les molécules visibles
La nouvelle méthode d’imagerie est basée sur la microscopie à expansion, une technique développée dans le laboratoire de Boyden en 2015 sur la base d’un principe simple : au lieu d’utiliser des microscopes puissants et coûteux pour obtenir des images haute résolution, les chercheurs ont conçu un moyen d’étendre le tissu lui-même, permettant il doit être imagé à très haute résolution avec un microscope optique ordinaire.
La technique fonctionne en intégrant le tissu dans un polymère qui gonfle lorsque de l’eau est ajoutée, puis en ramollissant et en brisant les protéines qui maintiennent normalement les tissus ensemble. Ensuite, l’ajout d’eau fait gonfler le polymère, séparant toutes les protéines les unes des autres. Cet agrandissement des tissus permet aux chercheurs d’obtenir des images avec une résolution d’environ 70 nanomètres, ce qui n’était auparavant possible qu’avec des microscopes très spécialisés et coûteux comme les microscopes électroniques à balayage.
En 2017, le laboratoire Boyden a développé un moyen de multiplier les échantillons de tissus humains préservés, mais les réactifs chimiques qu’ils ont utilisés ont également détruit les protéines que les chercheurs souhaitaient marquer. En marquant les protéines avec des anticorps fluorescents avant l’expansion, l’emplacement et l’identité des protéines ont pu être visualisés une fois le processus d’expansion terminé. Cependant, les anticorps généralement utilisés pour ce type de marquage ne peuvent pas facilement se faufiler à travers des tissus denses avant leur expansion.
Ainsi, pour cette étude, les auteurs ont conçu un protocole de ramollissement des tissus différent qui brise le tissu mais préserve les protéines dans l’échantillon. Une fois le tissu développé, les protéines peuvent être marquées avec des anticorps fluorescents disponibles dans le commerce. Les chercheurs peuvent alors effectuer plusieurs cycles d’imagerie, avec trois ou quatre protéines différentes marquées à chaque cycle. Ce marquage des protéines permet d’imager beaucoup plus de structures, car une fois le tissu étendu, les anticorps peuvent se faufiler et marquer les protéines qu’ils ne pouvaient pas atteindre auparavant.
« Nous ouvrons l’espace entre les protéines afin de pouvoir introduire des anticorps dans des espaces encombrés, ce que nous ne pourrions pas faire autrement », explique Valdes. « Nous avons vu que nous pouvions élargir les tissus, réduire les protéines et imager de très nombreuses protéines dans le même tissu en effectuant plusieurs cycles de coloration. »
En collaboration avec Deblina Sarkar, professeure adjointe au MIT, les chercheurs ont démontré une forme de ce « décombrement » en 2022 à l’aide de tissus de souris.
La nouvelle étude a abouti à une technique de réduction de la population à utiliser avec des échantillons de tissus cérébraux humains utilisés en milieu clinique pour le diagnostic pathologique et pour guider les décisions de traitement. Ces échantillons peuvent être plus difficiles à travailler car ils sont généralement inclus dans de la paraffine et traités avec d’autres produits chimiques qui doivent être décomposés avant que le tissu puisse se développer.
Dans cette étude, les chercheurs ont étiqueté jusqu’à 16 molécules différentes par échantillon de tissu. Les molécules ciblées comprennent des marqueurs pour diverses structures, notamment les axones et les synapses, ainsi que des marqueurs qui identifient des types de cellules tels que les astrocytes et les cellules qui forment des vaisseaux sanguins. Ils ont également marqué des molécules liées à l’agressivité tumorale et à la neurodégénérescence.
En utilisant cette approche, les chercheurs ont analysé des tissus cérébraux sains, ainsi que des échantillons provenant de patients atteints de deux types de gliomes : le glioblastome de haut grade, qui est la tumeur cérébrale primitive la plus agressive, avec un mauvais pronostic, et les gliomes de bas grade, qui sont considérés comme moins agressif.
« Nous voulions examiner les tumeurs cérébrales afin de mieux les comprendre à l’échelle nanométrique et, ce faisant, de pouvoir développer de meilleurs traitements et diagnostics à l’avenir. À ce stade, il s’agissait plutôt de développer un outil permettant de mieux les comprendre, car actuellement en neuro-oncologie, les gens n’ont pas fait grand-chose en termes d’imagerie à super-résolution », explique Valdes.
Un outil de diagnostic
Pour identifier les cellules tumorales agressives dans les gliomes étudiés, les chercheurs ont marqué la vimentine, une protéine présente dans les glioblastomes très agressifs. À leur grande surprise, ils ont trouvé beaucoup plus de cellules tumorales exprimant la vimentine dans les gliomes de bas grade que ce qui avait été observé avec toute autre méthode.
« Cela nous apprend quelque chose sur la biologie de ces tumeurs, en particulier sur le fait que certaines d’entre elles ont probablement un caractère plus agressif que ce que l’on pourrait soupçonner en appliquant des techniques de coloration standard », explique Valdes.
Lorsque les patients atteints de gliome subissent une intervention chirurgicale, des échantillons de tumeurs sont conservés et analysés par coloration immunohistochimique, qui peut révéler certains marqueurs d’agressivité, dont certains des marqueurs analysés dans cette étude.
« Ce sont des cancers du cerveau incurables, et ce type de découverte nous permettra de déterminer quelles molécules cancéreuses cibler afin de pouvoir concevoir de meilleurs traitements. Cela prouve également l’impact profond d’avoir des cliniciens comme nous au Brigham and Women’s qui interagissent avec des scientifiques fondamentaux tels qu’Ed Boyden au MIT pour découvrir de nouvelles technologies qui peuvent améliorer la vie des patients », déclare Chiocca.
Les chercheurs espèrent que leur technique de microscopie à expansion pourrait permettre aux médecins d’en apprendre beaucoup plus sur les tumeurs des patients, les aidant ainsi à déterminer le degré d’agressivité de la tumeur et à orienter les choix de traitement. Valdes prévoit maintenant de réaliser une étude plus vaste sur les types de tumeurs pour tenter d’établir des lignes directrices diagnostiques basées sur les traits tumoraux pouvant être révélés à l’aide de cette technique.
«Nous espérons que cela constituera un outil de diagnostic permettant de détecter les cellules marqueurs, les interactions, etc., ce que nous ne pouvions pas faire auparavant», dit-il. « C’est un outil pratique qui aidera le monde clinique de la neuro-oncologie et de la neuropathologie à examiner les maladies neurologiques à l’échelle nanométrique comme jamais auparavant, car fondamentalement, c’est un outil très simple à utiliser. »
Le laboratoire de Boyden prévoit également d’utiliser cette technique pour étudier d’autres aspects du fonctionnement cérébral, dans les tissus sains et malades.
« Il est important de pouvoir réaliser de la nanoimagerie, car la biologie concerne des éléments à l’échelle nanométrique – gènes, produits génétiques, biomolécules – et ils interagissent sur des distances nanométriques », explique Boyden. « Nous pouvons étudier toutes sortes d’interactions à l’échelle nanométrique, y compris les changements synaptiques, les interactions immunitaires et les changements qui se produisent au cours du cancer et du vieillissement. »
La recherche a été financée par K. Lisa Yang, le Howard Hughes Medical Institute, John Doerr, Open Philanthropy, la Fondation Bill et Melinda Gates, le Koch Institute Frontier Research Program via le Kathy and Curt Marble Cancer Research Fund, le Instituts nationaux de la santéet la Fondation pour la recherche et l’éducation en neurochirurgie.