L'humanité a un appétit insatiable pour l'ammoniac: cette substance est utilisée pour fabriquer des engrais, qui à leur tour sont utilisés dans l'agriculture la plus moderne. Jusqu'à présent, le processus Haber-Bosch a été la méthode de choix pour extraire l'azote de l'atmosphère apparemment inépuisable et la liant sous forme d'ammoniac. Cependant, cette méthode nécessite une quantité extrêmement importante de méthane gazeux et d'énergie.
Le professeur Nikolay Kornienko de l'Université de Bonn a découvert une alternative plus conviviale pour la production d'ammoniac à partir de sources d'énergie renouvelables. Les résultats sont publiés dans Communications de la nature.
Comme dans le jardin d'Eden, les céréales, les betteraves et les pommes de terre devraient germer aussi luxueusement que possible afin que les assiettes soient bien remplies. Ceci est assuré par la fertilisation régulière, en particulier avec l'azote. Une source de nutriments qui ne semble jamais se sécher. Au début du 20e siècle, Fritz Haber et Carl Bosch ont développé un processus qui extrait l'azote de l'air apparemment inépuisable. Cette réalisation leur a valu le prix Nobel de chimie en 1918.
En utilisant un catalyseur à base de fer, une pression très élevée et des températures allant jusqu'à 500 degrés Celsius, le processus Haber-Bosch lie l'azote de l'air à l'hydrogène, produisant de l'ammoniac. En passant, certaines plantes maîtrisent également l'art de la liaison de l'azote atmosphérique avec de minuscules bactéries dans leurs racines et la rendent disponible pour leur croissance. Cependant, les plantes vertes le font de manière neutre au climat, alors que les humains n'ont pas encore réussi à le faire.
« Le processus Haber-Bosch est extrêmement à forte intensité d'énergie », explique le professeur Nikolay Kornienko de l'Institut de chimie inorganique de l'Université de Bonn. La production d'ammoniac est basée principalement sur les combustibles fossiles, ce qui signifie que les émissions de gaz à effet de serre sont en conséquence élevées.
« Afin d'atteindre l'objectif d'une société durable et neutre, la recherche de processus alternatifs de synthèse d'ammoniac est une priorité », explique Kornienko, qui est également membre du domaine de recherche transdisciplinaire « l'affaire » à l'Université de Bonn.
Engrais azote du soleil et du vent
Méthodes alternatives? Ceux-ci ont été expérimentés depuis un certain temps. L'objectif est de remplacer la synthèse de l'ammoniac Haber-Bosch par un processus qui utilise des énergies renouvelables à partir de sources telles que le soleil et le vent. L'hydrogène requis ne proviendrait alors plus de méthane, mais serait obtenu directement à partir du fractionnement électrique de l'eau (H2O) en hydrogène (h2) et l'oxygène (o2).
Cela semble simple? Ce n'est pas le cas. Quiconque veut produire de l'ammoniac à grande échelle en utilisant l'énergie éolienne et solaire doit naviguer dans un certain nombre de pièges dans les voies de réaction chimique.
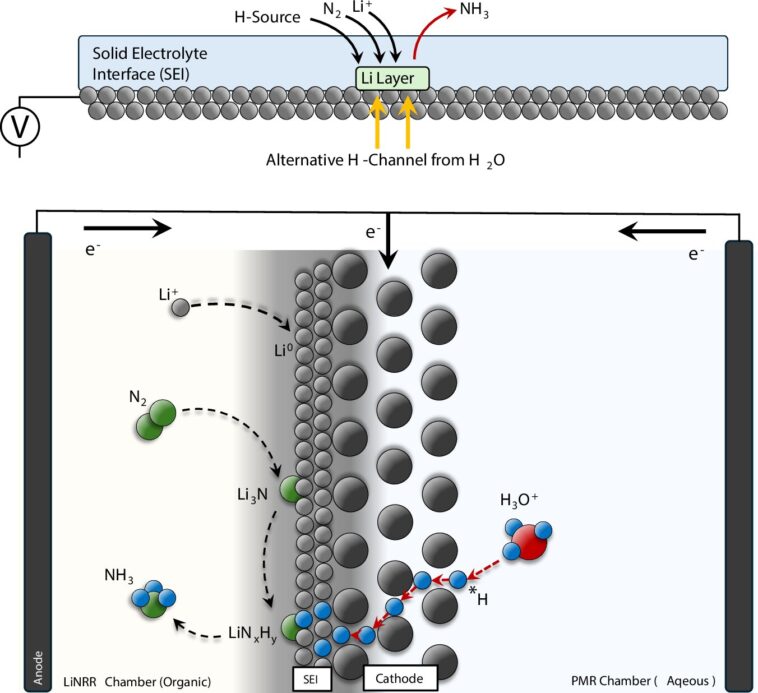
« La réaction de réduction de l'azote médiée par le lithium (LINRR) est considérée comme le moyen le plus robuste d'électrifier la synthèse de l'ammoniac », explique Hossein Bemana, l'auteur principal de l'étude. Dans ce système, les ions lithium (li+) sont réduits électrochimiquement à une couche de lithium métallique. Ce lithium métal peut ensuite réagir avec de l'azote gazeux (n2) pour former un composé au lithium-azote.
Si une source d'hydrogène est disponible, le composé au lithium-azote est converti en ammoniac (NH3) et les ions lithiums dissous. Ensuite, le processus recommence. C'est la théorie, au moins.
« Nous considérons généralement ce système comme un modèle pour le moment, car il y a plusieurs difficultés pratiques », explique Kornienko. Étant donné que la haute tension est nécessaire pour réduire les ions de lithium au lithium métallique, l'efficacité énergétique est limitée à environ 25%.
De plus, le système doit fonctionner dans un environnement sans air et eau, car le lithium métal est très réactif. Un autre défi est que, similaire aux batteries, une interphase d'électrolyte solide poreuse (SEI) se développe sur la couche de lithium. Cette couche doit permettre à l'azote gazeux et à l'hydrogène de passer en tant que réactifs au lithium.
La mauvaise chose est sacrifiée
Idéalement, l'hydrogène proviendrait directement du fractionnement de l'eau. Cependant, dans ce système, les alcools sont généralement utilisés comme source d'hydrogène. Dans certains cas, le solvant se décompose également puis sert de source d'hydrogène lui-même. « Cela rend le système peu pratique, car plusieurs molécules d'alcool ou de solvant doivent être sacrifiées pour produire de l'ammonium », explique le chimiste.
Cependant, les chercheurs ont trouvé un moyen d'extraire de l'hydrogène directement du fractionnement de l'eau et de le transférer dans de l'azote. Ils ont utilisé une feuille de palladium (PD) comme électrode et une membrane. « Le palladium peut servir de membrane car il permet aux atomes d'hydrogène de passer », rapporte Kornienko.
Dans l'expérience, la feuille de Pd a séparé un environnement de réaction anhydre, dans lequel les réactions de Linrr ont lieu, d'un environnement de réaction à base d'eau. « En fin de compte, nous avons pu extraire les atomes d'hydrogène électrochimiquement directement à partir de l'eau et les transférer dans le matériau réactif du lithium / lithium-azote pour produire de l'ammoniac », explique le chimiste.
Les chercheurs ont utilisé la spectroscopie infrarouge et la spectrométrie de masse pour vérifier que cela fonctionne vraiment comme prévu. Ils ont utilisé un isotope lourde d'hydrogène (deutérium = d) comme source d'eau et produit ND3 au lieu de NH3. Inversement, les chercheurs ont marqué toutes les molécules du compartiment Linrr avec D au lieu de H – comme désiré, NH3 a été produit dans ce cas et non nd3 comme avant.
Bemana et Kornienko ont déjà déposé une demande de brevet pour ce processus. L'équipe de recherche n'a utilisé que l'électricité pour que ses expériences produisent de l'ammoniac (NH3). Cependant, il reste encore un long chemin à parcourir avant que l'engrais azote souhaité puisse être produit économiquement à partir de sources d'énergie renouvelables. Pour y parvenir, les scientifiques devraient atteindre un rendement 1 000 fois supérieur à celui de leurs expériences actuelles. « Nous sommes encore aux premiers stades », explique le chimiste. « En général, la recherche doit être effectuée sur les taux de réaction et la sélectivité du système – le contrôle des électrons à la cible souhaitée. »