Le dichlorométhane du solvant, ou DCM, est couramment utilisé pour dépouiller la peinture et couper la graisse. C'est aussi ce que les générations d'étudiants en chimie ont utilisé pour dissoudre les comprimés d'analgésique dans un exercice de laboratoire conçu pour leur apprendre à isoler les composés dans un mélange.
Mais lorsque l'Agence américaine de protection de l'environnement a interdit la plupart des utilisations du DCM l'année dernière, Dartmouth et potentiellement des milliers d'autres écoles qui enseignent la chimie organique d'introduction ont été laissées en train de se déchaîner. Pour continuer à utiliser DCM, les écoles devraient surveiller de près son utilisation, ce qui les empêchant efficacement d'utiliser le solvant dans les laboratoires étudiants avec un grand nombre de chimistes débutants.
La solution conçue par le chercheur en visite Steve Wright '81 et la conférencière principale Cathy Welder ont maintenant attiré l'attention nationale: leur article détaillant des substitutions de solvants plus sûrs a récemment été classé parmi les plus lus dans le Journal of Chemical Education.
« Tout le monde a reconnu tout de suite que trouver un substitut était le seul véritable choix », explique Wright, assistant d'enseignement pour la chimie organique d'introduction.
Wright est retourné à Dartmouth l'été dernier après avoir pris sa retraite d'une longue carrière de chimiste chez Pfizer. Il avait proposé de faire du bénévolat en tant que TA pour la chimie organique d'introduction tout en créant un laboratoire avec son conseiller il y a longtemps, le professeur émérite Gordon Gribble.
Wright était la personne évidente pour attribuer la tâche de substitution DCM. Chez Pfizer, il avait aidé à évoluer des composés de médicaments prometteurs en éliminant ou en trouvant des alternatives plus sûres aux ingrédients toxiques ou dangereux. Travaillant avec l'équipe derrière le médicament anti-cuvide Paxlovid, il a réduit le nombre d'atomes impliqués dans le mécanisme d'action du médicament de 11 à deux.
Il a également eu un intérêt de longue date pour l'enseignement en chimie, en publiant des expériences assez faciles pour être faites à la maison avec des ingrédients ménagers courants comme le sel de table et la vitamine C. Il y a dix ans, il a créé un prix de chimie verte pour les majors de chimie senior à Dartmouth.
« Je suis devenu majeur dans les années 1970, lorsque l'énergie était rare, et tout coûte plus cher qu'auparavant », dit-il. « Je suis devenu apte à trouver des moyens de faire face et de compenser. En fin de compte, la chimie verte se résume à en faire plus avec moins de contributions, moins d'énergie, moins de déchets, moins de coûts et moins de problèmes. »
'Premier pingouin dans l'eau'
Wright a commencé à utiliser DCM dans les laboratoires de chimie en tant qu'élève du secondaire et a continué à le faire en tant que majeure en chimie et TA à Dartmouth. Les propriétés qui permettent à DCM de peler la peinture des murs en font également un solvant efficace pour dissoudre les composés et surveiller les réactions. Le DCM est non miscible, ce qui signifie qu'il ne se dissout pas dans l'eau, et il s'évapore facilement, simplifiant le processus de séparation et d'extraction des composés. Contrairement à de nombreux autres solvants, il ne prendra pas feu, ce qui en fait un choix attrayant dans les laboratoires d'enseignement.
Le DCM, cependant, est un cancérogène connu que l'EPA essaie de éliminer depuis des années. Bien que des alternatives plus sûres existent depuis un certain temps, les chimistes sont réticents à changer. « Il n'est pas trivial de changer les solvants pour les réactions », explique Welder. « Vous changez une chose, et vous devez souvent changer autre chose. »
« Personne ne veut tenter sa chance avec son travail, leur matériel, leur temps », explique Wright. « Personne ne veut être le premier pingouin de l'eau. »
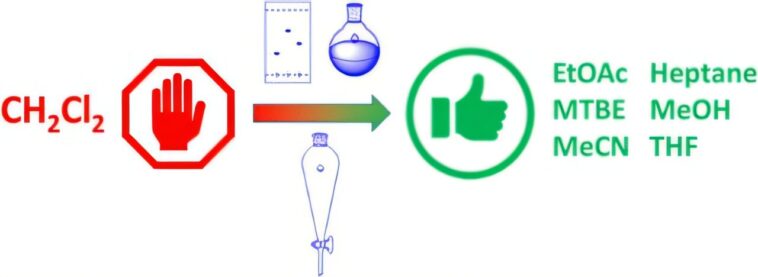
L'automne dernier, Wright a fait le pas à la demande de Welder, qu'il avait aidé dans le laboratoire au cours de l'été. Il s'est rapidement concentré sur l'acétate d'éthyle et le MTBE en tant que candidats de remplacement pour les analgésiques du cours et les laboratoires d'huile de Wintergreen. Pendant quatre jours, lui et Selder les ont testés dans le laboratoire des étudiants, sur l'équipement étudiant. Ils ont récemment partagé leurs résultats dans le Journal of Chemical Education.
Les étudiants en chimie organique de Dartmouth sont invités au premier semestre à utiliser un mélange de DCM et de lessive pour isoler et identifier les ingrédients actifs dans les comprimés de soulagement de la douleur en vente libre – à la fois de l'aspirine et un analgésique appelé phénacétine. Le terme suivant, ils convertissent l'aspirine en huile d'hiver, surveillant la réaction par chromatographie de couche mince et isolant l'huile d'hiver qu'ils ont synthétisé par extraction avec du DCM.
Alors que l'aspirine se transforme en salicylate de méthyle, la molécule qui donne à WinterGreen Gum son parfum boisé, les étudiants sont censés prendre note du composé intermédiaire, de l'acide salicylique, qui se trouve dans le bouleau et les saules et a été utilisé tout au long des âges pour soulager la douleur. Ingéré directement, l'acide salicylique provoque des maux d'estomac; L'aspirine a été inventée pour faciliter sa livraison.
« Dans les deux laboratoires, le choix de l'aspirine consiste principalement à engager les étudiants avec une molécule qu'ils connaissent déjà et ont vu sur les étagères des magasins », explique Wright.
Leurs expériences ont confirmé que l'acétate d'éthyle fonctionnait bien en tant que remplaçant pour DCM dans le laboratoire de analgésique. Ils ont également découvert que l'échange d'une base plus faible comme le bicarbonate de soude pour la lessive ralentissait suffisamment de réactions secondaires indésirables pour faciliter l'étape d'extraction de l'aspirine plus facile et plus efficace pour les étudiants.
Leurs expériences ont confirmé qu'un proche par rapport à l'acétate d'éthyle, le MTBE, un composé ajouté à l'essence pour augmenter sa teneur en oxygène et améliorer le kilométrage, a mieux fonctionné en tant que remplacement DCM dans le laboratoire WinterGreen.
Les nouveaux solvants ont été introduits dans le laboratoire d'enseignement cette année, et le plus grand ajustement pour les étudiants a été le temps nécessaire pour terminer le laboratoire. L'acétate d'éthyle et le MTBE prennent plus de temps à s'évaporer en raison de leurs points d'ébullition plus élevés. « Cela prend un peu plus de temps », explique Welder. « Ils doivent juste attendre leur tour pour évaporer le solvant sur un évaporateur rotatif. »
Solvants alternatifs et au-delà
Ailleurs à Dartmouth, les chercheurs tentent de minimiser l'utilisation du DCM tout en suivant les nouvelles directives de ventilation de l'EPA.
« Ce qui se passe dans Student Labs ne se traduit pas nécessairement par des laboratoires de recherche », explique le professeur de chimie de Dartmouth Ivan Aprihamian. « Néanmoins, chaque service de chimie du pays devra changer la façon dont ils dirigent leurs laboratoires organiques de premier cycle, et cet article les guidera tout au long du processus. »
Avec le papier DCM derrière lui, Wright s'est tourné vers le projet sur lequel il travaille avec Gribble – pour essayer de synthétiser les composés anticancéreux que l'on trouve dans certains types d'éponge de mer. Wright dit qu'il continuera également de documenter les substitutions DCM dans d'autres cas d'utilisation.
« Beaucoup de gens en parlent, mais personne n'a fait l'effort de montrer comment le faire », dit-il. « Sans le » montrant comment « , les gens continueront à utiliser le dichlorométhane. »