Une équipe de recherche internationale composée de scientifiques de Freie Universität Berlin et du Centre national français de recherche scientifique (CNRS) en collaboration avec Université de Lorraine à Metz, en France, a fait une percée importante dans la chimie des composés fluorants. À l'aide de simulations chimiques quantiques, ils ont pu prouver pour la première fois que de lourds atomes de fluor peuvent également «tunnel», ou en d'autres termes, se transforment entre deux états.
L'étude, «Observation expérimentale du tunneling de fluor mécanique quantique», a été publié dans la revue Communications de la nature. Il ouvre de nouvelles perspectives pour contrôler les réactions chimiques et mieux comprendre ce qui rend certains composés fluorés particulièrement stables ou réactifs.
Le fluor et les composés fluorés sont monnaie courante dans notre vie quotidienne. Les groupes fluorés améliorent l'absorption des médicaments dans le corps; Les composés fluorés rendent les batteries de téléphones portables plus efficaces et leur permettent de durer plus longtemps; et le fluorure dans le dentifrice empêche les cavités. Dans le même temps, les substances per- et polyfluoroalkyle (PFAS) posent un problème croissant pour la santé humaine et l'environnement.
Des recherches approfondies sur la science derrière les interactions produites par le fluor et ses composés sont nécessaires afin de saisir pleinement les effets positifs et négatifs du fluorure dans les composés. C'est l'un des objectifs du Collaborative Research Center (CRC) 1349 «interactions spécifiques au fluor».
Dans le cadre du CRC 1349, des équipes dirigées par le professeur Sebastian Hasenstab -riel et le professeur Beate Paulus de Freie Universität Berlin, avec le professeur Jean Christophe Tremblay du Centre national français pour la recherche scientifique (CNRS) en conjonction avec l'univers de Lorraine de Metz, en France, ont maintenant découvert une interaction rapide sur le fluor.
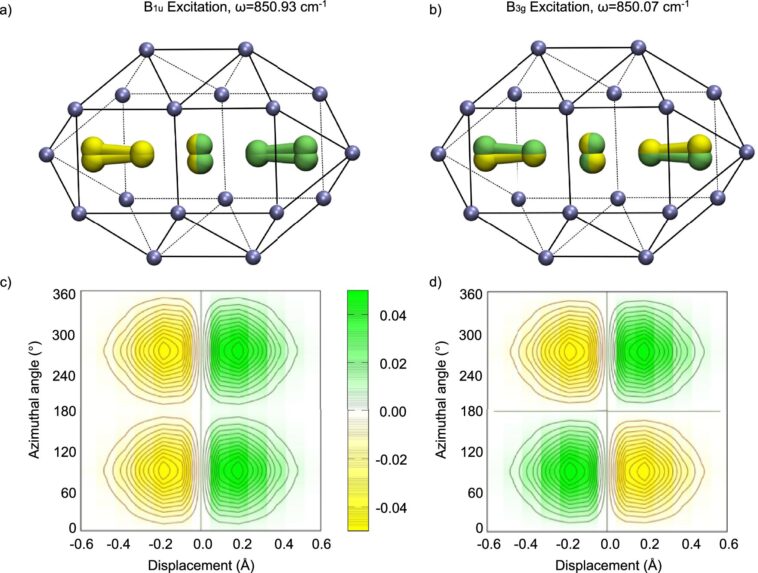
Il y a plus d'une décennie, Hasenstab -riel et son équipe ont réussi à capturer une molécule inhabituelle dans un cristal néon à -270 ° C. Cette molécule – un anion comprenant seulement cinq atomes de fluor étroitement emballés, hautement chargés et instables – ne devrait pas exister. Et pourtant, la molécule est restée étonnamment stable.
Afin de comprendre ce qui a maintenu cette molécule ensemble, les chercheurs de l'équipe de Paulus avec Tremblay ont effectué de vastes calculs et des simulations mécaniques quantiques. Ils sont tombés sur un effet surprenant qui avait jusqu'à présent été principalement observé pour l'hydrogène, qui est très léger, mais qui était considéré comme pratiquement impossible pour l'atome de fluor relativement lourd.
Les chercheurs ont pu prouver que même les atomes de fluor peuvent effectivement tunnel – IE, faire une molécule transformée spontanément entre deux états qui sont réellement séparés par une barrière d'énergie finie.
Ce type de tunnel a déjà été observé dans d'autres molécules d'éléments beaucoup plus légers tels que l'hydrogène et l'oxygène. Jusqu'à présent, les chercheurs supposaient que les atomes de fluor étaient trop lourds pour les tunnels, c'est pourquoi ils avaient tendance à parler d'un « mur de fluor » en ce qui concerne le tunneling.
Cependant, cette nouvelle étude semble signifier un changement de paradigme. La combinaison de conditions de liaison spéciales dans les molécules piégées dans un très petit espace semble permettre aux atomes plus lourds que l'oxygène au tunnel.
« Les résultats n'élargissent pas seulement notre compréhension des liaisons chimiques dans les composés fluorés », explique le Dr Carsten Müller de Freie Universität Berlin, premier auteur de l'étude. « Ils nous ont également fourni de nouveaux outils pour contrôler les réactions moléculaires de manière ciblée – que ce soit dans la recherche, la médecine ou la conception de nouvelles technologies. »