La microscopie optique est une technique clé pour comprendre les processus biologiques dynamiques dans les cellules, mais l'observation de ces dynamiques cellulaires à grande vitesse avec précision, à haute résolution spatiale, a longtemps été une tâche formidable.
Maintenant, dans un article publié dans Lumière: Science et applicationsdes chercheurs de l'Université d'Osaka, ainsi que des institutions collaboratrices, ont dévoilé une technique de microscopie cryo-optique qui prend un instantané à haute résolution et quantitativement précis à un point de cale précisément sélectionné dans l'activité cellulaire dynamique.
Capturer des événements cellulaires dynamiques rapides avec des détails spatiaux et une quantification a été un défi majeur, en raison d'un compromis fondamental entre la résolution temporelle et le «budget photon», c'est-à-dire combien de lumière peut être collectée pour l'image. Avec des photons limités et uniquement des images faibles et bruyantes, les caractéristiques importantes de l'espace et du temps se perdent dans le bruit.
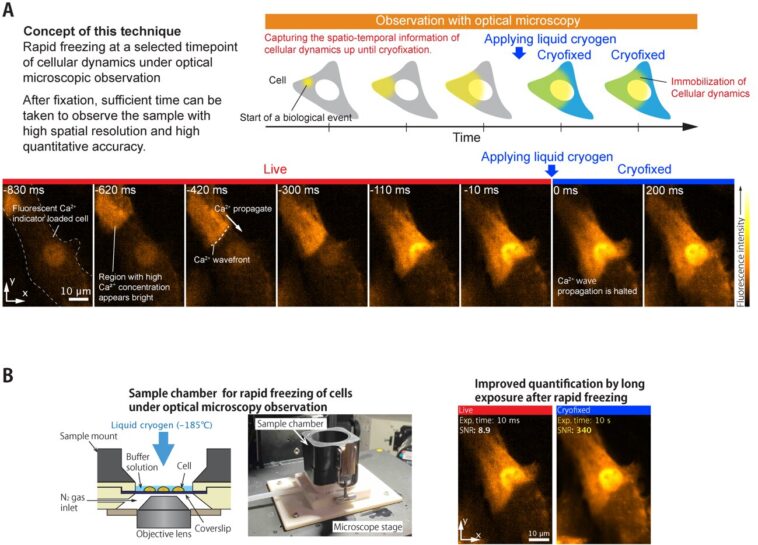
« Au lieu de chasser la vitesse dans l'imagerie, nous avons décidé de geler toute la scène », explique l'un des auteurs principaux, Kosuke Tsuji. « Nous avons développé une chambre spéciale de congélation d'échantillons pour combiner les avantages de la microscopie live et cryo-fixation.
Par exemple, l'équipe a gelé la propagation des ondes d'ions calcium dans les cellules du cœur vivant. L'onde congelée complexe détaillée a ensuite été observée en trois dimensions en utilisant une technique de super-résolution qui ne peut normalement pas observer la dynamique cellulaire rapide en raison de sa vitesse d'acquisition d'imagerie lente.
« Cette recherche a commencé par un changement audacieux en perspective: arrêter les processus cellulaires dynamiques pendant l'imagerie optique plutôt que de lutter pour les suivre en mouvement. Nous pensons que cela servira de technique fondamentale puissante, offrant de nouvelles idées à travers la science-vie et la recherche médicale », a déclaré l'auteur principal Katsumasa Fujita.
L'un des auteurs principaux, Masahito Yamanaka, ajoute: « Notre technique préserve à la fois les caractéristiques spatiales et temporelles des cellules vivantes avec une congélation instantanée, ce qui permet d'observer leurs états en détail. Bien que les cellules soient immobilisées, nous pouvons saisir l'occasion pour effectuer des mesures quantitatives très précises avec une variété d'outils de microscopie optique. »
Les chercheurs ont également démontré comment cette technique améliore la précision de la quantification. En congelant les cellules marquées avec une sonde de calcium-ion fluorescente, ils ont pu utiliser des temps d'exposition 1000 fois plus longs que pratiques dans l'imagerie des cellules vivantes, augmentant considérablement la précision de la mesure.

Pour capturer des événements biologiques transitoires à des moments définis avec précision, les chercheurs ont intégré un système d'injection de cryogène déclenché électriquement. Avec la stimulation de la lumière UV pour induire des ondes d'ions calcium, ce système a permis de congélation des ondes d'ions calcium à un moment spécifique après l'initiation de l'événement, avec une précision de 10 ms. Cela a permis à l'équipe d'arrêter des processus biologiques transitoires avec une précision temporelle sans précédent.
Enfin, l'équipe a réglé son attention sur la combinaison de différentes techniques d'imagerie, qui sont souvent difficiles à aligner dans le temps. Par la congélation presque instante des échantillons, plusieurs modalités d'imagerie peuvent désormais être appliquées séquentiellement sans se soucier de la non-concordance temporelle. Dans leur étude, l'équipe a combiné la microscopie Raman spontanée et la microscopie à fluorescence super-résolution sur les mêmes cellules cryofixées. Cela leur a permis de visualiser des informations cellulaires complexes à partir d'un certain nombre de perspectives au même moment.
Cette innovation ouvre de nouvelles voies pour observer les événements cellulaires transitoires rapides, offrant aux chercheurs un outil puissant pour explorer les mécanismes sous-jacents aux processus biologiques dynamiques.