Les scientifiques ont découvert le fonctionnement complexe d’un complexe de trois protéines dans la voie de signalisation de la réplication cellulaire, une avancée qui pourrait conduire à de nouveaux traitements contre le cancer plus efficaces. Cette recherche, utilisant des techniques d’imagerie avancées, améliore notre compréhension des interactions protéiques et ouvre de nouvelles voies pour le développement de médicaments. Crédit : Issues.fr.com
Déverrouiller les cibles des médicaments contre le cancer grâce à l’analyse des complexes protéiques
Trois protéines travaillent ensemble pour transmettre des signaux de division cellulaire, révélant ainsi de nouvelles cibles pour les médicaments anticancéreux.
La réplication cellulaire dans notre corps est déclenchée par une cascade de signaux moléculaires transmis entre protéines. Les composés qui bloquent ces signaux lorsqu’ils se déchaînent présentent un potentiel en tant que médicaments contre le cancer. Récemment, des scientifiques ont découvert les mécanismes moléculaires qui sont à la base d’une étape de la voie de transmission du signal qui nécessite la liaison de trois protéines.
Les connaissances détaillées sur ce complexe de trois protéines, déterminées grâce à des installations utilisant des rayons X synchrotron, ouvrent la voie à de nouvelles cibles pour les médicaments qui combattent certains types de cancer.
Progrès dans la compréhension des voies de signalisation du cancer
Certains médicaments anticancéreux prometteurs agissent en bloquant les protéines qui transmettent des signaux permettant aux cellules du corps de se répliquer. Cela ralentit la croissance des tumeurs. Cependant, les mécanismes de résistance aux médicaments permettent aux signaux de contourner le blocage. Les scientifiques travaillant sur les traitements contre le cancer doivent donc acquérir une compréhension au niveau moléculaire de la manière dont les protéines de signalisation interagissent les unes avec les autres.
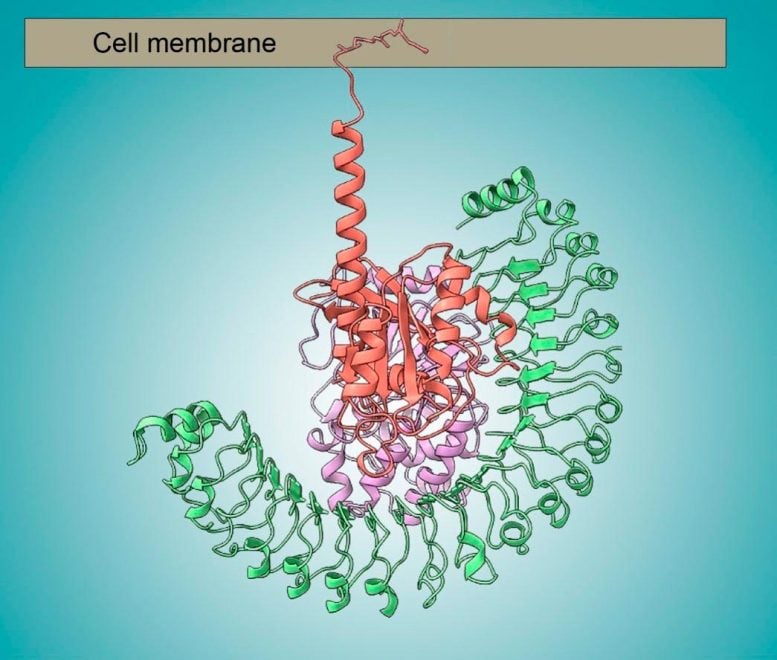
Lorsqu’il est réuni et ancré à l’intérieur d’une membrane cellulaire, ce complexe de trois protéines (représenté en saumon, violet et vert) joue un rôle clé dans la réplication cellulaire, ce qui en fait une cible potentielle pour le développement de médicaments anticancéreux. Crédit : Genentech et Laboratoire national Lawrence Berkeley
Dans cette étude, les scientifiques ont utilisé des expériences biochimiques combinées à des études sur la structure des protéines pour comprendre les détails d’une étape clé de la voie de signalisation. Les résultats donnent une image plus précise d’un processus qui restait flou malgré des décennies d’études. Cela pourrait conduire à de meilleurs médicaments contre les cancers du poumon, colorectal, pancréatique et autres.
Analyse approfondie d’un complexe protéique clé
Ce travail s’est concentré sur un maillon de la chaîne de signalisation de la réplication cellulaire, impliquant des protéines connues sous le nom de SHOC2, PPIC et RAS. Une fois assemblé, ce complexe de trois protéines devient chimiquement actif, permettant ainsi la prochaine étape de la cascade de signaux.
Pour obtenir des informations détaillées sur l’emplacement des atomes individuels dans les protéines, l’équipe de recherche a utilisé la microscopie électronique à Genentech et la cristallographie des protéines au laboratoire de rayonnement synchrotron de Stanford. Pour comprendre comment les trois protéines s’assemblent comme un puzzle, les chercheurs ont utilisé une technique appelée diffusion des rayons X aux petits angles (SAXS) à l’Advanced Light Source, une installation utilisateur du Bureau des sciences du Département de l’énergie du Laboratoire national Lawrence Berkeley.
Grâce aux données SAXS, les chercheurs ont pu capturer des instantanés du grand complexe protéique flexible sous sa forme native (suspendu dans une solution). Cela leur a permis de modéliser la flexibilité de SHOC2, qui agit comme un échafaudage pour les deux autres protéines.
Implications pour les futures thérapies contre le cancer
Avec d’autres données structurelles, études biochimiques et simulations informatiques, les travaux ont répondu à de nombreuses questions en suspens, notamment la manière dont les mutations liées à la maladie affectent l’assemblage du complexe et la manière dont les protéines travaillent collectivement pour activer la prochaine étape du processus de signalisation. De manière générale, les travaux ouvrent de nouvelles voies pour la découverte de nouvelles classes de médicaments anticancéreux ciblés.
Cette recherche a été réalisée à l’Advanced Light Source et au Stanford Synchrotron Radiation Laboratory, qui sont tous deux des installations utilisatrices du Bureau des sciences du Département de l’énergie (DOE). D’autres sources de financement comprenaient le programme du Bureau de la recherche scientifique, biologique et environnementale du DOE, le Instituts nationaux de la santéet Genentech.