Les chercheurs ont combiné la cryomicroscopie électronique et l’apprentissage profond pour étudier le processus complexe de dégradation des protéines, offrant ainsi un aperçu du fonctionnement d’une ubiquitine ligase clé et ouvrant la voie à la compréhension de maladies comme le cancer.
Des scientifiques du BioCenter de Vienne et de l’École de médecine de l’UNC ont révélé la chorégraphie intercellulaire qui régit la régulation des protéines, notamment la manière dont les protéines indésirables sont marquées pour être dégradées, un acteur important dans la santé et les maladies humaines.
Dans le paysage moléculaire complexe d’une cellule, l’orchestration des protéines exige un contrôle précis pour éviter les maladies. Alors que certaines protéines doivent être synthétisées à des moments précis, d’autres nécessitent une dégradation et un recyclage en temps opportun. La dégradation des protéines est un processus fondamental qui influence les activités cellulaires telles que le cycle cellulaire, la mort cellulaire ou la réponse immunitaire. Au cœur de ce processus se trouve le protéasome, centre de recyclage de la cellule. Le protéasome dégrade les protéines si elles portent une étiquette moléculaire formée par une chaîne de molécules d’ubiquitine. La tâche de fixer cette étiquette incombe à des enzymes appelées ubiquitine ligases.
Défis et techniques modernes
Ce processus, appelé polyubiquitination, a longtemps été difficile à étudier en raison de sa nature rapide et complexe. Pour relever ce défi, des scientifiques de l’Institut de recherche en biologie moléculaire (IMP) de Vienne, de l’École de médecine de l’Université de Caroline du Nord et de leurs collaborateurs ont utilisé une combinaison de techniques, intégrant la microscopie cryoélectronique (cryo-EM) avec des techniques de pointe. algorithmes d’apprentissage profond.
David Haselbach, PhD, chef de groupe à l’IMP, a déclaré : « Notre objectif était de capturer la polyubiquitination étape par étape grâce à des études cryo-EM résolues dans le temps. Cette méthode nous a permis de visualiser et de disséquer les interactions moléculaires complexes qui ont lieu au cours de ce processus, comme dans un film en stop motion.
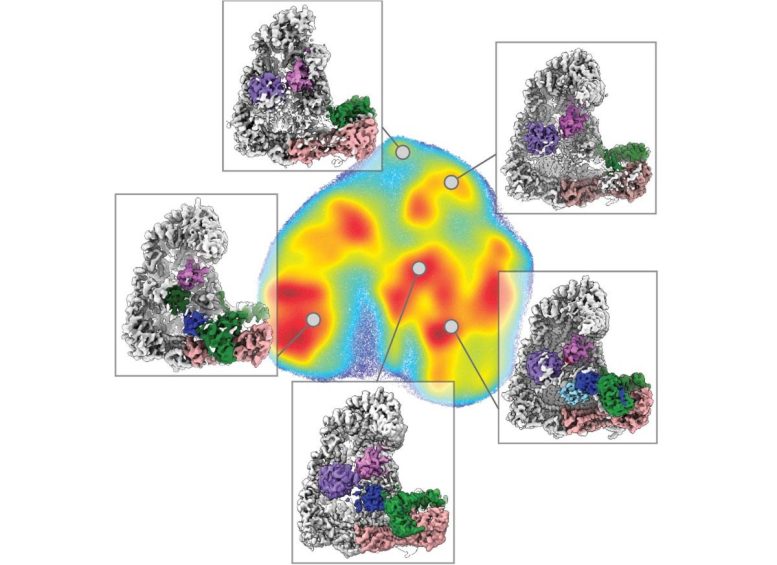
Cartes de la dynamique structurelle de l’ubiquitination dépendante d’APC/C, créées à l’aide de réseaux de neurones. Crédit : Brown, Haselbach et al.
Un timelapse biochimique
L’étude, publiée dans la revue Nature Biologie structurale et moléculaire, explore les mouvements du complexe/cyclosome favorisant l’anaphase (APC/C), une ubiquitine ligase qui pilote le cycle cellulaire. Les mécanismes derrière l’attachement par APC/C d’un signal d’ubiquitine restaient un casse-tête non résolu. Haselbach et Nicholas Brown, PhD, professeur agrégé de pharmacologie à la faculté de médecine de l’Université de Caroline du Nord, sont co-auteurs principaux.
« Nous avions une solide compréhension de la structure fondamentale d’APC/C, une condition préalable à la cryo-EM résolue dans le temps », a déclaré la première auteure Tatyana Bodrug, PhD, chercheuse postdoctorale en pharmacologie à l’UNC-Chapel Hill. « Nous comprenons désormais bien mieux sa fonction, à chaque étape du processus. »
Les ligases d’ubiquitine effectuent de nombreuses tâches, notamment le recrutement de différents substrats, l’interaction avec d’autres enzymes et la formation de différents types de signaux d’ubiquitine. Les scientifiques ont visualisé les interactions entre les protéines liées à l’ubiquitine et l’APC/C et ses co-enzymes. Ils ont reconstruit les mouvements subis par APC/C lors de la polyubiquitination en utilisant une forme d’apprentissage profond appelée réseaux de neurones. Il s’agissait d’une première dans la recherche sur la dégradation des protéines.
Collaboration et orientations futures
L’APC/C fait partie de la grande famille des ubiquitine ligases (plus de 600 membres) qui n’ont pas encore été caractérisées de cette manière. Les efforts mondiaux continueront de repousser les limites de ce domaine.
« La collaboration avec plusieurs autres équipes a été la clé du succès de notre travail », a déclaré Brown, également membre du UNC Lineberger Comprehensive Cancer Center. « À université de Princeton, les contributions d’Ellen Zhong aux logiciels et à la programmation ont été essentielles à la découverte de nouvelles connaissances sur le mécanisme APC/C. La validation ultérieure de ces résultats a nécessité l’aide de plusieurs autres groupes dirigés par les Drs Harrison, Steimel, Hahn, Emanuele et Zhang. « Un effort d’équipe a été crucial pour pousser nos recherches jusqu’au bout. »
L’importance de cette recherche s’étend au-delà de son impact immédiat, ouvrant la voie à de futures explorations de la régulation des ligases, promettant à terme des connaissances plus approfondies sur les mécanismes qui sous-tendent le métabolisme des protéines, importants pour la santé humaine et les maladies, telles que de nombreuses formes de cancer.