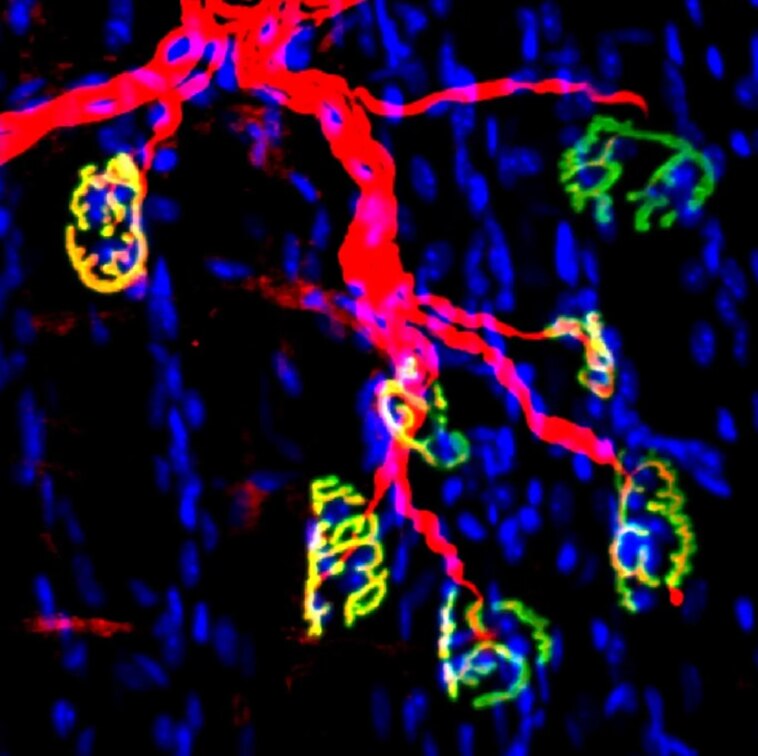
Jonctions neuromusculaires de souris : le nerf moteur et les synapses sont en rouge ; les récepteurs de l’acétylcholine des fibres musculaires sont en vert. Crédit : Laboratoire Blau, École de médecine de l’Université de Stanford
Des scientifiques de la faculté de médecine de l’université Stanford et de Sanford Burnham Prebys ont démontré une nouvelle façon d’accélérer la guérison d’une lésion nerveuse périphérique. Ils y sont parvenus en ciblant une enzyme considérée comme responsable de la fonte musculaire liée au vieillissement.
Comprendre le système nerveux périphérique
Les dommages au système nerveux périphérique (les nerfs qui forment le réseau de communication entre le cerveau, la moelle épinière et le corps) sont débilitants ; l’efficacité de la physiothérapie en tant que traitement est limitée. Que ce soit à cause d’un traumatisme, d’une maladie ou du vieillissement, la fonction nerveuse diminue et/ou est perdue, entraînant une diminution de la force, voire une paralysie.
Découvertes récentes
Dans la nouvelle étude, récemment publiée dans la revue Médecine translationnelle scientifique et co-écrit par Helen M. Blau, Ph.D., professeur de la Fondation Donald E. et Delia B. Baxter à la faculté de médecine de l’Université de Stanford, et Yu Xin Wang, Ph.D., professeur adjoint en développement, vieillissement et du programme de régénération à Sanford Burnham Prebys, l’équipe de recherche a découvert qu’une enzyme associée au vieillissement est déclenchée par la perte d’innervation.
L’inhibition de cette enzyme après une lésion nerveuse chez un modèle murin avec un inhibiteur à petite molécule a favorisé la régénération du nerf moteur et la formation de synapses neuromusculaires, ce qui a entraîné une récupération accélérée de la force.
« Nos données suggèrent que l’inhibition de la fonction de cette enzyme particulière, appelée 15-hydroxyprostaglandine déshydrogénase ou 15-PGDH, avec une petite molécule, a stimulé un composé naturel (prostaglandine E2 ou PGE2) dans les tissus musculaires qui aide à restaurer la connectivité, la fonction et la fonction nerveuse. force », a déclaré Wang.
Effets de la dénervation
Lorsque les muscles squelettiques perdent leur fonction nerveuse, phénomène appelé dénervation, ils s’atrophient et s’affaiblissent. La dénervation peut résulter d’un traumatisme physique, tel qu’une lésion des nerfs reliant les muscles à la moelle épinière, ou d’une fonte neuromusculaire héréditaire, telle que la sclérose latérale amyotrophique. L’âge avancé peut également entraîner une fonte musculaire grave appelée sarcopénie.
La dénervation musculaire et ses conséquences affectent jusqu’à environ 5 % de la population américaine (environ 17 millions de personnes) et entraînent des coûts annuels de santé nationaux estimés à 380 milliards de dollars.
Importance de la PGE2 et rôle du 15-PGDH
Wang faisait partie de l’équipe de Blau à l’Université de Stanford, qui avait montré dans des recherches antérieures que la PGE2 dans les tissus musculaires est nécessaire à la prolifération des cellules souches musculaires et à la régénération et à la réparation efficaces des muscles après une blessure.
Les chercheurs ont également découvert que la 15-PGDH dégrade la PGE2 et que l’enzyme s’accumule avec l’âge. Ils ont surnommé la 15-PGDH un gérozyme, une enzyme qui détermine la fonte musculaire et qui augmente avec le vieillissement.
« Nous nous sommes demandés pourquoi cette enzyme s’active avec l’âge si elle a un impact aussi négatif sur la masse et la force musculaires », a déclaré Wang.
Le nouveau travail consistait à étudier de jeunes souris en utilisant des méthodes chirurgicales pour modéliser les blessures du nerf sciatique. Les niveaux de 15-PGDH ont augmenté dans les muscles dénervés, mais l’inhibition pharmacologique de la 15-PGDH a favorisé la croissance ultérieure des axones moteurs, la connectivité neuromusculaire et une récupération plus rapide.
Dans des études sur des tissus humains, les chercheurs ont détecté des agrégats de 15-PGDH dans des biopsies provenant d’un large éventail de maladies neuromusculaires humaines, ce qui suggère que l’inhibition de cette enzyme pourrait être bénéfique.
« La restauration de la connectivité neuromusculaire est une étape cruciale dans le traitement de ces troubles débilitants. Cette nouvelle approche est intéressante car le traitement signale au nerf de repousser », a déclaré Wang. « C’est pourquoi cela a un effet si profond sur les muscles et la force. »
Parmi les autres auteurs de l’étude figurent Mohsen A. Bakooshli, Elena Monti, Shiqi Su, Peggy Kraft, Minas Nalbandian, Ludmila Alexandrova, Joshua R. Wheeler et Hannes Vogel, tous de l’Université de Stanford.
Cette étude a été soutenue par le Instituts nationaux de la santé Subvention pour instrumentation partagée (S100D026962) ; les Instituts canadiens de la santé (MFE-152457); Subvention pilote de recherche translationnelle et de médecine appliquée de Stanford ; National Institutes of Health (K99NS120278, R00NS120278, R01-AG020961, R01-AG069858, R01-G009674), doyen de la recherche de Stanford — programme de subventions de démarrage SUMS ; Fondation Donald E. et Delia B. Baxter ; la Fondation Li Ka Shing ; voie Lactée Fondation de recherche (MWRF-21664), Institut californien de médecine régénérative (DISC2-10604).