Des recherches récentes révèlent qu’une seule mutation dans une structure protéique critique, le complexe synaptonémique, peut provoquer l’infertilité masculine. Cette découverte, réalisée grâce à l’édition génétique chez la souris, ouvre de nouvelles possibilités pour comprendre et traiter l’infertilité masculine.
Les scientifiques du Stowers Institute collaborent pour découvrir une cause sous-jacente à l’infertilité masculine.
L’infertilité touche d’innombrables couples dans le monde et, dans la moitié de ces cas, le problème vient du partenaire masculin. Plus précisément, environ 10 % de ces hommes sont confrontés au défi de produire peu ou pas de spermatozoïdes. Des recherches récentes menées conjointement par le Stowers Institute for Medical Research et le Wellcome Center for Cell Biology de l’Université d’Édimbourg donnent un aperçu des dysfonctionnements survenant au cours du développement des spermatozoïdes. Cette recherche ouvre la porte à de nouvelles hypothèses concernant les méthodes de traitement potentielles.
« Une cause importante de l’infertilité chez les hommes est qu’ils ne peuvent tout simplement pas produire de spermatozoïdes », a déclaré Scott Hawley, Ph.D., chercheur chez Stowers. « Si vous savez exactement ce qui ne va pas, des technologies émergent actuellement qui pourraient vous permettre de résoudre le problème. »
L’étude récemment publiée dans Avancées scientifiques du Hawley Lab et du Wellcome Center, Owen Davies, Ph.D., chercheur, peut aider à expliquer pourquoi certains hommes ne produisent pas suffisamment de spermatozoïdes pour féconder un ovule. Dans la plupart des cas de reproduction sexuée espèces, y compris les humains, une structure protéique critique ressemblant à un pont en forme de treillis doit être construite correctement pour produire des spermatozoïdes et des ovules. L’équipe dirigée par Katherine Billmyre, Ph.D., ancienne associée de recherche postdoctorale, a découvert que chez la souris, la modification d’un point unique et très spécifique de ce pont provoquait son effondrement, conduisant à l’infertilité et fournissant ainsi un aperçu de l’infertilité humaine chez les hommes en raison de problèmes similaires avec la méiose.
Une vidéo expliquant les résultats. Crédit : Institut Stowers pour la recherche médicale
Le rôle de la méiose dans la santé reproductive
La méiose, le processus de division cellulaire donnant naissance aux spermatozoïdes et aux ovules, comporte plusieurs étapes, dont la formation d’une grande structure protéique appelée complexe synaptonémique. Comme un pont, le complexe maintient les paires de chromosomes en place, permettant ainsi les échanges génétiques nécessaires, essentiels à la séparation correcte des chromosomes en spermatozoïdes et en ovules.
« Les défauts de la méiose contribuent de manière significative à l’infertilité », a déclaré Billmyre. « Pour comprendre comment les chromosomes se séparent correctement en cellules reproductrices, nous nous intéressons vraiment à ce qui se passe juste avant, lorsque le complexe synaptonémique se forme entre eux. »
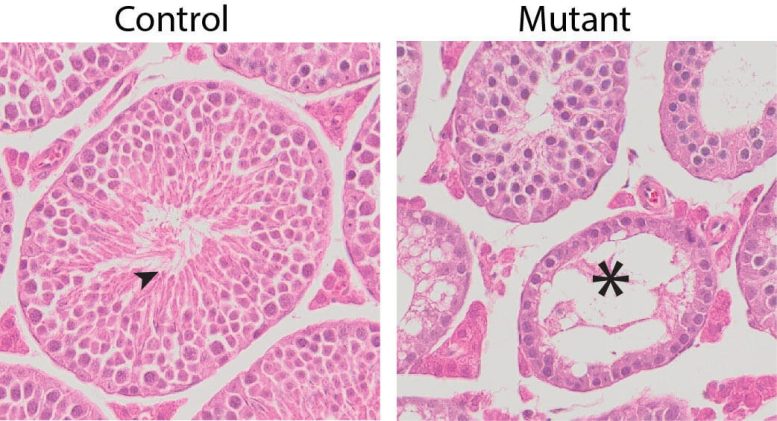
Images de microscopie montrant des tubules séminifères normaux dans des testicules témoins avec des spermatozoïdes matures (flèche noire : à gauche) mais des tubules séminifères vides plus petits dans des testicules hébergeant une mutation ponctuelle de la protéine complexe synaptonémique (astérisque noir : à droite). Crédit : Institut Stowers pour la recherche médicale
Des études antérieures ont examiné de nombreuses protéines composant le complexe synaptonémique, comment elles interagissent les unes avec les autres, et ont identifié diverses mutations liées à l’infertilité masculine. La protéine étudiée par les chercheurs dans cette étude forme le réseau du pont proverbial, qui comporte une section trouvée chez les humains, les souris et la plupart des autres espèces. vertébrés ce qui suggère qu’il est essentiel pour l’assemblage. La modélisation de différentes mutations dans une région potentiellement cruciale de la protéine humaine a permis à l’équipe de prédire laquelle d’entre elles pourrait perturber la fonction de la protéine.
Les auteurs ont utilisé une technique précise d’édition génétique pour effectuer des mutations dans une protéine complexe synaptonémique clé chez la souris, ce qui a permis aux chercheurs, pour la première fois, de tester la fonction de régions clés de la protéine chez des animaux vivants. Une seule mutation, prédite par les expériences de modélisation, a été vérifiée comme étant responsable de l’infertilité chez la souris.
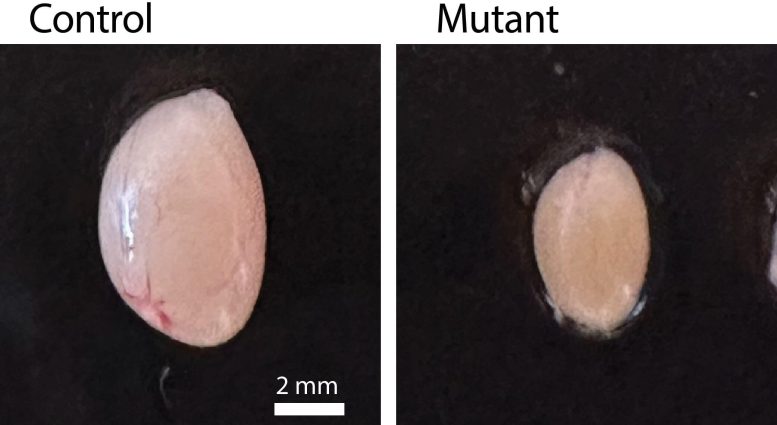
Testicules représentatifs de souris témoins âgées de 9 semaines (à gauche) et de souris présentant une mutation ponctuelle dans une protéine complexe synaptonémique (à droite). Crédit : Institut Stowers pour la recherche médicale
« Nous parlons ici d’une intervention chirurgicale ponctuelle », a déclaré Hawley. « Nous nous sommes concentrés sur une toute petite région d’une protéine dans cette gigantesque structure dont nous étions presque sûrs qu’elle pourrait être une cause importante d’infertilité. »
Implications pour la santé humaine
Les souris ont longtemps été utilisées comme modèles pour les maladies humaines. D’après les expériences de modélisation utilisant des séquences de protéines humaines, ainsi que la conservation élevée de cette structure protéique d’une espèce à l’autre, la molécule précise qui a causé l’infertilité chez la souris fonctionne probablement de la même manière chez l’homme.
« Ce qui me passionne vraiment, c’est que nos recherches peuvent nous aider à comprendre ce processus vraiment fondamental qui est nécessaire à la vie », a déclaré Billmyre.
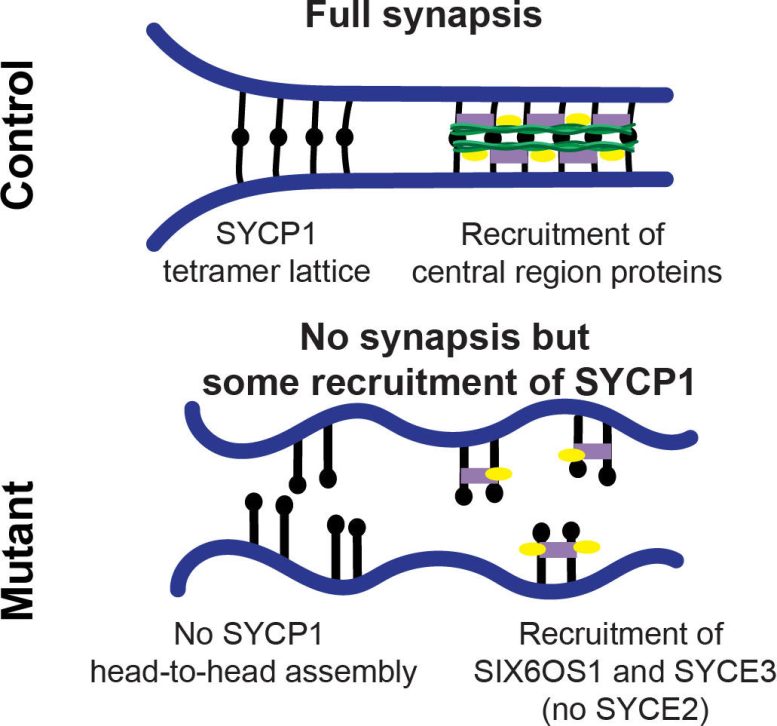
Modèle du complexe synaptonémique chez la souris témoin et mutante. La protéine étudiée par l’équipe (SYCP1) se forme normalement et toutes les protéines supplémentaires nécessaires sont recrutées. Chez le mutant, SYCP1 se localise sur les axes chromosomiques mais ne parvient pas à former la structure en forme de pont (interactions tête-à-tête), et les protéines supplémentaires qui aident à maintenir le pont intact sont manquantes ou mal organisées. Crédit : Institut Stowers pour la recherche médicale
Pour Hawley, cette recherche est une véritable représentation de la polyvalence de l’Institut. Le laboratoire de Hawley mène généralement des recherches sur les mouches des fruits, mais la protéine découverte dans cette étude n’était pas présente dans les mouches des fruits et a nécessité la poursuite d’un organisme de recherche différent. Grâce aux ressources et aux centres technologiques de l’Institut, il a été possible de faire pivoter et de tester rapidement la nouvelle hypothèse d’infertilité chez la souris.
« Je ne peux pas imaginer un autre endroit où cela pourrait se produire », a déclaré Hawley. « Je pense que c’est un exemple étonnant de la manière dont l’engagement du Stowers Institute en faveur de la découverte peut produire d’importants résultats, permettant ainsi des progrès importants dans la compréhension. »
Les autres auteurs incluent Emily A. Kesler, Dai Tsuchiya, Ph.D., Timothy J. Corbin, Kyle Weaver, Andrea Moran, Zulin Yu, Ph.D., Lane Adams, Kym Delventhal, Michael Durnin, Ph.D. et Owen Richard Davies, Ph.D.
Ce travail a été financé par le Wellcome Center for Cell Biology (prix : 203149), la Wellcome Senior Research Fellowship (prix : 219413/Z/19/Z) et par le soutien institutionnel du Stowers Institute for Medical Research.