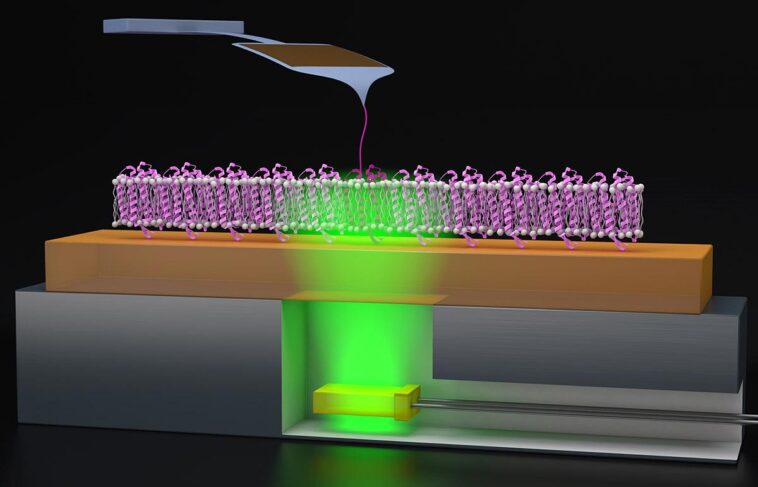
Schéma du dispositif expérimental (pas à l'échelle) : Photoactivation d'une seule molécule de bR. Crédit
Groupe Steven Burrows/Perkins
Les chercheurs ont fait progresser la compréhension de la dynamique des protéines membranaires en étudiant la bactériorhodopsine (bR) grâce à des méthodes innovantes combinant la microscopie à force atomique et les déclencheurs lumineux.
Lorsqu’il s’agit de développement de médicaments, les protéines membranaires jouent un rôle crucial, avec environ 50 % des médicaments ciblant ces molécules. Comprendre la fonction de ces protéines membranaires, qui se connectent aux membranes des cellules, est important pour concevoir la prochaine gamme de médicaments puissants. Pour ce faire, les scientifiques étudient des protéines modèles, telles que la bactériorhodopsine (bR), qui, lorsqu’elles sont déclenchées par la lumière, pompent des protons à travers la membrane des cellules.
Alors que bR est étudié depuis un demi-siècle, les physiciens ont récemment développé des techniques pour observer ses mécanismes de repliement et son énergie dans l'environnement natif de la membrane bicouche lipidique de la cellule. Dans une nouvelle étude publiée par Actes de l'Académie nationale des sciences (PNAS)Thomas Perkins, membre du JILA et du NIST, et son équipe ont avancé ces méthodes en combinant la microscopie à force atomique (AFM), un outil de mesure conventionnel des nanosciences, avec des déclencheurs de lumière précisément synchronisés pour étudier la fonctionnalité de la fonction des protéines en temps réel.
« L'énergie des protéines membranaires est difficile à étudier et n'est donc pas bien comprise », a expliqué Perkins. « En utilisant l'AFM et d'autres méthodes, nous pouvons créer des moyens d'approfondir cette question. » Armés d'une meilleure compréhension de l'énergie de ces protéines, les chimistes peuvent concevoir des médicaments plus puissants contre des symptômes et des maladies spécifiques causés par un dysfonctionnement des protéines.
Mesurer la dynamique des protéines en millisecondes
Bien que bR soit une protéine microscopique, elle peut être vue à l’œil nu, et même sur les images satellite, lorsque les micro-organismes archéens fleurissent, ils en laissent de grandes quantités sous forme de résidus dans les étangs d’eau salée. « Les étangs se remplissent de ce qu'on appelle Halobacterium salinarum, l'organisme parent de la bactériorhodopsine », a expliqué Perkins. « Ces étangs sont utilisés pour récolter le sel, et comme ils sont chauds et salés, les bactéries adorent s'y développer. »
Au niveau microscopique, bR travaille avec d'autres protéines membranaires pour produire de l'énergie pour la cellule en créant un gradient de protons d'un côté de la membrane cellulaire, qui fait passer le proton de l'autre côté de la membrane. Pour ce faire, bR plie et déplie ses hélices selon des formes spécifiques pour contrôler le nombre de protons qui traversent la membrane. Au cours de ce processus, la migration des protons produit de l'énergie chimique sous forme d'adénosine-tri-phosphate (ATP).
Pour Perkins et son co-auteur David Jacobson (ancien chercheur postdoctoral au JILA et maintenant professeur adjoint à l'Université de Clemson), bR a présenté une opportunité de concevoir une nouvelle méthode expérimentale pour étudier l'énergétique fonctionnelle en temps réel. Pour étudier des protéines comme bR, Jacobson et Perkins, utilisez l'AFM, qui agit comme un petit doigt pour tirer doucement sur la protéine, ce qui aide l'AFM à sentir la surface de la protéine, à cartographier sa structure et à mieux comprendre comment la protéine se replie. .
Étant donné que les processus de pliage du bR sont déclenchés par la lumière, Perkins et Jacobson ont ajouté un élément d'éclairage à la procédure AFM. « Nous avons eu cette idée intelligente de coller des LED vertes ultra fines, qui déclenchent la bactériorhodopsine, sur une rondelle métallique que nous pouvons attacher à l'AFM », a expliqué Perkins. « Ces LED vertes sont également bon marché, entre 1,00 $ pièce ou 1,50 $ pièce. Comparé à notre porte-à-faux AFM, qui coûte environ 80 dollars pièce, jeter une LED à 1,50 dollars ne nous inquiète guère.
Avec ce module complémentaire peu coûteux à leur AFM, Perkins et Jacobson pourraient inciter le bR à se plier et à se déplier avec une précision de la milliseconde. Après avoir collecté leurs données, les chercheurs ont constaté que la protéine se repliait correctement dans 60 % des cas, permettant ainsi aux protons de traverser la membrane.
Pour vérifier l’énergie et la fonction en temps réel du repliement de la protéine, les scientifiques ont muté la protéine bR pour qu’elle reste toujours à l’état « ouvert » ou déplié. Grâce à leur nouvelle configuration expérimentale, ils ont pu reproduire des résultats similaires à ceux qu’ils avaient observés auparavant dans la phase « ouverte » du photocycle bR.
« En biologie, vous pouvez voir quelque chose, mais vous devez vous demander : est-ce que je vois ce que je pense voir ? » » dit Perkins. « Ainsi, en effectuant une mutation et en constatant l'effet auquel nous nous attendions, nous avons accru la confiance dans le fait que nous étudions réellement le processus que nous pensons étudier. »
Le mystère de la protéine mal repliée
Alors que Perkins et Jacobson ont observé un repliement correct dans 60 % des cas, les 40 % restants les ont surpris, car la protéine s'est mal repliée mais pouvait quand même pomper un proton à travers la membrane. « Le mauvais pliage est en train de se stabiliser », a ajouté Perkins. « Et c'était vraiment surprenant. » Dans de nombreux cas, un mauvais repliement des protéines n’entraîne pas de stabilisation.
En raison de la stabilisation énergétique, Perkins et Jacobson ont émis l'hypothèse que les hélices structurelles du bR ne se séparaient pas correctement pour fournir un tunnel complètement ouvert au proton, même s'il se tortillait toujours, un processus difficile à détecter avec l'imagerie AFM.
En essayant de mieux comprendre les mécanismes sous-jacents du mauvais repliement, Perkins et Jacobson ont abaissé la force exercée sur le test de traction AFM à zéro pour voir si cela permettrait à la protéine de se replier correctement. Cependant, les résultats sont restés les mêmes : 40 % des cas ont abouti à un mauvais pliage.
Ces résultats, avec le même nombre d’erreurs de pliage, ont intrigué les chercheurs. Bien que Perkins et Jacobson n'aient pas pu identifier la cause de ces cas mal repliés, ils espèrent enquêter plus en profondeur. Ils souhaitent désormais voir ce que le reste de la communauté biophysique pense de ces résultats.
« Il pourrait y avoir des effets plus subtils, ou peut-être de nouvelles données scientifiques », a ajouté Perkins. « Il se pourrait qu'il existe un chemin que les gens n'avaient peut-être pas pu voir auparavant. »