Des chercheurs de l’Institut Salk ont découvert que les inhibiteurs d’HDAC sont efficaces dans le traitement du cancer du pancréas en ciblant les fibroblastes, les cellules responsables du tissu cicatriciel dense autour des tumeurs. Cette approche ralentit la croissance tumorale et réduit l’activation des fibroblastes, offrant ainsi une nouvelle stratégie dans la lutte contre ce cancer difficile à traiter. Crédit : Issues.fr.com
Les chercheurs de Salk ont découvert qu’une thérapie anticancéreuse peut empêcher l’activation des fibroblastes, des cellules qui forment généralement des barrières protectrices autour des tumeurs pancréatiques.
Le cancer du pancréas est l’un des cancers les plus mortels : seul un patient sur huit environ survit cinq ans après le diagnostic. Ces statistiques lamentables sont en partie dues à la paroi épaisse et presque impénétrable de fibrose, ou tissu cicatriciel, qui entoure la plupart des tumeurs pancréatiques et rend difficile l’accès des médicaments aux cellules cancéreuses et leur destruction.
Percée dans le traitement du cancer du pancréas
Aujourd’hui, des chercheurs de l’Institut Salk ont fait une découverte importante. Ils ont découvert que les inhibiteurs de HDAC, un type de médicament anticancéreux, peuvent traiter efficacement le cancer du pancréas en modifiant l’activation des fibroblastes. Les fibroblastes créent la barrière de tissu cicatriciel autour des tumeurs.
La nouvelle recherche a été publiée dans Communications naturelles le 6 décembre 2023.
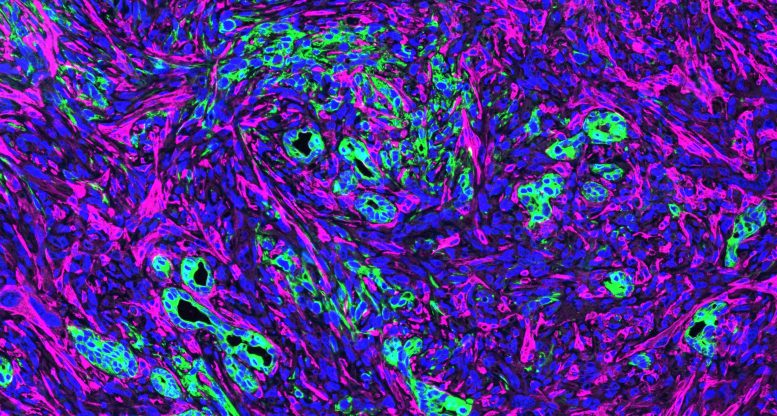
L’abondance de fibroblastes associés au cancer (magenta) dans le microenvironnement avec des cellules cancéreuses pancréatiques (vert). Crédit : Institut Salk
« Ces médicaments s’avèrent agir à la fois sur la tumeur elle-même ainsi que sur le tissu fibreux qui l’entoure. Cela pourrait être un moyen très efficace de traiter les cancers du pancréas, qui sont généralement très difficiles à atteindre », déclare le professeur Ronald Evans, directeur du laboratoire d’expression génique de Salk et de la chaire March of Dimes en biologie moléculaire et développementale.
Rôle des fibroblastes dans le cancer du pancréas
En réponse à une nouvelle tumeur pancréatique, le pancréas active généralement les fibroblastes, les cellules conjonctives qui soutiennent la structure de la plupart des organes. Lorsqu’ils passent d’un état de repos à un état actif, les fibroblastes construisent une épaisse couche de tissu cicatriciel autour du cancer. Bien que ce mécanisme de protection normal puisse aider à isoler un cancer et à empêcher sa propagation, les fibroblastes produisent également des molécules de signalisation dont la tumeur elle-même profite pour se développer.
« Dans le contexte de la plupart des cancers du pancréas, les fibroblastes agissent à la fois comme de bons et de mauvais joueurs », explique Michael Downes, scientifique principal et co-auteur correspondant de l’article. « C’est une arme à double tranchant. »
Impact des inhibiteurs de HDAC sur les fibroblastes
Dans la nouvelle recherche, l’équipe a étudié l’effet sur les fibroblastes d’une classe expérimentale de médicaments anticancéreux connus sous le nom d’inhibiteurs de l’histone désacétylase (HDAC). Les HDAC modifient la structure tridimensionnelle de ADN à l’intérieur des cellules, ce qui rend certaines portions d’ADN plus faciles ou plus difficiles à accéder et à lire pour d’autres molécules. Cibler les HDAC peut donc empêcher les cellules d’apporter des changements importants à leur comportement, comme la croissance incontrôlée des cellules cancéreuses. Mais la façon dont les médicaments agissent sur tous les types de cellules n’est pas bien comprise.
Lors d’expériences sur des cellules isolées, les chercheurs ont découvert que les inhibiteurs d’HDAC empêchaient les fibroblastes de s’activer et de soutenir la tumeur.

De gauche à droite : Yang Dai, Gabriela Estepa, Ruth Yu, Tony Hunter, Michael Downes, Annette Atkins, Yuwenbin Li, Gaoyang Liang, Dylan Nelson et Ronald Evans. Crédit : Institut Salk
Résultats prometteurs de la recherche sur les inhibiteurs HDAC
« L’utilisation d’inhibiteurs d’HDAC a en fait fait deux choses : elle a à la fois diminué les signaux de croissance des fibroblastes vers les cellules cancéreuses et a réduit l’activation et l’accumulation réelles des fibroblastes », explique Gaoyang Liang, premier auteur et associé de recherche dans le laboratoire d’Evans.
Chez la souris, les chercheurs ont découvert qu’un inhibiteur expérimental de l’HDAC, l’entinostat, réduisait l’activation des fibroblastes autour des tumeurs pancréatiques et ralentissait la croissance tumorale. Lorsque les chercheurs ont analysé les données provenant d’humains atteints d’un cancer du pancréas, ils ont découvert quelque chose de similaire : plus les niveaux de HDAC1 dans le tissu fibreux autour de la tumeur d’un patient sont élevés, plus l’issue est mauvaise.
« Cela est en accord avec ce que nous avons observé dans les cellules et chez la souris », explique Downes. « Si vous avez plus d’activités HDAC dans les fibroblastes, le résultat est pire. D’un autre côté, si vous inhibez les HDAC, vous obtenez de meilleurs résultats.
Orientations futures du traitement du cancer
Puisque les inhibiteurs d’HDAC agissent en empêchant les cellules d’activer certains programmes génétiques, les chercheurs voulaient savoir quelles portions d’ADN touchées par les médicaments étaient les plus pertinentes pour l’activation des fibroblastes. Ils ont identifié plusieurs gènes que les inhibiteurs d’HDAC empêchent d’être exprimés, ce qui suggère que de nouveaux médicaments pourraient cibler ces gènes pour empêcher les fibroblastes de s’activer et favoriser la croissance du cancer et de la fibrose.
« On s’est demandé par le passé si le ciblage des fibroblastes était une bonne ou une mauvaise chose dans les cancers du pancréas, car les chercheurs ont montré que si l’on se débarrassait complètement des fibroblastes, cela rendait les cancers plus agressifs », explique Annette Atkins. co-auteur de l’étude et chercheur principal dans le laboratoire d’Evans. « Mais ce que suggèrent nos résultats, c’est que nous n’avons pas besoin de nous en débarrasser ; le simple fait de limiter leur activation est bénéfique.
Des travaux supplémentaires sont nécessaires pour déterminer la meilleure façon d’administrer les inhibiteurs d’HDAC au tissu fibreux dense autour des tumeurs pancréatiques, ainsi que la manière dont ils pourraient être combinés le plus efficacement possible avec d’autres traitements contre le cancer.
Les autres auteurs de l’article sont Tae Gyu Oh, Nasun Hah, Yu Shi, Morgan L. Truitt, Corina E. Antal, Annette R. Atkins, Yuwenbin Li, Antonio FM Pinto, Dylan C. Nelson, Gabriela Estepa, Senada Bashi, Ester. Banayo, Yang Dai, Ruth T. Yu, Tony Hunter et Dannielle D. Engle de Salk ; Hervé Tiriac de l’Université de Californie à San Diego ; Cory Fraser de HonorHealth Scottsdale ; Serina Ng, Haiyong Han et Daniel D. Von Hoff de l’Institut de recherche génomique translationnelle ; et Christopher Lidddle du Université de Sydney.
Le travail a été soutenu par des subventions de la Fondation Lustgarten (y compris le prix 552873), de la Fondation Don et Lorraine Freeberg, d’Ipsen Bioscience, d’une subvention de recherche Stand Up To Cancer-Cancer Research UK-Lustgarten Foundation Pancreatic Cancer Dream Team (SU2C-AACR-DT- 20-16), un Ruth L. Kirschstein National Research Service Award (F32CA217033), une bourse de la Life Sciences Research Foundation, la Damon Runyon Cancer Research Foundation (DRG-2244-16), le Instituts nationaux de la santé (CA082683, 5T32CA009370) et la Fondation de recherche William Isacoff.